CAIU NO ENEM!
CAIU NO VESTIBULAR!
2018
E (FCMSCSP 2018) Os hidretos covalentes geralmente encontram-se no estado gasoso à temperatura ambiente, tais como a amônia (NH3), a arsina (AsH3), a fosfina (PH3), o cloreto de hidrogênio (HCl) e o sulfeto de hidrogênio (H2S). Desses hidretos, o que possui maior temperatura de ebulição é largamente utilizado na refrigeração industrial, especialmente nas indústrias frigoríficas. De acordo com o texto, o hidreto utilizado na refrigeração industrial é
- a) a fosfina.
- b) a arsina.
- c) o cloreto de hidrogênio.
- d) o sulfeto de hidrogênio.
- e) a amônia.
D (CEFET MG 2018) Para o preparo do soro caseiro, é necessário dissolver o cloreto de sódio em água. A dissolução do NaCl em H2O consiste em um
processo____________ , durante o qual, as interações responsáveis por manter os íons separados em meio aquoso são chamadas de_________________.
Os termos que completam, respectivamente, as lacunas são
- a) químico e dipolo-dipolo.
- b) físico e dipolo-dipolo.
- c) químico e íon-dipolo.
- d) físico e íon-dipolo.
A (UFPR 2018) Os mexilhões aderem fortemente às rochas através de uma matriz de placas adesivas que são secretadas pela depressão distal localizada na parte inferior do seu pé. Essas placas adesivas são ricas em proteínas, as quais possuem em abundância o aminoácido LDopa. Esse aminoácido possui, em sua cadeia lateral, um grupo catechol (dihidroxibenzeno), que tem papel essencial na adesão do mexilhão à superfície rochosa. A figura ilustra um esquema da placa adesiva do mexilhão e um esquema da principal interação entre o grupo catechol e a superfície do óxido de titânio, que representa uma superfície rochosa.
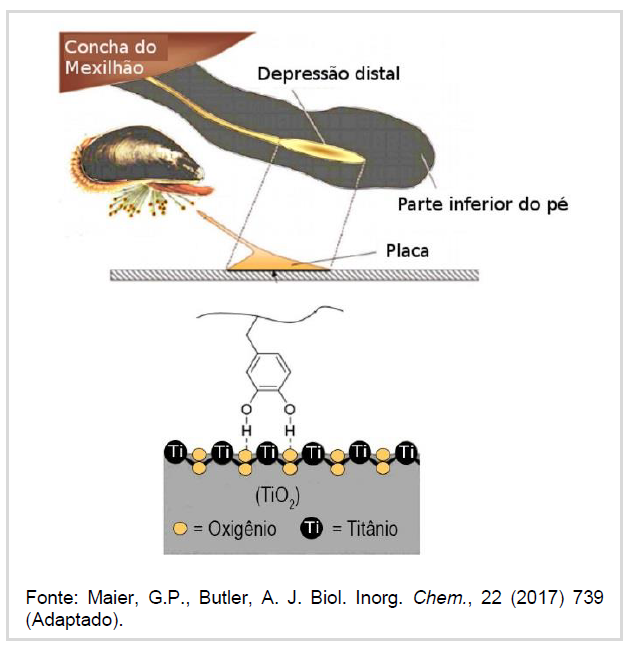
A adesão do mexilhão à rocha deve-se principalmente à interação intermolecular do tipo:
- a) ligação de hidrogênio.
- b) interação íon-dipolo.
- c) dispersão de London.
- d) interação eletrostática.
- e) dipolo permanente-dipolo induzido.
2017
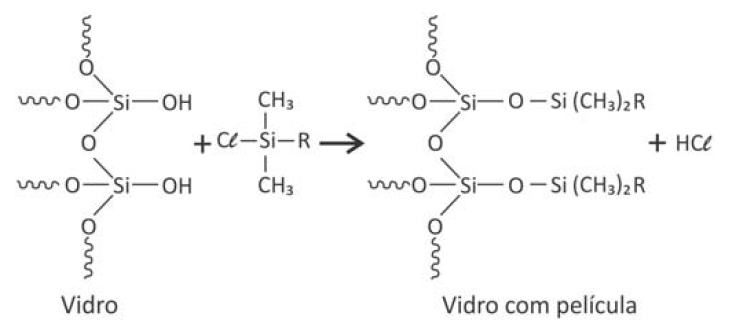
E (FUVEST 2017) Para aumentar o grau de conforto do motorista e contribuir para a segurança em dias chuvosos, alguns materiais podem ser aplicados no para-brisa do veículo, formando uma película que repele a água. Nesse tratamento, ocorre uma transformação na superfície do vidro, a qual pode ser representada pela seguinte equação química não balanceada:
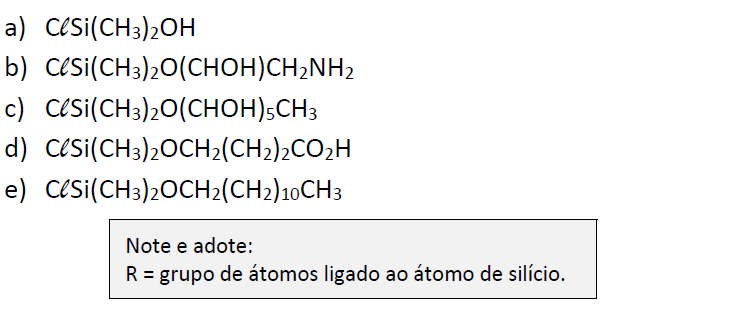
Das alternativas apresentadas, a que representa o melhor material a ser aplicado ao vidro, de forma a evitar o acúmulo de água, é:
2016
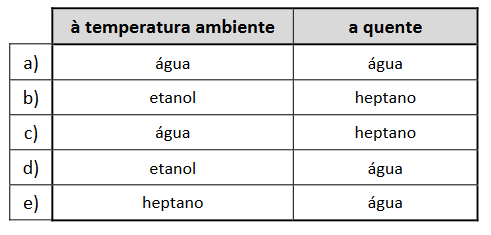
C (FUVEST 2016) Uma estudante recebeu uma amostra de ácido benzoico sólido contendo impurezas. Para purificá-lo, ela optou por efetuar uma recristalização. No procedimento adotado, o sólido deve ser dissolvido em um solvente aquecido, e a solução assim obtida deve ser resfriada. Sendo as impurezas mais solúveis à temperatura ambiente, ao final devem ser obtidos cristais de ácido benzoico puro. Para escolher o solvente apropriado para essa purificação, a estudante fez testes de solubilidade com etanol, água e heptano. Inicialmente, os testes foram efetuados à temperatura ambiente, e a estudante descartou o uso de etanol. A seguir, efetuou testes a quente, e o heptano não se mostrou adequado. Nos testes de solubilidade, a estudante observou a formação de sistema heterogêneo quando tentou dissolver o ácido benzoico impuro em
2010
A (UFC 2010) Sabendo-se que a temperatura de ebulição de uma substância depende da intensidade das forças intermoleculares presentes, assinale a alternativa que corretamente apresenta as substâncias em ordem crescente de temperatura de ebulição.
- a) H2, N2, O2, Br2
- b) N2, Br2, O2, Br2
- c) Br2, O2, N2, H2
- d) Br2, N2, H2, O2
- e) O2, Br2, N2, H2
2009
B (ESPCEX 2009) Assinale a alternativa correta:
- a) A condutividade elétrica dos metais é explicada admitindo-se a existência de nêutrons livres.
- b) O nitrato de sódio é um composto iônico, mas que apresenta ligações covalentes entre o átomo de nitrogênio e os átomos de oxigênio.
- c) Uma molécula com ligações polares pode somente ser classificada, quanto à sua polaridade, como uma molécula polar.
- d) Não existe força de atração entre moléculas apolares.
- e) As forças de atração entre as moléculas do ácido bromídrico são denominadas ligações de hidrogênio.
A (ESPCEX 2009) O dissulfeto de carbono, CS2, é um líquido incolor, volátil, que pode ser produzido em erupções vulcânicas.

Sobre essa substância, considere as seguintes afirmações:
I-A geometria da molécula do dissulfeto de carbono é igual à geometria da molécula da água.
II-O dissulfeto de carbono é um líquido totalmente solúvel em água, nas condições ambientes.
III-As interações entre as moléculas do dissulfeto de carbono são do tipo dipolo induzido-dipolo induzido.
Das afirmações feitas, está(ão) correta(s)
- a) apenas III.
- b) apenas II e III.
- c) apenas I e II.
- d) apenas II.
- e) todas.
2008
D (PUC MG 2008) Análise o gráfico, que apresenta as temperaturas de ebulição de compostos binários do hidrogênio com elementos do grupo 16 (coluna 6A), à pressão de 1 atm.
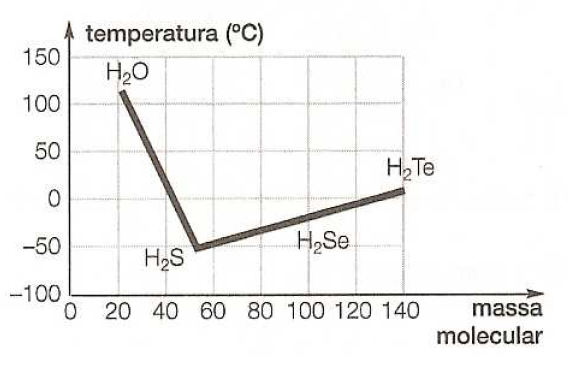
A partir das informações apresentadas, é INCORRETO afirmar que:
- a) a substância mais volátil é o H2S, pois apresenta a menor temperatura de ebulição.
- b) a água apresenta maior temperatura de ebulição, pois apresenta ligações de hidrogênio.
- c) todos os hidretos são gases à temperatura ambiente, exceto a água, que é líquida.
- d) a 100ºC, a água ferve, rompendo as ligações covalentes antes das intermoleculares.