RESUMO
CALOR
Calor é a energia térmica em trânsito, que se transfere do corpo de maior temperatura para o corpo de menor temperatura. Nessa transferência pode ocorrer uma mudança de temperatura (calor sensível) ou uma mudança de estado físico (calor latente).
A substância utilizada como padrão para definir a unidade de quantidade de calor, a caloria (cal), foi a água. Uma caloria é a quantidade de calor necessária para que 1 grama de água pura, sob pressão normal, sofra a elevação de temperatura de 1°C. Como calor é energia, experimentalmente, Joule estabeleceu o equivalente mecânico do calor:
1 cal = 4,186 J
Quando uma transformação ocorre sem troca de calor, dizemos que ela é adiabática.
CALOR SENSÍVEL
Calor sensível é o calor trocado por um sistema e que provoca nesse sistema apenas uma variação de temperatura. As quantidades de calor (Q) recebidas ou cedidas por um corpo são diretamente proporcionais à sua massa (m) e à variação de temperatura (Δθ). Assim:
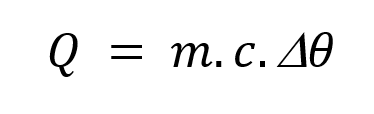 A quantidade de calor, por ser uma forma de energia, é medida no Sistema Internacional de Unidades pelo joule (J). Contudo, por razões históricas as unidades mais usadas na calorimetria para medir a quantidade de calor são a caloria (cal) e a quilocaloria (kcal).
A quantidade de calor, por ser uma forma de energia, é medida no Sistema Internacional de Unidades pelo joule (J). Contudo, por razões históricas as unidades mais usadas na calorimetria para medir a quantidade de calor são a caloria (cal) e a quilocaloria (kcal).
CALOR ESPECÍFICO
Nessa equação, conhecida como equação fundamental da calorimetria, o coeficiente de proporcionalidade c é uma característica do material que constitui o corpo, denominada calor específico. Sua unidade usual é cal/g°C.
Substâncias diferentes apresentam diferentes calores específicos.
Para cada substância, o calor específico depende do estado de agregação. Por exemplo, para a água, nos três estados, temos:
- Sólido (gelo): 0,5 cal/g°C
- Água líquida: 1,0 cal/g°C
- Vapor d’água: 0,5 cal/g°C
O calor específico da água líquida é bastante elevado em comparação com o de outras sustâncias. Na verdade, é um dos maiores da natureza. Por esse motivo, o aquecimento ou o resfriamento da água líquida faz com que ela troque grandes quantidades de calor sofrendo variações de temperatura relativamente pequenas quando comparadas a outras substâncias.
CAPACIDADE TÉRMICA
O produto da massa m de um corpo pelo calor específico c do material que o constitui define a capacidade térmica do corpo:
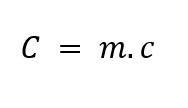 CALOR LATENTE
CALOR LATENTE
Calor latente é o calor trocado por um sistema e que provoca nesse sistema apenas uma mudança de estado físico. Para calcular a quantidade de calor Q a ser trocada por um corpo de massa m para que esse corpo sofra a mudança de estado físico, podemos fazer:
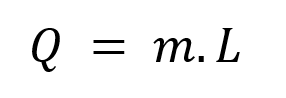 Nessa expressão, temos: m, a massa que sofre a mudança de estado, em gramas (g); L, o calor latente da mudança de estado da substância, em caloria por grama (cal/g); e Q, a quantidade de calor latente a ser trocada em caloria (cal).
Nessa expressão, temos: m, a massa que sofre a mudança de estado, em gramas (g); L, o calor latente da mudança de estado da substância, em caloria por grama (cal/g); e Q, a quantidade de calor latente a ser trocada em caloria (cal).
TROCAS DE CALOR
Quando dois ou mais corpos trocam calor entre si, em um sistema termicamente isolado, até ser atingido o equilíbrio térmico, a soma algébrica das quantidades de calor trocadas é nula.
∑Q = 0 (∑ = somatório)
CAIU NO ENEM!
C (ENEM 2016) Durante a primeira fase do projeto de uma usina de geração de energia elétrica, os engenheiros da equipe de avaliação de impactos ambientais procuram saber se esse projeto está de acordo com as normas ambientais. A nova planta estará localizada à beira de um rio, cuja temperatura média da água é de 25 °C, e usará a sua água somente para refrigeração. O projeto pretende que a usina opere com 1,0 MW de potência elétrica e, em razão de restrições técnicas, o dobro dessa potência será dissipada por seu sistema de arrefecimento, na forma de calor. Para atender a resolução número 430, de 13 de maio de 2011, do Conselho Nacional do Meio Ambiente, com uma ampla margem de segurança, os engenheiros determinaram que a água só poderá ser devolvida ao rio com um aumento de temperatura de, no máximo, 3 °C em relação à temperatura da água do rio captada pelo sistema de arrefecimento. Considere o calor específico da água igual a 4 kJ/(kg °C)
Para atender essa determinação, o valor mínimo do fluxo de água, em kg/s, para a refrigeração da usina deve ser mais próximo de
- a) 42
- b) 84
- c) 167
- d) 250
- e) 500
E (ENEM 2016) Num dia em que a temperatura ambiente é de 37 °C, uma pessoa, com essa mesma temperatura corporal, repousa à sombra. Para regular sua temperatura corporal e mantê-la constante, a pessoa libera calor através da evaporação do suor. Considere que a potência necessária para manter seu metabolismo é 120 W e que, nessas condições, 20% dessa energia é dissipada pelo suor, cujo calor de vaporização é igual ao da água (540 cal/g). Utilize 1 cal igual a 4 J. Após duas horas nessa situação, que quantidade de água essa pessoa deve ingerir para repor a perda pela transpiração?
- a) 0,08 g
- b) 0,44 g
- c) 1,30 g
- d) 1,80 g
- e) 80,0 g
B (ENEM 2013) Aquecedores solares usados em residências têm o objetivo de elevar a temperatura da água até 70°C. No entanto, a temperatura ideal da água para um banho é de 30°C. Por isso, deve-se misturar a água aquecida com a água à temperatura ambiente de um outro reservatório, que se encontra a 25°C.
Qual a razão entre a massa de água quente e a massa de água fria na mistura para um banho à temperatura ideal?
- a) 0,111.
- b) 0,125.
- c) 0,357.
- d) 0,428.
- e) 0,833.
CAIU NO VESTIBULAR!
2018
B (FUVEST 2018) Furacões são sistemas físicos que liberam uma enorme quantidade de energia por meio de diferentes tipos de processos, sendo um deles a condensação do vapor em água. De acordo com o Laboratório Oceanográfico e Meteorológico do Atlântico, um furacão produz, em média, 1,5 cm de chuva por dia em uma região plana de 660 km de raio. Nesse caso, a quantidade de energia por unidade de tempo envolvida no processo de condensação do vapor em água da chuva é, aproximadamente,
Note e adote: π = 3; Calor latente de vaporização da água: 2 x 106 J/kg. Densidade da água: 103 kg/m3; 1 dia = 8,6 x 104 s.
- a) 3,8 x 1015 W.
- b) 4,6 x 1014 W.
- c) 2,1 x 1013 W.
- d) 1,2 x 1012 W.
- e) 1,1 x 1011 W.
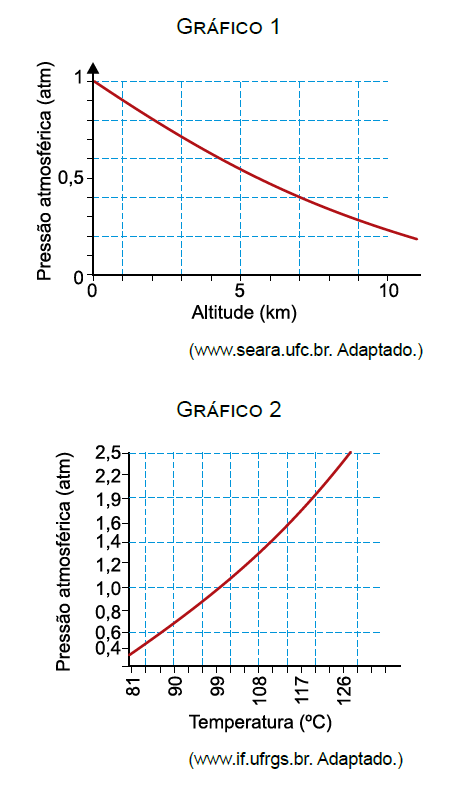
E (UNESP 2018) O gráfico 1 mostra a variação da pressão atmosférica em função da altitude e o gráfico 2 a relação entre a pressão atmosférica e a temperatura de ebulição da água.
Considerando o calor específico da água igual a 1,0 cal/(g · ºC), para aquecer 200 g de água, de 20 ºC até que se inicie a ebulição, no topo do Pico da Neblina, cuja altitude é cerca de
3 000 m em relação ao nível do mar, é necessário fornecer para essa massa de água uma quantidade de calor de, aproximadamente,
- a) 4,0 × 103 cal.
- b) 1,4 × 102 cal.
- c) 1,2 × 103 cal.
- d) 1,2 × 107 cal.
- e) 1,4 × 104 cal.
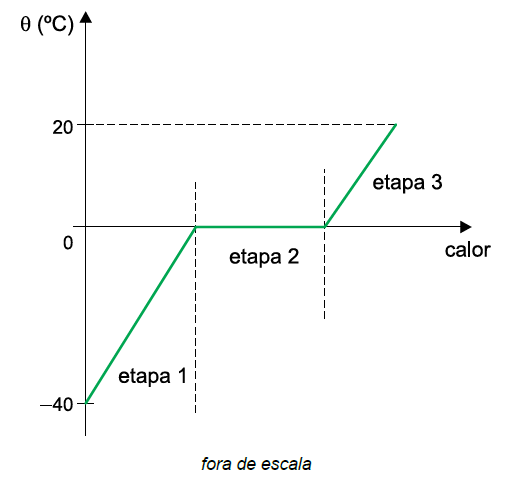
D (FCMSCSP 2018) O gráfico representa parte da curva de aquecimento de determinada massa de gelo, inicialmente a uma temperatura de – 40 ºC, até transformar-se em água líquida a 20 ºC. As etapas 1, 2 e 3 indicadas ocorrem em intervalos de tempo Δt1, Δt2 e Δt3, respectivamente.
Considerando que a energia necessária para provocar essa transformação tenha sido fornecida por uma fonte térmica de potência constante, que todo o calor fornecido por essa fonte tenha sido absorvido pela massa que sofreu a transformação, que o calor específico do gelo é 0,5 cal/(g · ºC), que o calor específico da água líquida é 1 cal/(g · ºC) e que o calor latente de fusão do gelo é 80 cal/g, é correto afirmar que
- a) Δt1 < Δt3 < Δt2
- b) Δt1 > Δt2 > Δt3
- c) Δt1 = Δt2 = Δt3
- d) Δt1 = Δt3 < Δt2
- e) Δt1 = Δt3 > Δt2
E (FMABC 2018) O número aproximado de calorias a serem fornecidas a um cubo de ferro com 1 cm de aresta, para que a temperatura do cubo varie de 59 °F a 338 K, é:
Dados:
Densidade do ferro 8.000 kg/m3
Calor específico do ferro 460 J/kg. °C
1 cal = 4,2 J
- a) 408
- b) 1.877
- c) 70
- d) 187
- e) 44
D (UFRGS 2018) Uma quantidade de calor Q = 56.100,0 J é fornecida a 100 g de gelo que se encontra inicialmente a -10 ºC.
Sendo
o calor específico do gelo cg = 2,1 J/(gºC),
o calor específico da água ca = 4,2 J/(gºC) e
o calor latente de fusão CL = 330,0 J/g,
a temperatura final da água em °C é, aproximadamente,
- a) 83,8.
- b) 60,0.
- c) 54,8.
- d) 50,0.
- e) 37,7.
2017
C (FACULDADE DE MEDICINA ALBERT EINSTEIN 2017) Nos veículos com motores refrigerados por meio líquido, o aquecimento da cabine de passageiros é feito por meio da troca de calor entre o duto que conduz o líquido de arrefecimento que circula pelo motor e o ar externo. Ao final, esse ar que se encontra aquecido, é lançado para o interior do veículo.
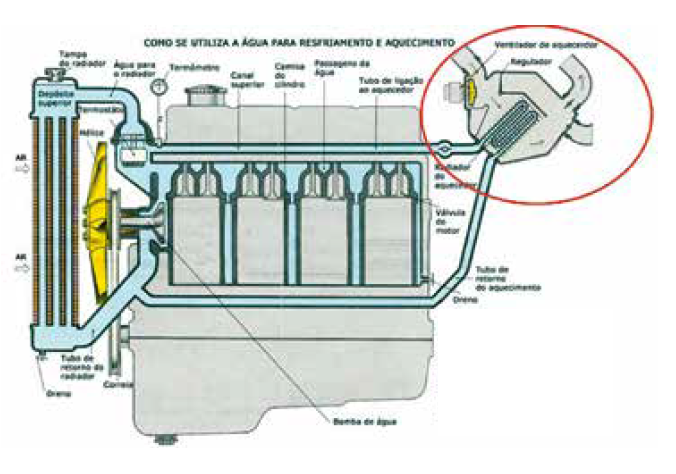
Num dia frio, o ar externo, que está a uma temperatura de 5 °C, é lançado para o interior da cabine, a 30 °C, a uma taxa de 1,5 L/s. Determine a potência térmica aproximada, em watts, absorvida pelo ar nessa troca de calor.
• densidade do ar: 1,2 kg/m3
• calor específico do ar: 0,24 cal.g–1 °C–1
• 1cal = 4,2 J
- a) 20
- b) 25
- c) 45
- d) 60
C (FUVEST 2017) No início do século XX, Pierre Curie e colaboradores, em uma experiência para determinar características do recém-descoberto elemento químico rádio, colocaram uma pequena quantidade desse material em um calorímetro e verificaram que 1,30 grama de água líquida ia do ponto de congelamento ao ponto de ebulição em uma hora. A potência média liberada pelo rádio nesse período de tempo foi, aproximadamente,
- a) 0,06 W
- b) 0,10 W
- c) 0,14W
- d) 0,18 W
- e) 0,22 W
C (UDESC 2017) A queima de 1,000 g de gás de cozinha fornece 6000 cal. A massa de gás que deve ser queimada para elevar a temperatura de meio litro de água de 25,00ºC até 100,0 ºC, e, ainda, produzir a evaporação de 100,0 mL de água, é:
- a) 15,24 g
- b) 15,23 g
- c) 15,25 g
- d) 15,22 g
- e) 15,21 g
B (FACULDADE DE MEDICINA ALBERT EINSTEIN 2017) Sabe-se que um líquido possui calor específico igual a 0,58 cal/g. °C . Com o intuito de descobrir o valor de seu calor latente de vaporização, foi realizado um experimento onde o líquido foi aquecido por meio de uma fonte de potência uniforme, até sua total vaporização, obtendo-se o gráfico abaixo. O valor obtido para o calor latente de vaporização do líquido, em cal/g, está mais próximo de:
- a) 100
- b) 200
- c) 540
- d) 780
2014
(UNESP 2014) Para testar os conhecimentos de termofísica de seus alunos, o professor propõe um exercício de calorimetria no qual são misturados 100 g de água líquida a 20 °C com 200 g de uma liga metálica a 75 °C. O professor informa que o calor específico da água líquida é 1 cal/g°C e o da liga é 0,1 cal/(g.°X) onde X é uma escala arbitrária de temperatura, cuja relação com a escala Celsius está representada no gráfico.
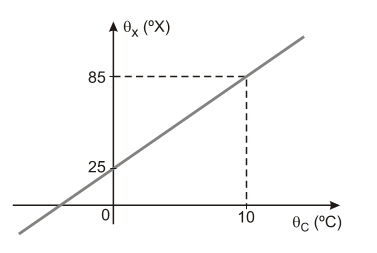 Obtenha uma equação de conversão entre as escalas X e Celsius e, considerando que a mistura seja feita dentro de um calorímetro ideal, calcule a temperatura final da mistura, na escala Celsius, depois de atingido o equilíbrio térmico.
Obtenha uma equação de conversão entre as escalas X e Celsius e, considerando que a mistura seja feita dentro de um calorímetro ideal, calcule a temperatura final da mistura, na escala Celsius, depois de atingido o equilíbrio térmico.
RESPOSTA: 50 °C
C (FUVEST 2014) No sistema cardiovascular de um ser humano, o coração funciona como uma bomba, com potência média de 10 W, responsável pela circulação sanguínea. Se uma pessoa fizer uma dieta alimentar de 2500 kcal diárias, a porcentagem dessa energia utilizada para manter sua circulação sanguínea será, aproximadamente, igual a
- a) 1%
- b) 4%
- c) 9%
- d) 20%
- e) 25%
Note e adote: 1 cal = 4 J
(UFPR 2014) Recentemente houve incidentes com meteoritos na Rússia e na Argentina, mas felizmente os danos foram os menores possíveis, pois, em geral, os meteoritos ao sofrerem atrito com o ar se incineram e desintegram antes de tocar o solo. Suponha que um meteorito de 20 kg formado basicamente por gelo entra na atmosfera, sofre atrito com o ar e é vaporizado completamente antes de tocar o solo. Considere o calor latente de fusão e de vaporização da água iguais a 300 kJ/kg e 2200 kJ/kg, respectivamente. O calor específico do gelo é 0,5 cal/(g°C) e da água líquida é 1,0 cal/(g°C). Admita que 1 cal é igual a 4,2 J. Supondo que o bloco de gelo estava à temperatura de -10 °C antes de entrar na atmosfera, calcule qual é a quantidade de energia fornecida pelo atrito, em joules, para:
- a) aumentar a temperatura do bloco de gelo de -10 °C até gelo a 0 °C.
- b) transformar o gelo que está na temperatura de 0 °C em água líquida a 20 °C.
RESPOSTA: a) 4,2 x105 J; b) 7,68 x 106 J.
(UERJ 2014) A energia consumida por uma pessoa adulta em um dia é igual a 2 400 kcal.
Determine a massa de gelo a 0°C que pode ser totalmente liquefeita pela quantidade de energia consumida em um dia por um adulto. Em seguida, calcule a energia necessária para elevar a temperatura dessa massa de água até 30°C.
RESPOSTA: 30 kg e 900 kcal.
B (UERJ 2014) Um sistema é constituído por uma pequena esfera metálica e pela água contida em um reservatório. Na tabela, estão apresentados dados das partes do sistema, antes de a esfera ser inteiramente submersa na água.
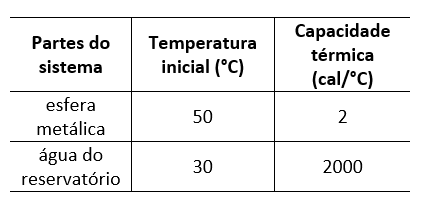 A temperatura final da esfera, em graus Celsius, após o equilíbrio térmico com a água do reservatório, é cerca de:
A temperatura final da esfera, em graus Celsius, após o equilíbrio térmico com a água do reservatório, é cerca de:
- a) 20
- b) 30
- c) 40
- d) 50
A (ACAFE 2014) Com 77% de seu território acima de 300m de altitude e 52% acima de 600m, Santa Catarina figura entre os estados brasileiros de mais forte relevo. Florianópolis, a capital, encontra-se ao nível do mar. Lages, no planalto, varia de 850 a 1200 metros acima do nível do mar. Já o Morro da Igreja situado em Urubici é considerado o ponto habitado mais alto da Região Sul do Brasil.
A tabela abaixo nos mostra a temperatura de ebulição da água nesses locais em função da altitude.
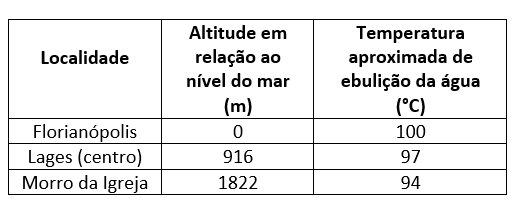 Considere a tabela e os conhecimentos de termologia e analise as afirmações a seguir.
Considere a tabela e os conhecimentos de termologia e analise as afirmações a seguir.
- Em Florianópolis os alimentos preparados dentro da água em uma panela comum são cozidos mais depressa que em Lages, utilizando-se a mesma panela.
- No Morro da Igreja, a camada de ar é menor, por consequência, menor a pressão atmosférica exercida sobre a água, o que implica em um processo de ebulição a uma temperatura inferior a Florianópolis.
- Se quisermos cozinhar em água algum alimento no Morro da Igreja, em uma panela comum, será mais difícil que em Florianópolis, utilizando-se a mesma panela. Isso porque a água irá entrar em ebulição e secar antes mesmo que o alimento termine de cozinhar.
- Se quisermos cozinhar no mesmo tempo em Lages e Florianópolis um mesmo alimento, devemos usar em Florianópolis uma panela de pressão.
Todas as afirmações corretas estão em:
- a) I – II – III
- b) I – II – IV
- c) II – III – IV
- d) III – IV
A (CPS 2014) Uma atração turística da Áustria é Salzburgo, cidade natal de Mozart, construída na Antiguidade graças às minas de sal.
Salzburgo significa castelo do sal, pois nessa cidade está localizada a mina de sal mais antiga do mundo, em atividade desde a Idade do Ferro (1000 a.C.).
No passado, o sal era um importante e quase insubstituível conservante alimentar e, além de cair bem ao nosso paladar, ele é uma necessidade vital, pois, sem o sódio presente no sal, o organismo seria incapaz de transmitir impulsos nervosos ou mover músculos, entre eles o coração.
(terra.com.br/turismo/roteiros/2000/11/10/009.htm Acesso em: 16.08.2013. Adaptado)
O sal também pode ser obtido da água do mar, processo que ocorre em salinas.
 Durante a obtenção de sal em uma salina,
Durante a obtenção de sal em uma salina,
- a) a água sofre evaporação.
- b) a água sofre sublimação.
- c) o sal sofre fusão.
- d) a água e o sal sofrem sublimação.
- e) a água e o sal sofrem solidificação.
2013
B (UERN 2013) Ao trocar calor com o meio ambiente, um corpo de massa 0,5 kg teve sua temperatura reduzida para 20°C, sem sofrer mudança no seu estado físico. Sendo o calor específico da substância que constitui esse corpo igual a 0,175 cal/g °C e a quantidade total de calor transferida igual a 4.900 cal, então, a temperatura inicial do corpo no início do processo era de
- a) 72°C.
- b) 76°C.
- c) 80°C.
- d) 84°C.
B (UERJ 2013) Considere duas amostras, X e Y, de materiais distintos, sendo a massa de X igual a quatro vezes a massa de Y.
As amostras foram colocadas em um calorímetro e, após o sistema atingir o equilíbrio térmico, determinou-se que a capacidade térmica de X corresponde ao dobro da capacidade térmica de Y.
Admita que cX e cY sejam os calores específicos, respectivamente, de X e Y.
A razão cX/cY é dada por:
- a) 1/4
- b) 1/2
- c) 1
- d) 2
B (PUC RJ 2013) Um líquido é aquecido através de uma fonte térmica que provê 50,0 cal por minuto. Observa-se que 200 g deste líquido se aquecem de 20,0 °C em 20,0 min.
Qual é o calor específico do líquido, medido em cal/(g °C)?
- a) 0,0125
- b) 0,25
- c) 5,0
- d) 2,5
- e) 4,0
(UERJ 2013) Uma pessoa, com temperatura corporal igual a 36,7°C, bebe 1/2 litro de água a 15°C.
Admitindo que a temperatura do corpo não se altere até que o sistema atinja o equilíbrio térmico, determine a quantidade de calor, em calorias, que a água ingerida absorve do corpo dessa pessoa.
Utilize: Calor específico da água = 1,0 cal/g°C; Massa específica da água = 1 g/cm3.
RESPOSTA: 10.850 cal
C (UERN 2013) Para se aquecer um corpo constituído por uma substância de calor específico 0,4 cal/g °C foi utilizado uma fonte térmica que fornece 120 cal/min. Se, no aquecimento, o corpo sofreu um aumento de 50 °C em sua temperatura num intervalo de 15 minutos, então, a massa desse corpo e de
- a) 60 g.
- b) 80 g.
- c) 90 g.
- d) 180 g.
E (PUC RJ 2013) Três cubos de gelo de 10,0 g, todos eles a 0,0 °C, são colocados dentro de um copo vazio e expostos ao sol até derreterem completamente, ainda a 0,0 °C.
Calcule a quantidade total de calor requerida para isto ocorrer, em calorias.
Considere o calor latente de fusão do gelo LF = 80 cal/g
- a) 3,7 x 10–1
- b) 2,7 x 101
- c) 1,1 x 102
- d) 8,0 x 102
- e) 2,4 x 103
C (UFPR 2013) O gráfico abaixo, obtido experimentalmente, mostra a curva de aquecimento que relaciona a temperatura de uma certa massa de um líquido em função da quantidade de calor a ele fornecido.
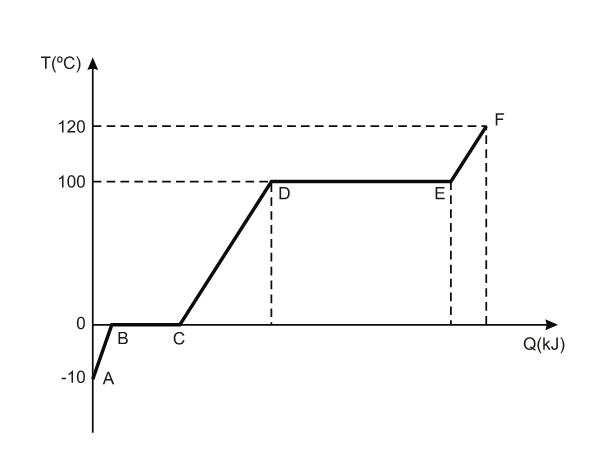 Sabemos que, por meio de gráficos desse tipo, é possível obter os valores do calor específico e do calor latente das substâncias estudadas. Assinale a alternativa que fornece corretamente o intervalo em que se pode obter o valor do calor latente de vaporização desse líquido.
Sabemos que, por meio de gráficos desse tipo, é possível obter os valores do calor específico e do calor latente das substâncias estudadas. Assinale a alternativa que fornece corretamente o intervalo em que se pode obter o valor do calor latente de vaporização desse líquido.
- a) AB
- b) BD
- c) DE
- d) CD
- e) EF
A (FUVEST 2013) Em um recipiente termicamente isolado e mantido a pressão constante, são colocados 138 g de etanol líquido. A seguir, o etanol é aquecido e sua temperatura T é medida como função da quantidade de calor Q a ele transferida. A partir do gráfico de TxQ, apresentado na figura abaixo, pode-se determinar o calor específico molar para o estado líquido e o calor latente molar de vaporização do etanol como sendo, respectivamente, próximos de
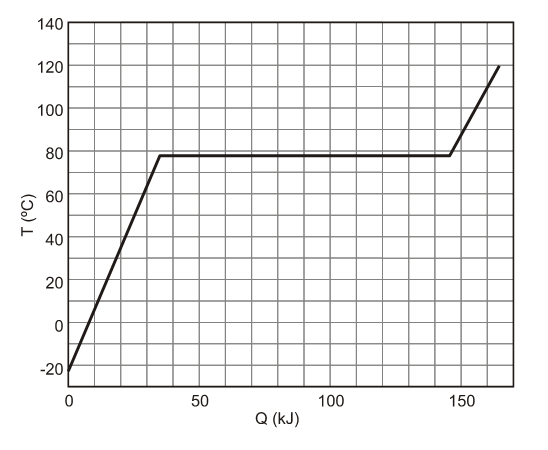 Dados: Fórmula do etanol = C2H5OH; Massas molares = C (12g/mol), H (1g/mol), O (16g/mol).
Dados: Fórmula do etanol = C2H5OH; Massas molares = C (12g/mol), H (1g/mol), O (16g/mol).
- a) 0,12 kJ/(mol°C) e 36 kJ/mol.
- b) 0,12 kJ/(mol°C) e 48 kJ/mol.
- c) 0,21 kJ/(mol°C) e 36 kJ/mol.
- d) 0,21 kJ/(mol°C) e 48 kJ/mol.
- e) 0,35 kJ/(mol°C) e 110 kJ/mol.
(UNIFESP 2013) O gráfico representa o processo de aquecimento e mudança de fase de um corpo inicialmente na fase sólida, de massa igual a 100g.
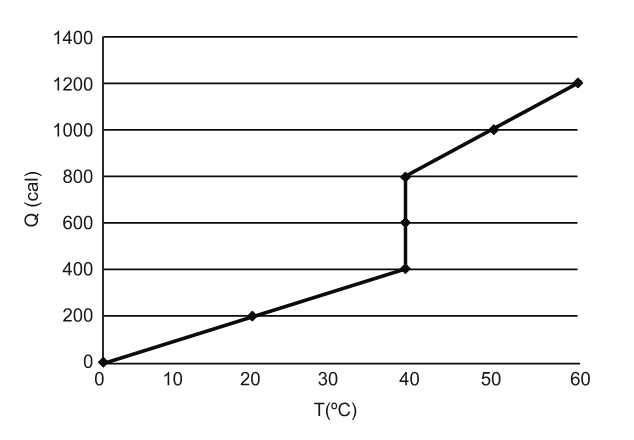 Sendo Q a quantidade de calor absorvida pelo corpo, em calorias, e T a temperatura do corpo, em graus Celsius, determine:
Sendo Q a quantidade de calor absorvida pelo corpo, em calorias, e T a temperatura do corpo, em graus Celsius, determine:
- a) o calor específico do corpo, em cal/(g°C), na fase sólida e na fase líquida.
- b) a temperatura de fusão, em °C, e o calor latente de fusão, em calorias, do corpo.
RESPOSTA: cS = 01 cal/g°C e cL = 0,2 cal/g°C; b) 40 °C e 400 cal.
2012
D (UEL 2012) O homem utiliza o fogo para moldar os mais diversos utensílios. Por exemplo, um forno é essencial para o trabalho do ferreiro na confecção de ferraduras. Para isso, o ferro é aquecido até que se torne moldável. Considerando que a massa de ferro empregada na confecção de uma ferradura é de 0,5 kg, que a temperatura em que o ferro se torna moldável é de 520 ºC e que o calor específico do ferro vale 0,1 cal/gºC, assinale a alternativa que fornece a quantidade de calor, em calorias, a ser cedida a essa massa de ferro para que possa ser trabalhada pelo ferreiro.
Dado: temperatura inicial da ferradura: 20 ºC.
- a) 25
- b) 250
- c) 2500
- d) 25000
- e) 250000
C (UNESP 2012) Clarice colocou em uma xícara 50 mL de café a 80 °C, 100 mL de leite a 50 °C e, para cuidar de sua forma física, adoçou com 2 mL de adoçante líquido a 20 °C. Sabe-se que o calor específico do café vale 1 cal/(g.°C), do leite vale 0,9 cal/(g.°C), do adoçante vale 2 cal/(g.°C) e que a capacidade térmica da xícara é desprezível.
 Considerando que as densidades do leite, do café e do adoçante sejam iguais e que a perda de calor para a atmosfera é desprezível, depois de atingido o equilíbrio térmico, a temperatura final da bebida de Clarice, em °C, estava entre
Considerando que as densidades do leite, do café e do adoçante sejam iguais e que a perda de calor para a atmosfera é desprezível, depois de atingido o equilíbrio térmico, a temperatura final da bebida de Clarice, em °C, estava entre
- a) 75,0 e 85,0.
- b) 65,0 e 74,9.
- c) 55,0 e 64,9.
- d) 45,0 e 54,9.
- e) 35,0 e 44,9.
(UNIFESP 2012) Um calorímetro de capacidade térmica 10 cal/ºC, contendo 500 g de água a 20 ºC, é utilizado para determinação do calor específico de uma barra de liga metálica de 200 g, a ser utilizada como fundo de panelas para cozimento. A barra é inicialmente aquecida a 80 ºC e imediatamente colocada dentro do calorímetro, isolado termicamente. Considerando o calor específico da água 1,0 cal/(g · ºC) e que a temperatura de equilíbrio térmico atingida no calorímetro foi 30 ºC, determine:
- a) a quantidade de calor absorvido pelo calorímetro e a quantidade de calor absorvido pela água.
- b) a temperatura final e o calor específico da barra.
RESPOSTA: a) 100 cal e 5000 cal; b) 30 °C e 0,51 cal/g°C.
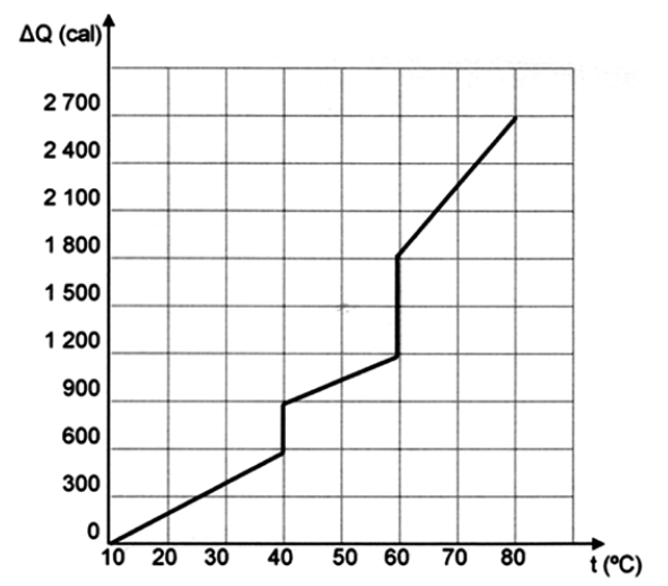
B (MACKENZIE 2012) Um estudante, no laboratório de Física de sua escola, forneceu calor a um corpo de massa 50 g, utilizando uma fonte térmica de potência constante. Com as medidas obtidas, construiu o gráfico ao lado, que representa a quantidade de calor ΔQ recebida pelo corpo em função de sua temperatura t.
Analisando o gráfico, pode-se afirmar que o calor específico, no estado sólido e o calor latente de vaporização da substância que constitui o corpo, valem, respectivamente,
- a) 0,6 cal/(g.°C) e 12 cal/g
- b) 0,4 cal/(g.°C) e 12 cal/g
- c) 0,4 cal/(g.°C) e 6 cal/g
- d) 0,3 cal/(g.°C) e 12 cal/g
- e) 0,3 cal/(g.°C) e 6 cal/g
2011
A (UEL 2011) Um martelo de massa M = 1, 2 kg, com velocidade de módulo 6, 5 m/s, golpeia um prego de massa m = 14 g e para, após cada impacto. Considerando que o prego absorve toda a energia das marteladas, uma estimativa do aumento da temperatura do prego, gerado pelo impacto de dez marteladas sucessivas, fornecerá o valor aproximado de:
Dado: Calor específico do ferro c = 450J/kgºC
- a) 40 ºC
- b) 57 ºC
- c) 15 ºK
- d) 57 ºK
- e) 15 ºF
C (UNESP 2011) Foi realizada uma experiência em que se utilizava uma lâmpada de incandescência para, ao mesmo tempo, aquecer 100 g de água e 100 g de areia. Sabe-se que, aproximadamente, 1 cal = 4 J e que o calor específico da água é de 1 cal/g ºC e o da areia é 0,2 cal/g ºC. Durante 1 hora, a água e a areia receberam a mesma quantidade de energia da lâmpada, 3,6 kJ, e verificou-se que a água variou sua temperatura em 8 ºC e a areia em 30 ºC. Podemos afirmar que a água e a areia, durante essa hora, perderam, respectivamente, a quantidade de energia para o meio, em kJ, igual a
- a) 0,4 e 3,0.
- b) 2,4 e 3,6.
- c) 0,4 e 1,2.
- d) 1,2 e 0,4.
- e) 3,6 e 2,4.
(UFPE 2011) Um estudante precisa de três litros de água a temperatura de 37 ºC. Ele já dispõe de dois litros de água a 17 ºC. A que temperatura, em ºC, ele deve aquecer o litro de água a ser misturado com o volume já disponível? Considere a existência de trocas térmicas apenas entre os volumes de água na mistura.
RESPOSTA: 77 °C.
E (UFTM 2011) Dona Joana é cozinheira e precisa de água a 80 ºC para sua receita. Como não tem um termômetro, decide misturar água fria, que obtém de seu filtro, a 25 ºC, com água fervente. Só não sabe em que proporção deve fazer a mistura. Resolve, então, pedir ajuda a seu filho, um excelente aluno em física. Após alguns cálculos, em que levou em conta o fato de morarem no litoral, e em que desprezou todas as possíveis perdas de calor, ele orienta sua mãe a misturar um copo de 200 mL de água do filtro com uma quantidade de água fervente, em mL, igual a
- a) 800
- b) 750
- c) 625
- d) 600
- e) 550
B (IFSP 2011) A temperatura normal do corpo humano é de 36,5 °C. Considere uma pessoa de 80 kg de massa e que esteja com febre a uma temperatura de 40°C. Admitindo que o corpo seja feito basicamente de água, podemos dizer que a quantidade de energia, em quilocalorias (kcal), que o corpo dessa pessoa gastou para elevar sua temperatura até este estado febril, deve ser mais próxima de
Dado: calor específico da água c = 1,0 cal/g°C
- a) 200
- b) 280
- c) 320
- d) 360
- e) 420
E (IFTO 2011-2) Um bloco de chumbo de massa igual a 0,2 kg encontra-se à temperatura de 27 °C e sob pressão de 1 atm. A quantidade de calorias que deve ser fornecida ao bloco para que ele sofra fusão total é igual a:
Dados: calor específico do chumbo = 0,031 cal/g°C; calor latente de fusão do chumbo = 5,5 cal/g; temperatura de fusão do chumbo = 327°C.
- a) 3.060 cal
- b) 2.860 cal
- c) 3.960 cal
- d) 2.690 cal
- e) 2.960 cal
C (UNESP 2011) Uma bolsa térmica com 500 g de água à temperatura inicial de 60 ºC é empregada para tratamento da dor nas costas de um paciente. Transcorrido um certo tempo desde o início do tratamento, a temperatura da água contida na bolsa é de 40 ºC. Considerando que o calor específico da água é 1 cal/(g ∙ºC), e supondo que 60% do calor cedido pela água foi absorvido pelo corpo do paciente, a quantidade de calorias recebidas pelo paciente no tratamento foi igual a:
- a) 2 000.
- b) 4 000.
- c) 6 000.
- d) 8 000.
- e) 10 000.
(UFPE 2011) Uma pessoa que deseja beber água fresca, mistura duas porções, de 150 ml cada; uma, à temperatura de 5 ºC, e a outra à temperatura de 31 ºC. Após algum tempo, ela verifica que a temperatura da mistura é de 16 ºC. Determine o módulo da quantidade de calor que é cedido para o ambiente (sala mais copo). Expresse sua resposta em unidades de 102 calorias.
RESPOSTA: 6
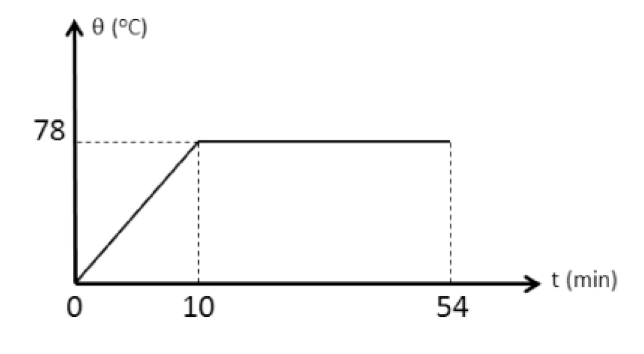
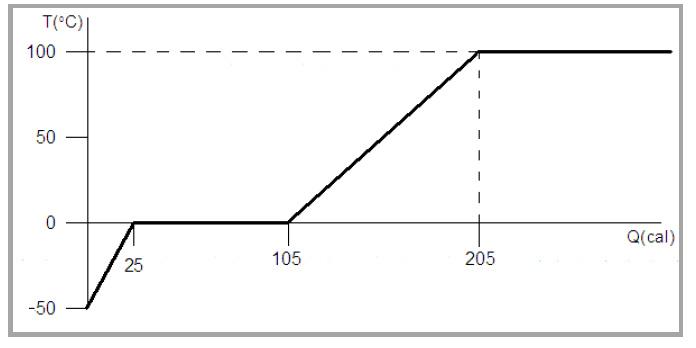
B (UFRN 2011) A existência da água em seus três estados físicos, sólido, líquido e gasoso, torna nosso Planeta um local peculiar em relação aos outros Planetas do Sistema Solar. Sem tal peculiaridade, a vida em nosso Planeta seria possivelmente inviável. Portanto, conhecer as propriedades físicas da água ajuda a melhor utilizá-la e assim contribuir para a preservação do Planeta. Na superfície da Terra, em altitudes próximas ao nível do mar, os estados físicos da água estão diretamente relacionados à sua temperatura conforme mostrado no Gráfico a seguir.
Esse Gráfico representa o comportamento de uma massa de 1,0 g de gelo a uma temperatura inicial de -50 °C, colocada em um calorímetro que, ligado a um computador, permite determinar a temperatura da água em função da quantidade de calor que lhe é cedida.
Observando-se o Gráfico, pode-se concluir que a quantidade de calor necessária para liquefazer a massa de 1,0 g de água e elevar sua temperatura de 0 °C até 100 °C é, respectivamente,
- a) 105 cal e 80 cal.
- b) 105 cal e 100 cal.
- c) 80 cal e 105 cal.
- d) 100 cal e 105 cal.
2009
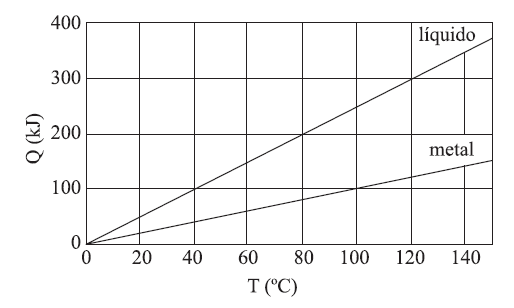
E (UNIFESP 2009) O gráfico mostra as curvas de quantidade de calor absorvido em função da temperatura para dois corpos distintos: um bloco de metal e certa quantidade de líquido.
O bloco de metal, a 115 ºC, foi colocado em contato com o líquido, a 10 ºC, em um recipiente ideal e isolado termicamente. Considerando que ocorreu troca de calor somente entre o bloco e o líquido, e que este não se evaporou, o equilíbrio térmico ocorrerá a
- a) 70 ºC.
- b) 60 ºC.
- c) 55 ºC.
- d) 50 ºC.
- e) 40 ºC.