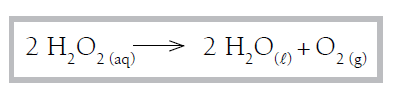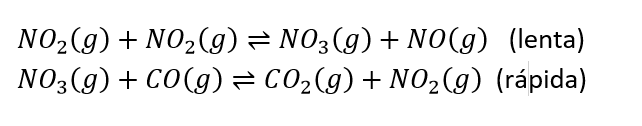CAIU NO ENEM!
C (ENEM 2ª aplicação 2010) Alguns fatores podem alterar a rapidez das reações químicas. A seguir, destacam-se três exemplos no contexto da preparação e da conservação de alimentos:
- A maioria dos produtos alimentícios se conserva por muito mais tempo quando submetidos à refrigeração. Esse procedimento diminui a rapidez das reações que contribuem para a degradação de certos alimentos.
- Um procedimento muito comum utilizado em práticas de culinária é o corte dos alimentos para acelerar o seu cozimento, caso não se tenha uma panela de pressão.
- Na preparação de iogurtes, adicionam-se ao leite bactérias produtoras de enzimas que aceleram as reações envolvendo açúcares e proteínas lácteas.
Com base no texto, quais são os fatores que influenciam a rapidez das transformações químicas relacionadas aos exemplos 1, 2 e 3, respectivamente?
- a) Temperatura, superfície de contato e concentração.
- b) Concentração, superfície de contato e catalisadores.
- c) Temperatura, superfície de contato e catalisadores.
- d) Superfície de contato, temperatura e concentração.
- e) Temperatura, concentração e catalisadores.
B (ENEM PPL 2013) Há processos industriais que envolvem reações químicas na obtenção de diversos produtos ou bens consumidos pelo homem. Determinadas etapas de obtenção desses produtos empregam catalisadores químicos tradicionais, que têm sido, na medida do possível, substituídos por enzimas. Em processos industriais, uma das vantagens de se substituírem os catalisadores químicos tradicionais por enzimas decorre do fato de estas serem
- a) consumidas durante o processo.
- b) compostos orgânicos e biodegradáveis.
- c) inespecíficas para os substratos.
- d) estáveis em variações de temperatura.
- e) substratos nas reações químicas.
B (ENEM PPL 2013) A hematita (a-Fe2O3), além de ser utilizada para obtenção do aço, também é utilizada como um catalisador de processos químicos, como na síntese da amônia, importante matéria-prima da indústria agroquímica.
MEDEIROS, M. A. F. Química Nova na Escola, São Paulo, v. 32, n. 3, ago. 2010 (adaptado).
O uso da hematita viabiliza economicamente a produção da amônia, porque
- a) diminui a rapidez da reação.
- b) diminui a energia de ativação da reação.
- c) aumenta a variação da entalpia da reação.
- d) aumenta a quantidade de produtos formados.
- e) aumenta o tempo do processamento da reação.
C (ENEM 2002) O milho verde recém-colhido tem um sabor adocicado. Já o milho verde comprado na feira, um ou dois dias depois de colhido, não é mais tão doce, pois cerca de 50% dos carboidratos responsáveis pelo sabor adocicado são convertidos em amido nas primeiras 24 horas.
Para preservar o sabor do milho verde pode-se usar o seguinte procedimento em três etapas:
1o descascar e mergulhar as espigas em água fervente por alguns minutos;
2o resfriá-las em água corrente;
3o conservá-las na geladeira.
A preservação do sabor original do milho verde pelo procedimento descrito pode ser explicada pelo seguinte argumento:
- a) O choque térmico converte as proteínas do milho em amido até a saturação; este ocupa o lugar do amido que seria formado espontaneamente.
- b) A água fervente e o resfriamento impermeabilizam a casca dos grãos de milho, impedindo a difusão de oxigênio e a oxidação da glicose.
- c) As enzimas responsáveis pela conversão desses carboidratos em amido são desnaturadas pelo tratamento com água quente.
- d) Micro-organismos que, ao retirarem nutrientes dos grãos, convertem esses carboidratos em amido, são destruídos pelo aquecimento.
- e) O aquecimento desidrata os grãos de milho, alterando o meio de dissolução onde ocorreria espontaneamente a transformação desses carboidratos em amido.
CAIU NO VESTIBULAR!
2018
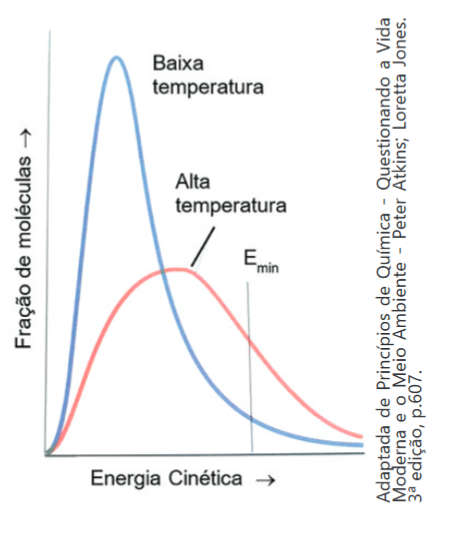 Sobre a influência do aumento da temperatura para a formação do complexo ativado e na rapidez das reações químicas foram feitas as afirmações abaixo
Sobre a influência do aumento da temperatura para a formação do complexo ativado e na rapidez das reações químicas foram feitas as afirmações abaixo- Com o aumento da temperatura, um maior número de moléculas irá possuir energia suficiente para atingir o estado de ativação.
- O aumento da temperatura aumenta o número de colisões entre as moléculas dos reagentes e, consequentemente, aumentam os choques não eficazes e os eficazes.
- Para que ocorra a formação do complexo ativado, as moléculas dos reagentes devem possuir uma quantidade de energia no mínimo igual à energia de ativação e, portanto, o aumento de temperatura favorece a formação do complexo ativado.
- A formação do complexo ativado ocorre apenas em reações endotérmicas.
- a) Apenas I.
- b) I e II.
- c) I, II, e III.
- d) Todas.
- a) reduzida a um quarto.
- b) reduzida à metade.
- c) mantida constante.
- d) duplicada.
- e) quadruplicada.
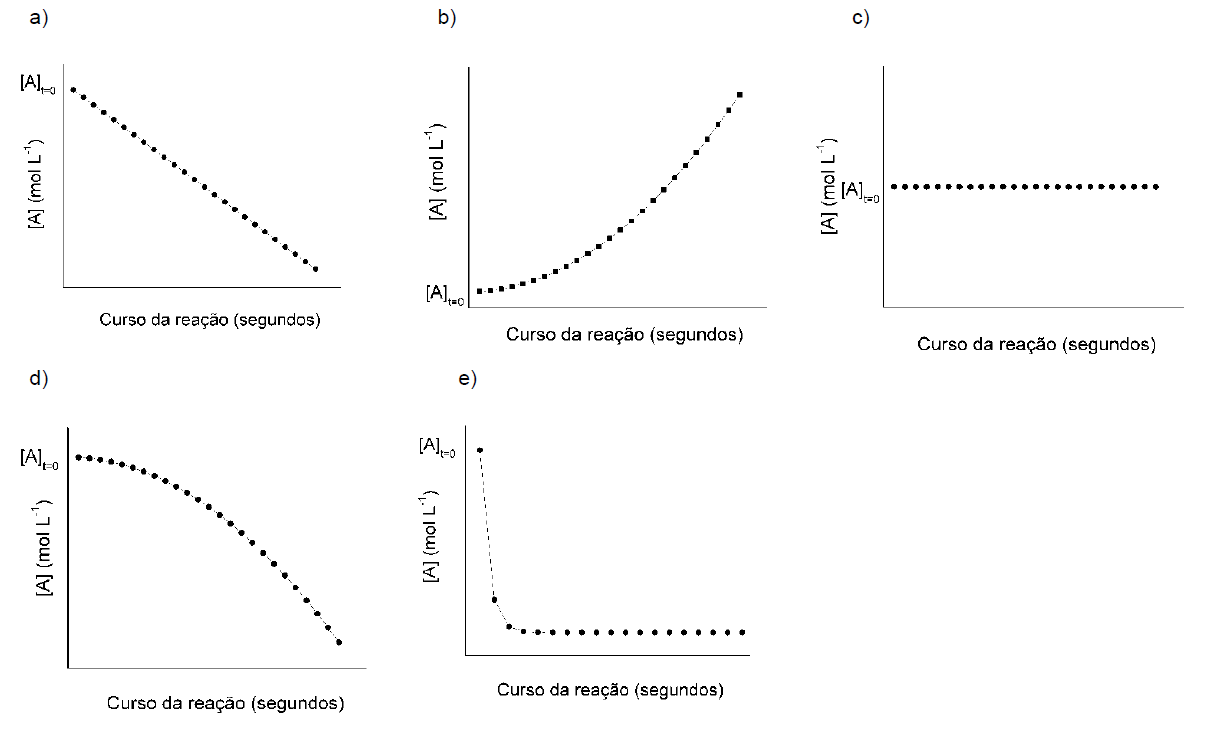
E (UFPR 2018) Uma certa espécie química A, quando em solução, reage rapidamente com oxigênio molecular dissolvido e é degradada por ele. A velocidade dessa reação segue a lei da velocidade v = k[A].
O gráfico que representa de forma adequada a relação entre a concentração da espécie A em solução com o decorrer da reação é:
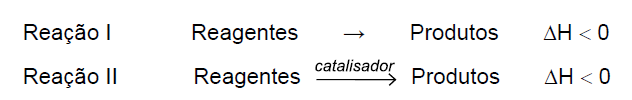
B (FGV SP 2018) Em um experimento de química, são realizadas duas reações, I e II, empregando-se os mesmos reagentes nas mesmas condições de temperatura e pressão. Essas reações ocorrem em uma única etapa.
Assinale a alternativa que apresenta os gráficos que descrevem, correta e respectivamente, as reações I e II.
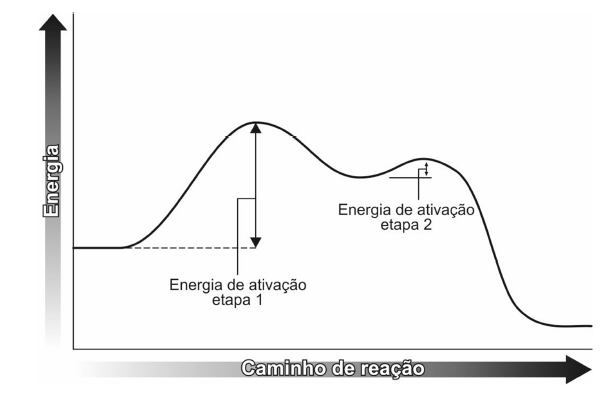
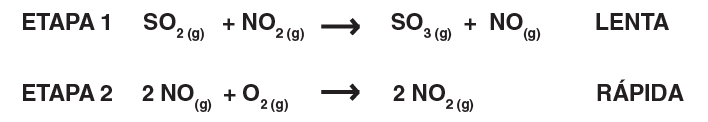
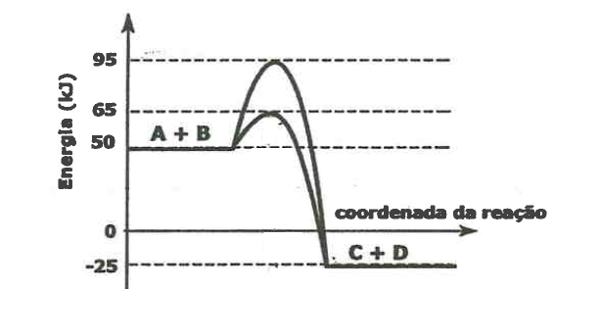
C (FMABC 2018) Considere as seguintes informações sobre a formação de ácido sulfúrico atmosférico, precursor da chuva ácida,
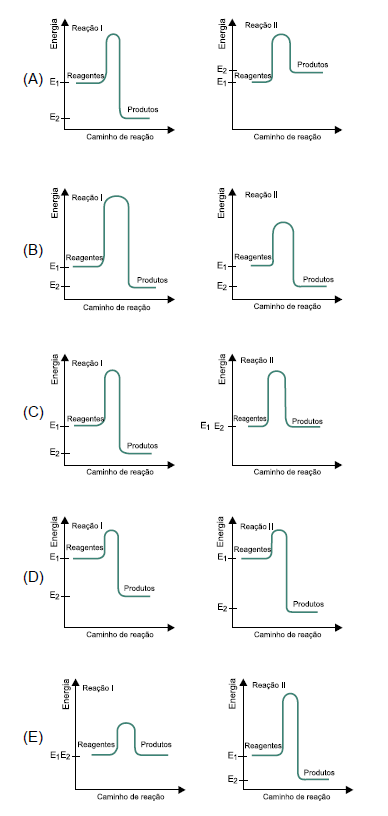
Considere o gráfico das etapas do processo de formação do H2SO4 (l).
Analisando o gráfico, conclui-se que a etapa lenta do processo é a
- a) 2, porque apresenta menor energia de ativação.
- b) 2, porque apresenta maior energia de ativação.
- c) 1, porque apresenta maior energia de ativação.
- d) 1, e para retardá-la pode-se utilizar um catalisador.
- e) 2, e para acelerá-la pode-se utilizar um catalisador.
2017
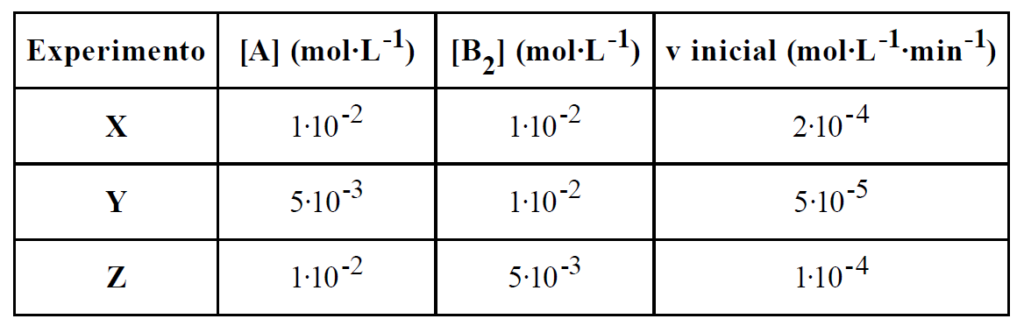
- As ordens de reação para os reagentes A e B2, respectivamente, são 2 e 1.
- A equação cinética da velocidade para o processo pode ser representada pela equação v = k∙[A]2∙[B2].
- A constante cinética da velocidade k tem valor igual a 200.
- a) nenhuma afirmativa é certa.
- b) apenas a afirmativa I está certa.
- c) apenas as afirmativas I e II estão certas.
- d) apenas as afirmativas II e III estão certas.
- e) todas as afirmativas estão certas.
B (PUCCAMP 2017) Para mostrar a diferença da rapidez da reação entre ferro e ácido clorídrico, foi utilizado o ferro em limalha e em barra. Pingando dez gotas de ácido clorídrico 1,0 mol.L-1 em cada material de ferro, espera-se que a reação seja
- a) mais rápida no ferro em barra porque a superfície de contato é menor.
- b) mais rápida no ferro em limalha porque a superfície de contato é maior.
- c) igual, pois a concentração e a quantidade do ácido foram iguais.
- d) mais lenta no ferro em limalha porque a superfície de contato é menor.
- e) mais lenta no ferro em barra porque a superfície de contato é maior.
D (UPE-ssa 2 2017) O gráfico a seguir indica a decomposição de azida de sódio em nitrogênio gasoso, que é a reação usada para inflar airbags, quando ocorrem acidentes com veículos automotivos. Por ser um perigo potencial, o sódio metálico formado é convertido por reação com outros reagentes, tais como o KNO3 e a SiO2.
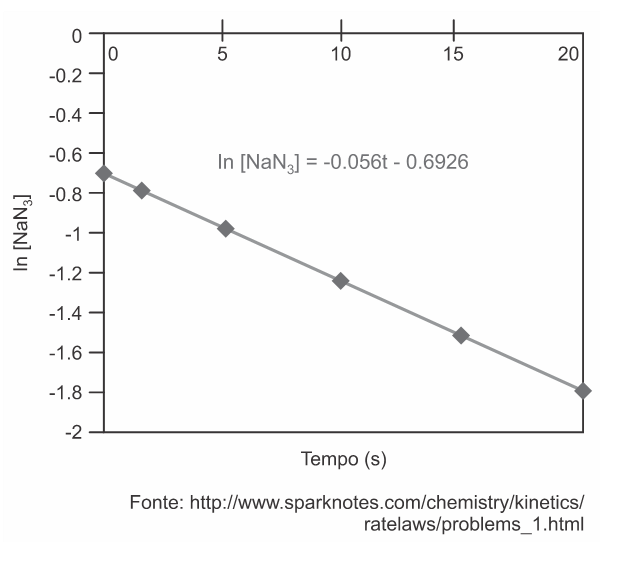 Sobre esse processo, é CORRETO afirmar que a
Sobre esse processo, é CORRETO afirmar que a
- a) reação é de segunda ordem.
- b) reação ocorre em uma velocidade lenta.
- c) velocidade é dada pela taxa de consumo do N2.
- d) constante de velocidade, k, é igual a 0,056 s-1.
- e) concentração de NaN3 aumenta ao longo dos 20 s.
(FEPAR 2017)
 Um dos grandes problemas ambientais nas últimas décadas tem sido a redução da camada de ozônio. Uma das reações que contribui para a destruição dessa camada é expressa pela seguinte equação:
Um dos grandes problemas ambientais nas últimas décadas tem sido a redução da camada de ozônio. Uma das reações que contribui para a destruição dessa camada é expressa pela seguinte equação:
![]() Os dados abaixo foram coletados em laboratório, a 25 °C.
Os dados abaixo foram coletados em laboratório, a 25 °C.
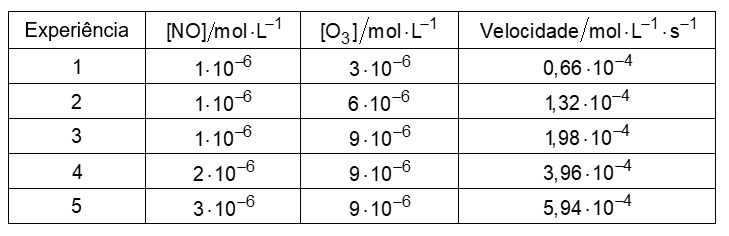 Considere os dados e avalie as afirmativas.
Considere os dados e avalie as afirmativas.
( ) A expressão da lei da velocidade é v = k ∙ [NO] ∙ [O3]2.
( ) A reação é de segunda ordem.
( ) O valor da constante da velocidade é 7,3 ∙ 1014.
( ) A velocidade fica inalterada se variarmos igualmente as concentrações de NO e O3.
( ) Se o uso de um catalisador provocasse o aumento de velocidade da reação, isso seria consequência da diminuição da energia de ativação do sistema.
RESPOSTA: F – V – F – F – V.
A (UEMG 2017) Uma reação química hipotética é representada pela seguinte equação:
A(g) + B(g) → C(g) + D(g) e ocorre em duas etapas:
A(g) → E(g) + D(g) (Etapa lenta)
E(g) + B(g) → C(g) (Etapa rápida)
A lei da velocidade da reação pode ser dada por
- a) v=k.[A]
- b) v=k.[A][B]
- c) v=k.[C][D]
- d) v=k.[E][B]
2016
E (UFRGS 2016) Na reação
![]() a lei cinética é de segunda ordem em relação ao dióxido de nitrogênio e de ordem zero em relação ao monóxido de carbono. Quando, simultaneamente, dobrar-se a concentração de dióxido de nitrogênio e reduzir-se a concentração de monóxido de carbono pela metade, a velocidade da reação
a lei cinética é de segunda ordem em relação ao dióxido de nitrogênio e de ordem zero em relação ao monóxido de carbono. Quando, simultaneamente, dobrar-se a concentração de dióxido de nitrogênio e reduzir-se a concentração de monóxido de carbono pela metade, a velocidade da reação
- a) será reduzida a um quarto do valor anterior.
- b) será reduzida à metade do valor anterior.
- c) não se alterará.
- d) duplicará.
- e) aumentará por um fator de 4 vezes.
2015
B (FUVEST 2015) O eugenol, extraído de plantas, pode ser transformado em seu isômero isoeugenol, muito utilizado na indústria de perfumes. A transformação pode ser feita em solução alcoólica de KOH.
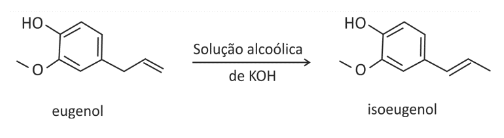 Foram feitos três experimentos de isomerização, à mesma temperatura, empregando-se massas iguais de eugenol e volumes iguais de soluções alcoólicas de KOH de diferentes concentrações. O gráfico a seguir mostra a porcentagem de conversão do eugenol em isoeugenol em função do tempo, para cada experimento.
Foram feitos três experimentos de isomerização, à mesma temperatura, empregando-se massas iguais de eugenol e volumes iguais de soluções alcoólicas de KOH de diferentes concentrações. O gráfico a seguir mostra a porcentagem de conversão do eugenol em isoeugenol em função do tempo, para cada experimento.
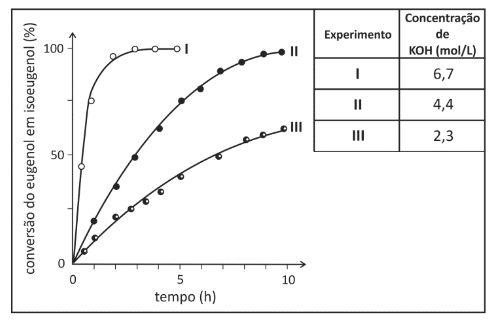 Analisando-se o gráfico, pode-se concluir corretamente que
Analisando-se o gráfico, pode-se concluir corretamente que
- a) a isomerização de eugenol em isoeugenol é exotérmica.
- b) o aumento da concentração de KOH provoca o aumento da velocidade da reação de isomerização.
- c) o aumento da concentração de KOH provoca a decomposição do isoeugenol.
- d) a massa de isoeugenol na solução, duas horas após o início da reação, era maior do que a de eugenol em dois dos experimentos realizados.
- e) a conversão de eugenol em isoeugenol, três horas após o início da reação, era superior a 50% nos três experimentos.
2013
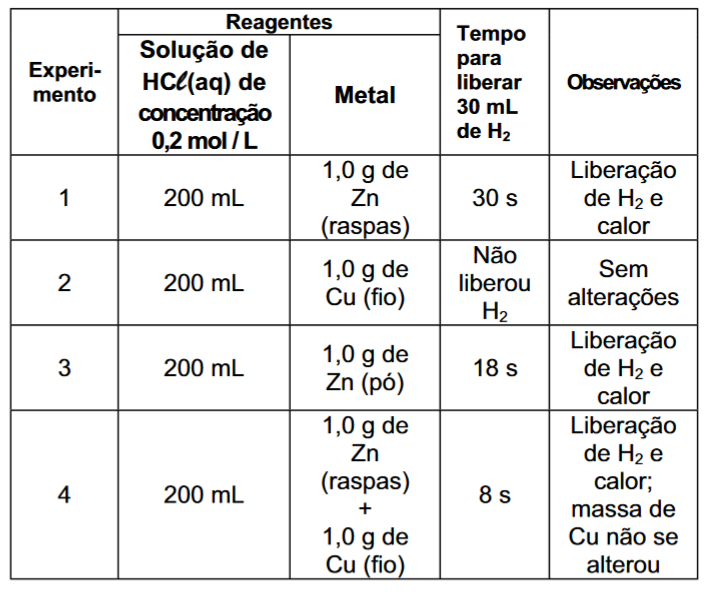
D (FUVEST 2013) Quando certos metais são colocados em contato com soluções ácidas, pode haver formação de gás hidrogênio. Abaixo, segue uma tabela elaborada por uma estudante de Química, contendo resultados de experimentos que ela realizou em diferentes condições.
Após realizar esses experimentos, a estudante fez três afirmações:
- A velocidade da reação de Zn com ácido aumenta na presença de Cu.
- O aumento na concentração inicial do ácido causa o aumento da velocidade de liberação do gás H2.
- Os resultados dos experimentos 1 e 3 mostram que, quanto maior o quociente superfície de contato/massa total de amostra de Zn, maior a velocidade de reação.
Com os dados contidos na tabela, a estudante somente poderia concluir o que se afirma em
- a) I.
- b) II.
- c) I e II.
- d) I e III.
- e) II e III.
2011
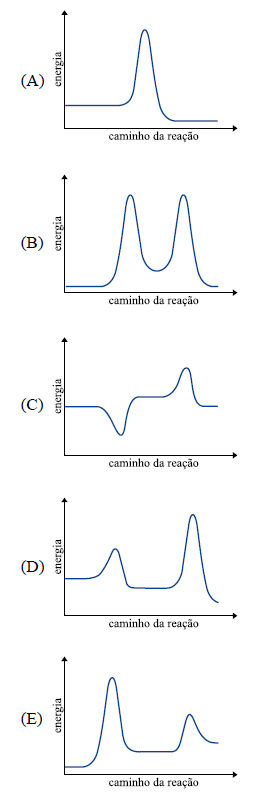
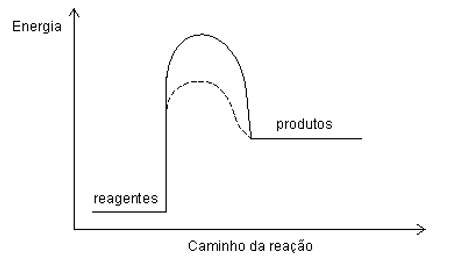
D (UNESP 2011) Um professor de química apresentou a figura como sendo a representação de um sistema reacional espontâneo.
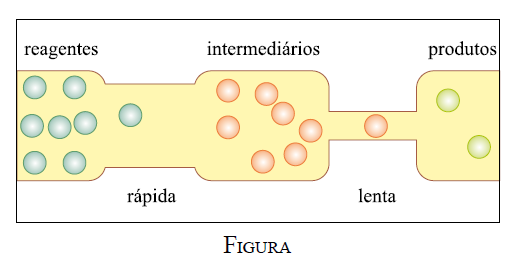
Em seguida, solicitou aos estudantes que traçassem um gráfico da energia em função do caminho da reação, para o sistema representado.
Para atender corretamente à solicitação do professor, os estudantes devem apresentar um gráfico como o que está representado em
B (FUVEST 2011) Ao abastecer um automóvel com gasolina, é possível sentir o odor do combustível a certa distância da bomba. Isso significa que, no ar, existem moléculas dos componentes da gasolina, que são percebidas pelo olfato. Mesmo havendo, no ar, moléculas de combustível e de oxigênio, não há combustão nesse caso. Três explicações diferentes foram propostas para isso:
- As moléculas dos componentes da gasolina e as do oxigênio estão em equilíbrio químico e, por isso, não reagem.
- À temperatura ambiente, as moléculas dos componentes da gasolina e as do oxigênio não têm energia suficiente para iniciar a combustão.
- As moléculas dos componentes da gasolina e as do oxigênio encontram-se tão separadas que não há colisão entre elas.
Dentre as explicações, está correto apenas o que se propõe em
- a) I.
- b) II.
- c) III.
- d) I e II.
- e) II e III.
2010
D (UFC 2010) Metano (CH4) é o gás produzido a partir da biomassa, e a sua queima na indústria, para obtenção de energia térmica, corresponde à seguinte reação:
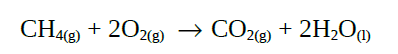 Se a velocidade de consumo do metano é 0,01 mol min–1, assinale a alternativa que corretamente expressa o número de moles de CO2 produzido durante uma hora de reação.
Se a velocidade de consumo do metano é 0,01 mol min–1, assinale a alternativa que corretamente expressa o número de moles de CO2 produzido durante uma hora de reação.
- a) 0,3
- b) 0,4
- c) 0,5
- d) 0,6
- e) 0,7
2009
A (PUC MG 2009) Considere a seguir o diagrama energético de uma reação:
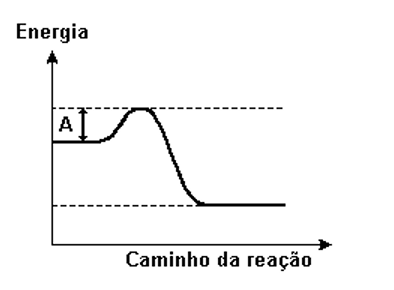 O valor representado por A corresponde:
O valor representado por A corresponde:
- a) à energia de ativação da reação.
- b) à entalpia da reação.
- c) à entropia da reação.
- d) à velocidade da reação.
C (ESPCEX 2009) Considere a sequência de reações associadas ao processo de oxidação do dióxido de enxofre.
A alternativa que apresenta corretamente o catalisador e a expressão da lei da velocidade para a reação global é:
- a] catalisador NO e v=k·[SO2]2 ·[O2]
- b] catalisador NO2 e v=k·[SO2]2 ·[O2]
- c] catalisador NO2 e v=k·[SO2]·[NO2]
- d] catalisador NO e v=k·[SO2]·[NO2]
- e] catalisador O2 e v=k·[SO2]·[NO2]
2008
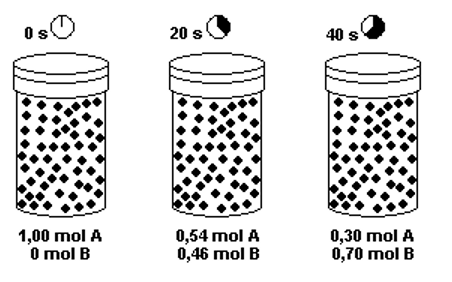
(VELOCIDADE DE REAÇÃO) B (PUC RIO 2008) Considere a reação de decomposição da substância A na substância B e as espécies a cada momento segundo o tempo indicado.
Sobre a velocidade dessa reação, é correto afirmar que a velocidade de:
- a) decomposição da substância A, no intervalo de tempo de 0 a 20 s, é 0,46 mol s-1.
- b) decomposição da substância A, no intervalo de tempo de 20 a 40 s, é 0,012 mol s-1.
- c) decomposição da substância A, no intervalo de tempo de 0 a 40 s, é 0,035 mol s-1.
- d) formação da substância B, no intervalo de tempo de 0 a 20 s, é 0,46 mol s-1.
- e) formação da substância B, no intervalo de tempo de 0 a 40 s, é 0,70 mol s-1.
(VELOCIDADE DE REAÇÃO) A (UERJ 2009) A água oxigenada consiste em uma solução aquosa de peróxido de hidrogênio, que se decompõe, sob a ação da luz e do calor, segundo a equação química:
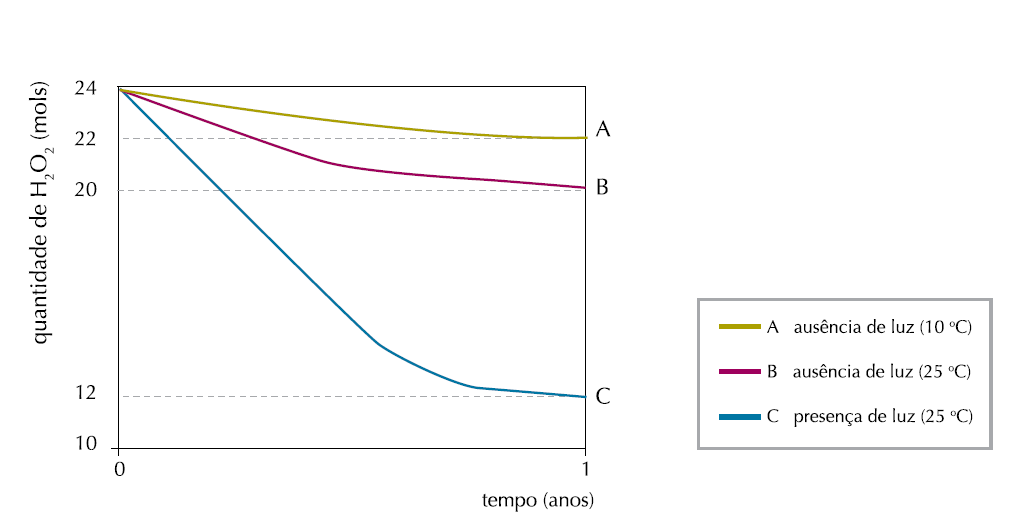
Em um experimento, foi monitorada a quantidade de peróxido de hidrogênio em três frascos idênticos – A, B e C – de 1 L de água oxigenada, mantidos em diferentes condições de luminosidade e temperatura.
Observe os resultados no gráfico:
Na condição em que ocorreu a menor taxa de decomposição do peróxido de hidrogênio, a velocidade média de formação de O2, em mol.ano-1, foi igual a:
- a) 1
- b) 2
- c) 6
- d) 12
C (PUC MG 2008) Na presença de ácido clorídrico, o magnésio reage para formar cloreto de magnésio e hidrogênio conforme a equação:
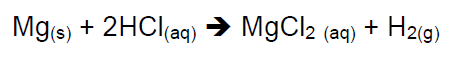 Utilizando a mesma quantidade de magnésio e numa mesma temperatura, considere os quatro experimentos a seguir.
Utilizando a mesma quantidade de magnésio e numa mesma temperatura, considere os quatro experimentos a seguir.
I. Fita de magnésio em presença de HCl 0,5 mol . L–1.
II. Magnésio em barra na presença de HCl 1,0 mol . L–1.
III. Pó de magnésio na presença de HCl 1,0 mol . L-1.
IV. Limalha de magnésio na presença de HCl 0,5 mol . L–1.
É CORRETO afirmar que a formação de H2 é mais rápida no experimento:
- a) I
- b) II
- c) III
- d) IV
C (PUC MG 2008) Considere o gráfico a seguir, referente aos diagramas energéticos de uma reação química com e sem catalisador.
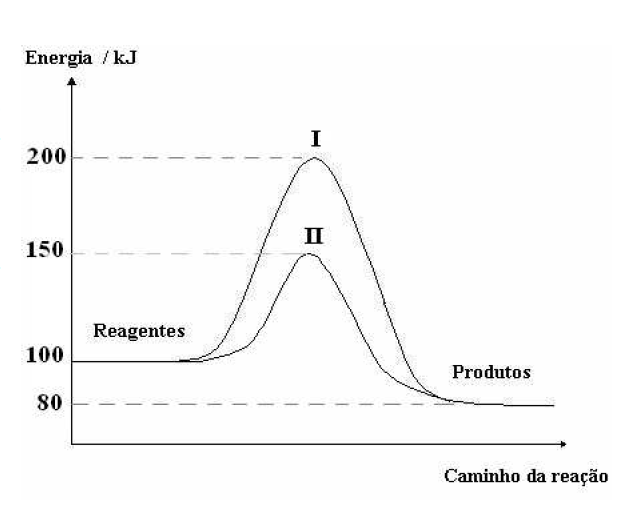
Assinale a afirmativa CORRETA.
- a) A reação é endotérmica.
- b) A energia de ativação em presença do catalisador é 150 kJ.
- c) A curva II representa o diagrama energético da reação catalisada.
- d) A reação acontece em duas etapas.
C (UFRGS 2008) A figura a seguir representa o esquema energético de uma reação genérica reversível, processo simples realizado em uma única etapa e que pode ocorrer sem catálise (linha cheia) ou com catálise (linha tracejada).
Sobre essa reação, são feitas as seguintes afirmações.
I – A reação direta é endotérmica.
II – A reação inversa é mais rápida na presença de catalisador.
III – O rendimento da reação direta é aumentado com o uso do catalisador.
Quais estão corretas?
- a) Apenas I.
- b) Apenas II.
- c) Apenas I e II.
- d) Apenas II e III.
- e) I, II e III.
EXERCÍCIOS EXTRAS
(CSA 2011 – BIB – U2b) Explique por que a elevação de temperatura altera a velocidade de uma reação química.
(CSA 2011 – BIB – U3b) Têm-se os dados abaixo, relativos à reação:
| velocidade
(mol/L.min) |
[A]
(mol/L) |
[B]
(mol/L) |
|
| 1ª experiência | 0,036 | 0,3 | 0,5 |
| 2ª experiência | 0,144 | 0,6 | 0,5 |
| 3ª experiência | 0,288 | 0,6 | 1,0 |
a) Escreva a lei de velocidade dessa reação.
b) Determine o valor da constante de velocidade desse processo.
E (CSA 2011 – BIB – U17) A combustão completa do pentano (C5H10) está ocorrendo com o oxigênio sendo consumido a uma razão de 2,4 mol/L.s. Nessa reação, a obtenção do gás carbônico deve ocorrer com velocidade de:
- a) 2,4 mol/L.s
- b) 0,3 mol/L.s
- c) 1,8 mol/L.s
- d) 12,0 mol/L.s
- e) 1,5 mol/L.s
A (CSA 2011 – BIB – U18) Com base no gráfico abaixo relativo a uma reação genérica com e sem catalisador:
Podemos afirmar que a energia de ativação e a variação de entalpia da reação inversa com catalisador (em kJ) são, respectivamente:
- a) 90 e 75
- b) 120 e 75
- c) 95 e -75
- d) 15 e -75
- e) 45 e -75
(CSA 2010 – BIB – U2) A reação:
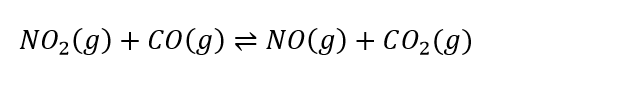 ocorre em duas etapas quando realizada a 100 °C:
ocorre em duas etapas quando realizada a 100 °C:
- a) Escreva a lei da velocidade para a reação global.
- b) Quando as concentrações do NO2 e do CO são 0,2 mol/L e 0,1 mol/L, respectivamente, essa reação ocorre com velocidade de 4,8 x 10-4 mol/L.min. Determine a constante de velocidade do processo.