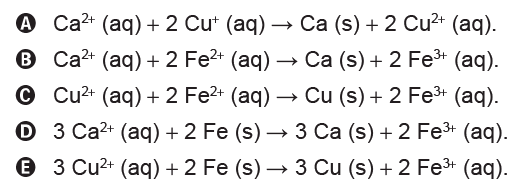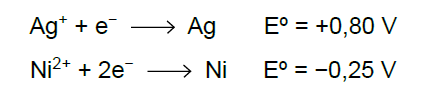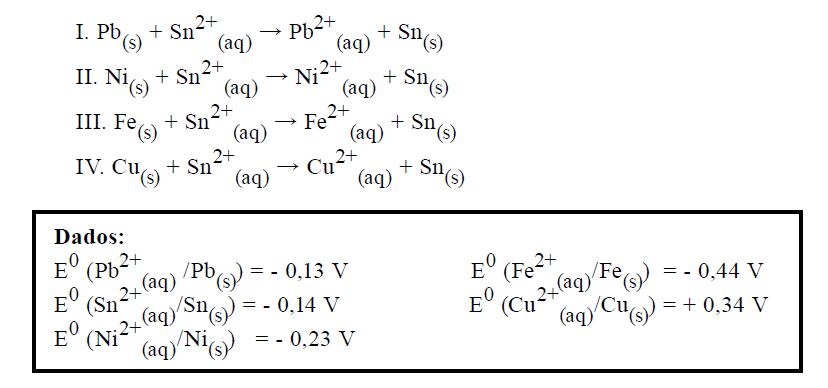QUÍMICA – LISTA DE EXERCÍCIOS SOBRE REAÇÕES ESPONTÂNEAS
NA ELETROQUÍMICA (PILHAS)
CAIU NO ENEM!
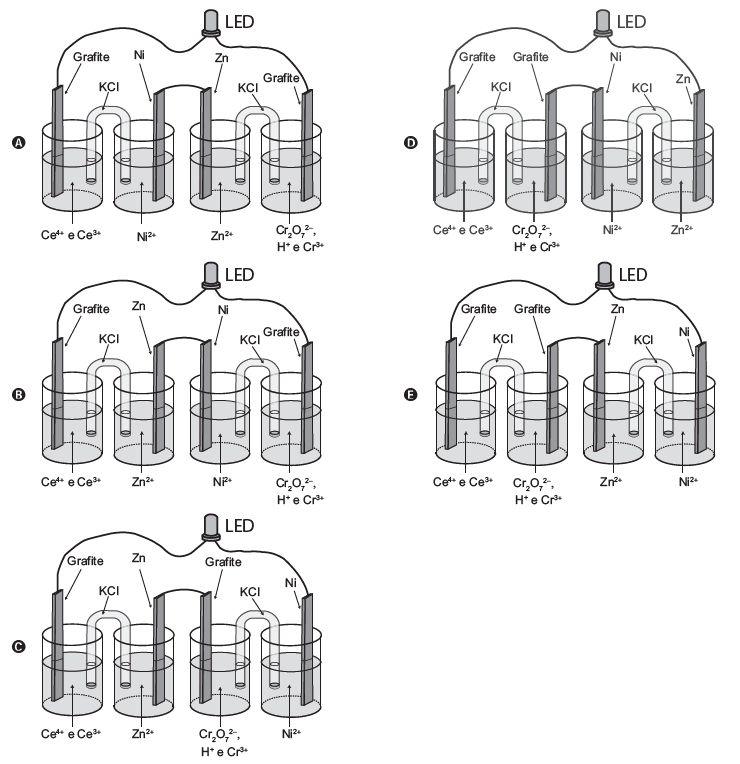
C (ENEM 2017) A invenção do LED azul, que permite a geração de outras cores para compor a luz branca, permitiu a construção de lâmpadas energeticamente mais eficientes e mais duráveis do que as incandescentes e fluorescentes. Em um experimento de laboratório, pretende-se associar duas pilhas em série para acender um LED azul que requer 3,6 volts para o seu funcionamento. Considere as semirreações de redução e seus respectivos potenciais mostrados no quadro.
Qual associação em série de pilhas fornece diferença de potencial, nas condições-padrão, suficiente para acender o LED azul?
B (ENEM 2016) Em sistemas bioeletroquímicos, os potenciais padrão (E°’) apresentam valores característicos. Para as biocélulas de acetato, considere as seguintes semirreações de redução e seus respectivos potenciais:
Nessas condições, qual é o número mínimo de biocélulas de acetato, ligadas em série, necessárias para se obter uma diferença de potencial de 4,4 V?
- a) 3
- b) 4
- c) 6
- d) 9
- e) 15
A (ENEM 2015) A calda bordalesa é uma alternativa empregada no combate a doenças que afetam folhas de plantas. Sua produção consiste na mistura de uma solução aquosa de sulfato de cobre(II), CuSO4, com óxido de cálcio, CaO, e sua aplicação só deve ser realizada se estiver levemente básica. A avaliação rudimentar da basicidade dessa solução é realizada pela adição de três gotas sobre uma faca de ferro limpa. Após três minutos, caso surja uma mancha avermelhada no local da aplicação, afirma-se que a calda bordalesa ainda não está com a basicidade necessária. O quadro apresenta os valores de potenciais padrão de redução (Eo) para algumas semirreações de redução.
A equação química que representa a reação de formação da mancha avermelhada é:
D (ENEM 2014) A revelação das chapas de raios X gera uma solução que contém íons prata na forma de Ag(S2O3)2-3 . Para evitar a descarga desse metal no ambiente, a recuperação de prata metálica pode ser feita tratando eletroquimicamente essa solução com uma espécie adequada. O quadro apresenta semirreações de redução de alguns íons metálicos.
Das espécies apresentadas, a adequada para essa recuperação é
- a) Cu (s).
- b) Pt (s).
- c) Al3+(aq).
- d) Sn (s).
- e) Zn2+(aq)
E (ENEM 2013) O Instituto Luiz Coimbra (UFRJ) lançou o primeiro ônibus urbano movido a hidrogênio do Hemisfério Sul, com tecnologia inteiramente nacional. Sua tração provém de três fontes de energia, sendo uma delas a pilha de combustível, na qual o hidrogênio, gerado por um processo eletroquímico, reage com o oxigênio do ar, formando água.
FRAGA, I. Disponível em: http://cienciahoje.uol.com.br. Acesso em: 20 jul. 2010 (adaptado).
A transformação de energia que ocorre na pilha de combustível responsável pelo movimento do ônibus decorre da energia cinética oriunda do(a)
- a) calor absorvido na produção de água.
- b) expansão gasosa causada pela produção de água.
- c) calor liberado pela reação entre o hidrogênio e o oxigênio.
- d) contração gasosa causada pela reação entre o hidrogênio e o oxigênio.
- e) eletricidade gerada pela reação de oxirredução do hidrogênio com o oxigênio.
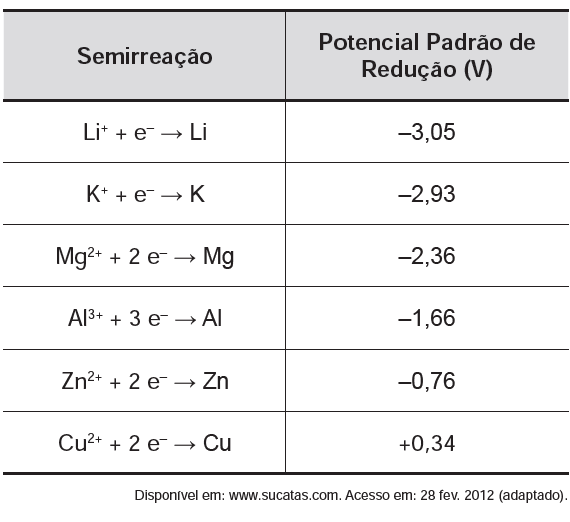
E (ENEM 2012) O boato de que os lacres das latas de alumínio teriam um alto valor comercial levou muitas pessoas a juntarem esse material na expectativa de ganhar dinheiro com sua venda. As empresas fabricantes de alumínio esclarecem que isso não passa de uma “lenda urbana”, pois ao retirar o anel da lata, dificulta-se a reciclagem do alumínio. Como a liga do qual é feito o anel contém alto teor de magnésio, se ele não estiver junto com a lata, fica mais fácil ocorrer a oxidação do alumínio no forno. A tabela apresenta as semirreações e os valores de potencial padrão de redução de alguns metais:
Com base no texto e na tabela, que metais poderiam entrar na composição do anel das latas com a mesma função do magnésio, ou seja, proteger o alumínio da oxidação nos fornos e não deixar diminuir o rendimento da sua reciclagem?
- a) Somente o lítio, pois ele possui o menor potencial de redução.
- b) Somente o cobre, pois ele possui o maior potencial de redução.
- c) Somente o potássio, pois ele possui potencial de redução mais próximo do magnésio.
- d) Somente o cobre e o zinco, pois eles sofrem oxidação mais facilmente que o alumínio.
- e) Somente o lítio e o potássio, pois seus potenciais de redução são menores do que o do alumínio.
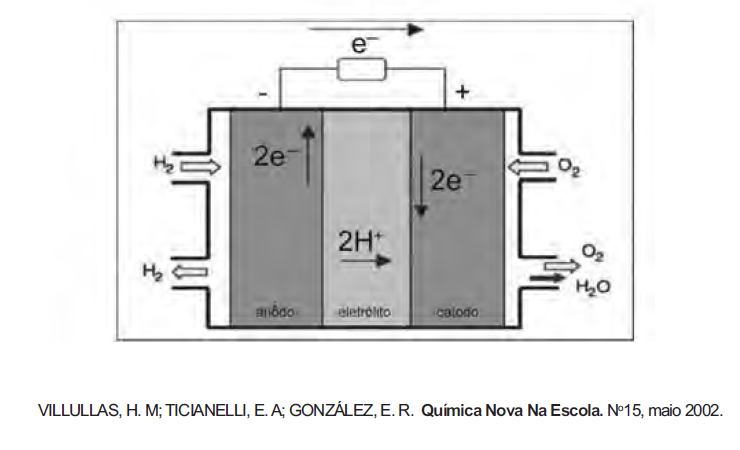
A (ENEM 2010) O crescimento da produção de energia elétrica ao longo do tempo tem influenciado decisivamente o progresso da humanidade, mas também tem criado uma séria preocupação: o prejuízo ao meio ambiente. Nos próximos anos, uma nova tecnologia de geração de energia elétrica deverá ganhar espaço: as células a combustível hidrogênio/oxigênio.
Com base no texto e na figura, a produção de energia elétrica por meio da célula a combustível hidrogênio/oxigênio diferencia-se dos processos convencionais porque
- a) transforma energia química em energia elétrica, sem causar danos ao meio ambiente, porque o principal subproduto formado é a água.
- b) converte a energia química contida nas moléculas dos componentes em energia térmica, sem que ocorra a produção de gases poluentes nocivos ao meio ambiente.
- c) transforma energia química em energia elétrica, porém emite gases poluentes da mesma forma que a produção de energia a partir dos combustíveis fósseis.
- d) converte energia elétrica proveniente dos combustíveis fósseis em energia química, retendo os gases poluentes produzidos no processo sem alterar a qualidade do meio ambiente.
- e) converte a energia potencial acumulada nas moléculas de água contidas no sistema em energia química, sem que ocorra a produção de gases poluentes nocivos ao meio ambiente.
CAIU NO VESTIBULAR!
2019
C (FCMSCSP 2019) A tabela indica a tensão elétrica mínima para colocar em funcionamento cinco diferentes equipamentos.
Uma bateria foi montada com quatro pilhas em série. Cada uma dessas pilhas consiste em um dispositivo com eletrodos de níquel e de prata em um meio eletrólito adequado. Os potenciais-padrão desses eletrodos estão indicados nas equações:
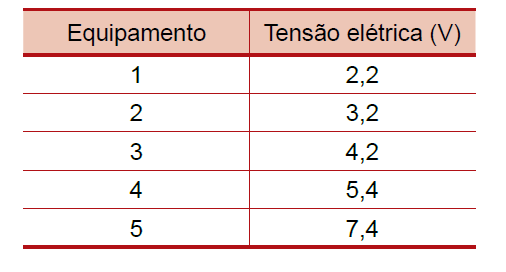
Desprezando a resistência interna das pilhas, o equipamento que funciona com a tensão elétrica mínima igual àquela gerada pela bateria é o de número
- a) 2.
- b) 4.
- c) 3.
- d) 1.
- e) 5.
2018
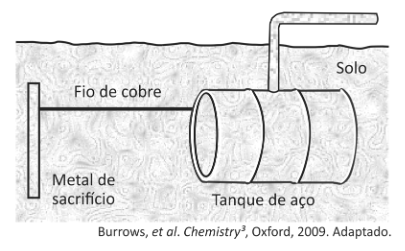
A (FUVEST 2018) Um método largamente aplicado para evitar a corrosão em estruturas de aço enterradas no solo, como tanques e dutos, é a proteção catódica com um metal de sacrifício. Esse método consiste em conectar a estrutura a ser protegida, por meio de um fio condutor, a uma barra de um metal diferente e mais facilmente oxidável, que, com o passar do tempo, vai sendo corroído até que seja necessária sua substituição.
Um experimento para identificar quais metais podem ser utilizados como metal de sacrifício consiste na adição de um pedaço de metal a diferentes soluções contendo sais de outros metais, conforme ilustrado, e cujos resultados são mostrados na tabela. O símbolo ( + ) indica que foi observada uma reação química e o ( – ) indica que não se observou qualquer reação química.
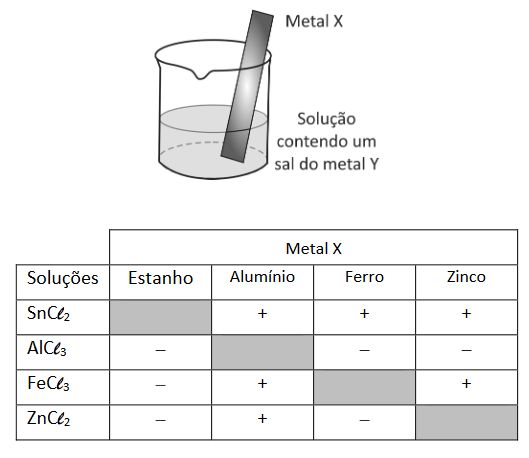 Da análise desses resultados, conclui se que pode(m) ser utilizado(s) como metal(is) de sacrifício para tanques de aço:
Da análise desses resultados, conclui se que pode(m) ser utilizado(s) como metal(is) de sacrifício para tanques de aço:
- a) Al e Zn
- b) somente Zn
- c) Al e Sn
- d) somente Al.
- e) Sn e Zn
D (UFPR 2018) Na mitocôndria, ocorre o processo final das vias de degradação oxidativa, chamado de cadeia de transporte de elétrons. Nesse processo, os elétrons provindos do NADH e FADH2 são transportados por complexos proteicos dispostos espacial e energeticamente, de modo que formem um gradiente de energia livre, em que o fluxo de elétrons vai do componente de maior energia livre para o de menor. O receptor final dos elétrons é a molécula de oxigênio, que é convertida em água. O potencial redox está relacionado com a energia livre através da relação ΔG = nF(-ΔE), em que ΔG é a variação de energia livre, ΔE é a variação de potencial, n é número de elétrons e F é a constante de Faraday. Na tabela abaixo, são fornecidos alguns componentes presentes na cadeia de transporte de elétrons e os respectivos valores de potencial de redução.
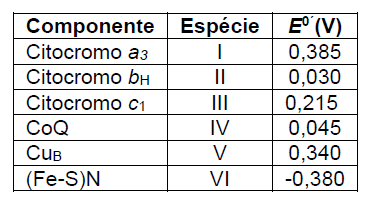 Respeitando o gradiente de energia livre, o fluxo de elétrons deve percorrer a sequência mostrada em:
Respeitando o gradiente de energia livre, o fluxo de elétrons deve percorrer a sequência mostrada em:
- a) I→II→IV→III→V→VI.
- b) II→III→IV→VI→V→I.
- c) I→IV→VI→III→V→II.
- d) VI→II→IV→III→V→I.
- e) VI→I→V→II→IV→III.
C (FGV SP 2018) Uma bateria de recarga ultrarrápida foi desenvolvida por pesquisadores da Universidade Stanford. Ela emprega eletrodos de alumínio e de grafite; e, como eletrólito, um sal
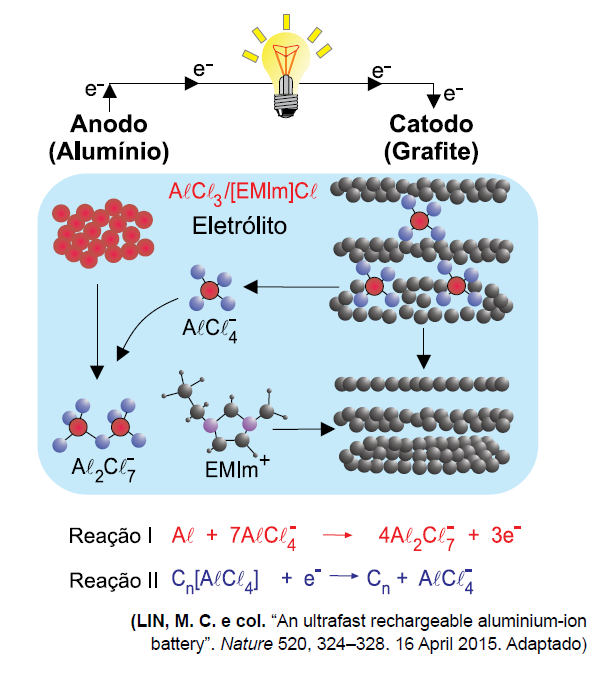
orgânico que é líquido na temperatura ambiente, cloreto de 1-etil-3-metilimidazolio, representado pela fórmula [EMIm]Cl. Durante as reações, o alumínio metálico forma espécies complexas com o ânion cloreto, AlCl4– e Al2Cl7–. Nos demais aspectos, a operação da bateria segue o comportamento usual de uma pilha.
Um esquema de sua operação é representado na figura.
Quando esta bateria está operando no sentido de fornecer corrente elétrica, o eletrodo de grafite é o polo _______________________. A reação I é a reação de , e, na reação global, o total de elétrons envolvidos para cada mol de alumínio metálico que participa do processo é _____________________.
As lacunas são preenchidas, correta e respectivamente, por:
- a) negativo … oxidação … três
- b) negativo … oxidação … quatro
- c) positivo … oxidação … três
- d) positivo … redução … três
- e) positivo … redução … quatro
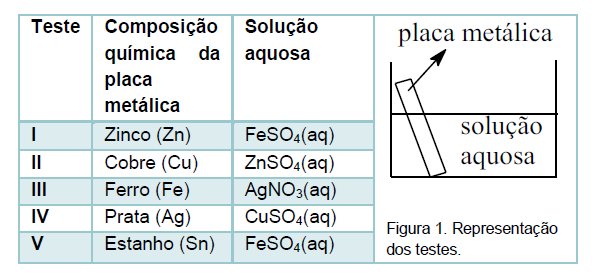
A (UPF 2018) Foram realizados testes mergulhando diferentes placas metálicas dentro de determinadas soluções aquosas (Figura 1), segundo os dados indicados no quadro a seguir.
Considerando os dados a seguir referentes ao potencial padrão de redução (Eored) em volts, a 25 °C, marque a opção que indica corretamente quais os testes nos quais ocorrerá reação
espontânea.
- a) I e III, apenas.
- b) II e IV, apenas.
- c) I e V, apenas.
- d) I, II, III e V, apenas.
- e) III e V, apenas.
2017
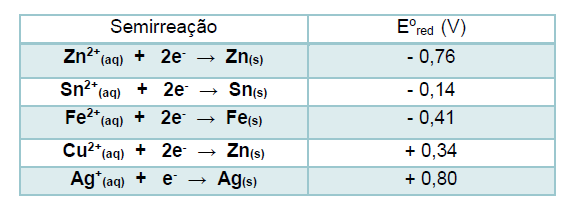
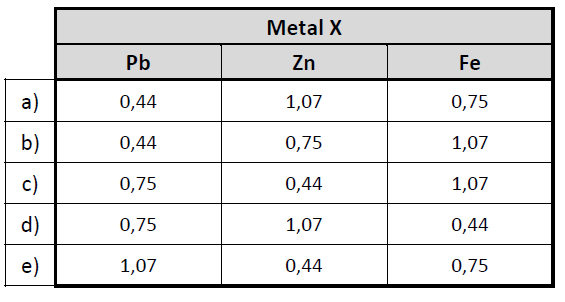
A (FUVEST 2017) Um estudante realizou um experimento para avaliar a reatividade dos metais Pb, Zn e Fe. Para isso, mergulhou, em separado, uma pequena placa de cada um desses metais em cada uma das soluções aquosas dos nitratos de chumbo, de zinco e de ferro. Com suas observações, elaborou a seguinte tabela, em que (sim) significa formação de sólido sobre a placa e (não) significa nenhuma evidência dessa formação:
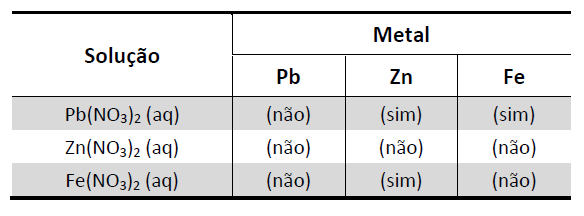 A seguir, montou três diferentes pilhas galvânicas, conforme esquematizado.
A seguir, montou três diferentes pilhas galvânicas, conforme esquematizado.
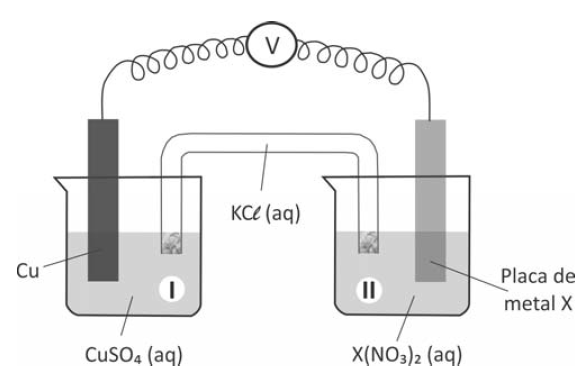 Nessas três montagens, o conteúdo do béquer I era uma solução aquosa de CuSO4 de mesma concentração, e essa solução era renovada na construção de cada pilha. O eletrodo onde ocorria a redução (ganho de elétrons) era o formado pela placa de cobre mergulhada em CuSO4 (aq).
Nessas três montagens, o conteúdo do béquer I era uma solução aquosa de CuSO4 de mesma concentração, e essa solução era renovada na construção de cada pilha. O eletrodo onde ocorria a redução (ganho de elétrons) era o formado pela placa de cobre mergulhada em CuSO4 (aq).
Em cada uma das três pilhas, o estudante utilizou, no béquer II, uma placa de um dos metais X (Pb, Zn ou Fe), mergulhada na solução aquosa de seu respectivo nitrato.
O estudante mediu a força eletromotriz das pilhas, obtendo os valores: 0,44 V; 0,75 V e 1,07 V.
A atribuição correta desses valores de força eletromotriz a cada uma das pilhas, de acordo com a reatividade dos metais testados, deve ser
- a) I, II e IV, apenas.
- b) II e III, apenas.
- c) I, II e III, apenas.
- d) I e II, apenas.
- e) I e IV, apenas.
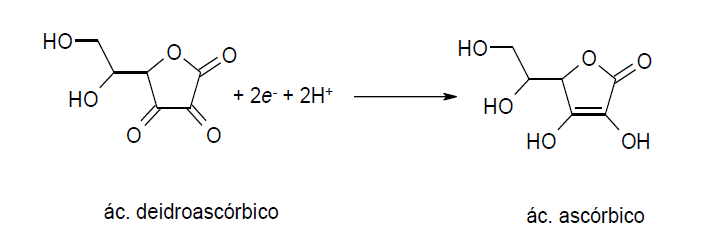
B (UFPR 2017) O ácido ascórbico é uma das formas da vitamina C que apresenta propriedade antioxidante. Na indústria de alimentos, ele é largamente utilizado como aditivo para prevenir a oxidação. Uma maneira de analisar a quantidade de ácido ascórbico em bebidas é através de uma reação de oxirredução utilizando iodo. Com base nisso, foi montada uma pilha, conforme ilustração ao lado, contendo eletrodos inertes de platina ligados a um voltímetro. Foram mantidas condições padrão (298 K, 1 atm e 1 mol L-1) para o experimento, e no instante em que se fechou o circuito, conectando-se os fios ao voltímetro, o valor de potencial medido foi de 0,48 V.
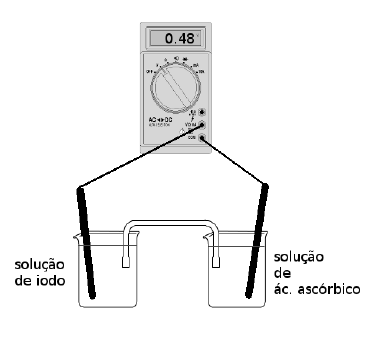
Sabendo que o potencial padrão de redução de iodo a iodeto é de E0 = 0,54 V, o potencial padrão da reação abaixo é:
- a) 0,03 V.
- b) 0,06 V.
- c) 0,24 V.
- d) 0,48 V.
- e) 1,02 V.
D (UPF 2017) A figura abaixo apresenta a representação de uma célula eletroquímica (pilha) e potenciais de redução das semirreações.
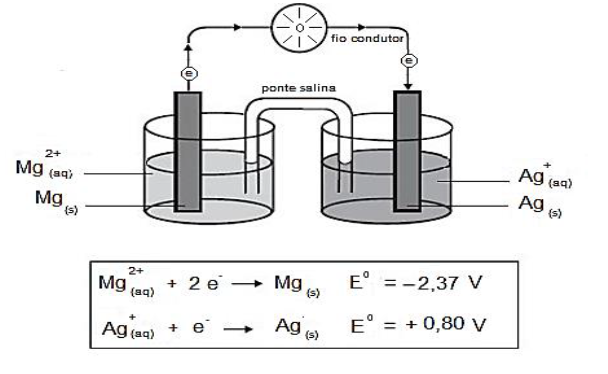 Considerando-se a informação dada, analise as seguintes afirmações:
Considerando-se a informação dada, analise as seguintes afirmações:
I. O eletrodo de prata é o polo positivo, no qual ocorre a redução.
II. O magnésio é o agente oxidante da pilha.
III. A diferença de potencial (ddp) da pilha representada na figura é de +3,17 V.
IV. O sentido do fluxo dos elétrons se dá do catodo para o ânodo.
É incorreto apenas o que se afirma em:
- a) I e II.
- b) I e III.
- c) II e III.
- d) II e IV.
- e) III e IV.
2016
A (UFRGS 2016) O quadro abaixo relaciona algumas semirreações e seus respectivos potenciais padrão de redução, em solução aquosa.
A partir desses dados, é correto afirmar que
- a) uma solução aquosa de hipoclorito poderá oxidar os íons Mn2+.
- b) uma solução aquosa de H2O2 é um forte agente redutor.
- c) o ozônio tem uma forte tendência a ceder elétrons em solução aquosa.
- d) a adição de H2O2 a uma solução aquosa, contendo oxigênio dissolvido, promove a formação de ozônio gasoso.
- e) o permanganato, entre as substâncias relacionadas no quadro, é o mais poderoso agente oxidante.
2008
A (PUC MG 2008) Um aluno deseja preparar uma solução aquosa de nitrato de chumbo 1mol × L-1 , a 25ºC. Para preparar a mistura, ele tem à disposição um bastão de cobre, um bastão de zinco, um bastão de ferro, um bastão de níquel e um bastão de prata. Considere abaixo os potenciais normais de redução:
E° (Pb 2+/Pb) = -0,13 V
E° (Cu 2+/Cu) = +0,34 V
E° (Ni 2+/Ni) = -0,25 V
E° (Fe 2+/Fe) = -0,44 V
E° (Zn 2+/Zn) = -0,76 V
Eo (Ag+/Ag) = + 0,80 V
Assinale os bastões misturadores que poderão ser usados sem contaminar a solução.
- a) cobre e prata.
- b) ferro e zinco.
- c) níquel e zinco.
- d) níquel e ferro.