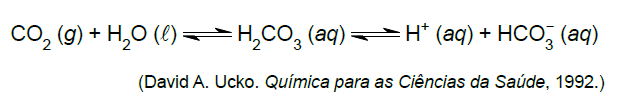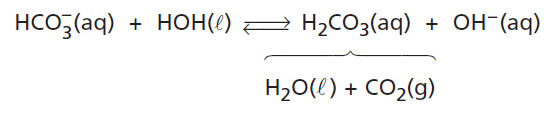CAIU NO ENEM!
CAIU NO VESTIBULAR!
2018
(pH) B (UERJ SIMULADO 2018) O cianeto de hidrogênio (HCN) é um gás extremamente tóxico, que sofre ionização ao ser dissolvido em água, conforme a reação abaixo.
HCN (aq) ⇄ H+ (aq) + CN– (aq)
Em um experimento, preparou-se uma solução aquosa de HCN na concentração de 0,1 mol.L‑1 e grau de ionização igual a 0,5%. A concentração de íons cianeto nessa solução, em mol.L‑1, é igual a:
- a) 2,5 x 10-4
- b) 5,0 x 10-4
- c) 2,5 x 10-2
- d) 5,0 x 10-2
(HIDRÓLISE SALINA) A (UNESP 2018) Para sua apresentação em um “show de química”, um grupo de estudantes confeccionou um recipiente com três compartimentos, 1, 2 e 3, dispostos de modo a lembrar o formato da bandeira brasileira. A esses compartimentos, adicionaram três soluções aquosas diferentes, todas incolores e de concentração igual a 0,1 mol/L, uma em cada compartimento. O recipiente foi mantido em posição horizontal.
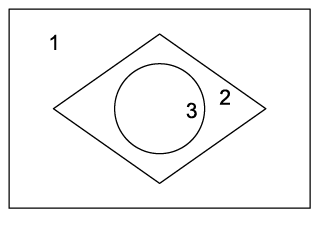 Em seguida, acrescentaram em cada compartimento o indicador azul de bromotimol, que apresenta cor azul em pH > 7,6 e amarela em pH < 6,0. Como resultado, o recipiente apresentou as cores da bandeira nacional, conforme mostra a figura.
Em seguida, acrescentaram em cada compartimento o indicador azul de bromotimol, que apresenta cor azul em pH > 7,6 e amarela em pH < 6,0. Como resultado, o recipiente apresentou as cores da bandeira nacional, conforme mostra a figura.
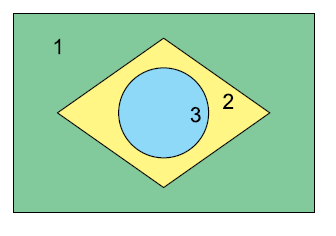 As soluções aquosas colocadas inicialmente pelos estudantes nos compartimentos 1, 2 e 3 podem ter sido, respectivamente,
As soluções aquosas colocadas inicialmente pelos estudantes nos compartimentos 1, 2 e 3 podem ter sido, respectivamente,
- a) cloreto de sódio, ácido clorídrico e hidróxido de sódio.
- b) cloreto de sódio, carbonato de sódio e ácido clorídrico.
- c) hidróxido de sódio, ácido clorídrico e cloreto de sódio.
- d) hidróxido de sódio, carbonato de sódio e ácido clorídrico.
- e) carbonato de sódio, hidróxido de sódio e ácido clorídrico.
C (UNESP 2018) Sob temperatura constante, acrescentou-se cloreto de sódio em água até sobrar sal sem se dissolver, como corpo de fundo. Estabeleceu-se assim o seguinte equilíbrio:
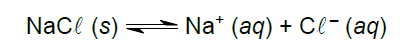 Mantendo a temperatura constante, foi acrescentada mais uma porção de NaCl(s). Com isso, observa-se que a condutibilidade elétrica da solução sobrenadante _____________, a quantidade de corpo de fundo _____________ e a concentração de íons em solução __________________. As lacunas do texto devem ser preenchidas, respectivamente, por:
Mantendo a temperatura constante, foi acrescentada mais uma porção de NaCl(s). Com isso, observa-se que a condutibilidade elétrica da solução sobrenadante _____________, a quantidade de corpo de fundo _____________ e a concentração de íons em solução __________________. As lacunas do texto devem ser preenchidas, respectivamente, por:
- a) não se altera – aumenta – aumenta
- b) não se altera – não se altera – não se altera
- c) não se altera – aumenta – não se altera
- d) aumenta – diminui – aumenta
- e) diminui – aumenta – aumenta
C (FCMSCSP 2018) Para o corpo humano funcionar adequadamente, o pH de seus fluidos deve ser mantido dentro de certos limites. Por exemplo, o pH do sangue deve ficar entre 7,35 e 7,45. O principal tampão do plasma sanguíneo é representado pelo seguinte equilíbrio químico:
Em quadros clínicos de acidose metabólica, que podem ocorrer em casos graves de doença renal, o pH do sangue fica ____________ . O uso intravenoso de solução injetável de bicarbonato de sódio no tratamento de casos graves de doença renal _____________ a concentração de íons H+ no
plasma sanguíneo. Assinale a alternativa que preenche, correta e respectivamente, as lacunas do texto.
- a) acima de 7,45 ─ diminui
- b) acima de 7,45 ─ aumenta
- c) abaixo de 7,35 ─ diminui
- d) abaixo de 7,35 ─ aumenta
- e) entre 7,35 e 7,45 ─ aumenta
C (FMABC 2018) Considere os seguintes equilíbrios existentes numa solução de comprimido antiácido efervescente.
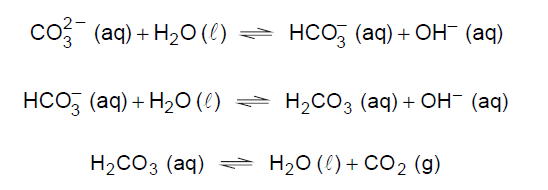 Essa solução, ao entrar em contato com o suco gástrico estomacal, provocará
Essa solução, ao entrar em contato com o suco gástrico estomacal, provocará
- a) aumento da produção do CO2 (g) sem alteração do pH estomacal.
- b) aumento do pH estomacal e diminuição da produção de CO2 (g).
- c) aumento do pH estomacal e aumento da produção de CO2 (g).
- d) diminuição do pH estomacal e diminuição da produção de CO2 (g).
- e) diminuição do pH estomacal e aumento da produção de CO2 (g).
(pH) E (FGV SP 2018) Os resultados das análises de pH a 20 °C de amostras de duas marcas brasileiras distintas de água mineral são indicados no quadro.
 Considere também que essas duas amostras podem estar gaseificadas com CO2, cujo equilíbrio químico em meio aquoso é representado na equação
Considere também que essas duas amostras podem estar gaseificadas com CO2, cujo equilíbrio químico em meio aquoso é representado na equação
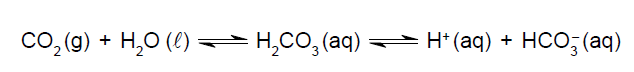 É correto afirmar que a 20 °C a água mineral
É correto afirmar que a 20 °C a água mineral
- a) X é ácida e gaseificada, e sua concentração de íons H+ é 1 x 10–10 mol/L.
- b) X é básica e gaseificada, e sua concentração de íons OH– é 1 x 10–10 mol/L.
- c) Y é básica e gaseificada, e sua concentração de íons OH– é 1 x 10–4 mol/L.
- d) Y é ácida e gaseificada, e sua concentração de íons H+ é 1 x 10–10 mol/L.
- e) Y é ácida e gaseificada, e sua concentração de íons H+ é 1 x 10–4 mol/L.
2017
(HIDRÓLISE SALINA) C (MACKENZIE 2017) Um aluno preparou três soluções aquosas, a 25 ºC, de acordo com a figura abaixo.
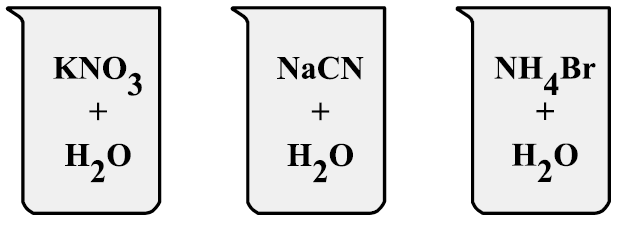 Conhecedor dos conceitos de hidrólise salina, o aluno fez as seguintes afirmações:
Conhecedor dos conceitos de hidrólise salina, o aluno fez as seguintes afirmações:
- a solução de nitrato de potássio apresenta caráter neutro.
- o cianeto de sódio sofre ionização em água, produzindo uma solução básica.
- ao verificar o pH da solução de brometo de amônio, a 25 ºC, conclui-se que Kb > Ka.
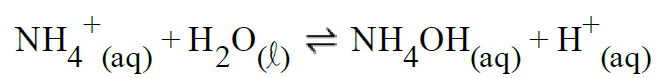 representa a hidrólise do cátion amônio.
representa a hidrólise do cátion amônio.
Estão corretas somente as afirmações
- a) I e II.
- b) I, II e III.
- c) I e IV.
- d) II e III.
- e) I, II e IV.
(EFEITO DO ÍON COMUM) C (PUC SP 2017) Uma das reações utilizadas para a demonstração de deslocamento de equilíbrio, devido à mudança de cor, é a representada pela equação a seguir:
2 CrO42- (aq) + 2 H+ (aq) ⇄ Cr2O72- (aq) + H2O (l)
sendo que, o cromato (CrO42-) possui cor amarela e o dicromato (Cr2O72-) possui cor alaranjada.
Sobre esse equilíbrio foram feitas as seguintes afirmações:
- A adição de HCl provoca o deslocamento do equilíbrio para a direita.
- A adição de NaOH resulta na cor alaranjada da solução.
- A adição de HCl provoca o efeito do íon comum.
- A adição de dicromato de potássio não desloca o equilíbrio.
As afirmações corretas são:
- a) I e II.
- b) II e IV.
- c) I e III.
- d) III e IV.
2016
(PRODUTO DE SOLUBILIDADE) C (UFRGS 2016) O equilíbrio de solubilidade do cloreto de prata é expresso pela reação
![]() cuja constante de equilíbrio tem o valor 1,7 x 10 –10. Sobre esse equilíbrio, é correto afirmar que
cuja constante de equilíbrio tem o valor 1,7 x 10 –10. Sobre esse equilíbrio, é correto afirmar que
- a) uma solução em que [Ag+] = [Cl –] = 1,0 x 10–5 mol L–1 será uma solução supersaturada.
- b) a adição de cloreto de prata sólido a uma solução saturada de AgCl irá aumentar a concentração de cátions prata.
- c) a adição de cloreto de sódio a uma solução saturada de AgCl irá diminuir a concentração de cátions prata.
- d) a adição de nitrato de prata a uma solução supersaturada de AgCl irá diminuir a quantidade de AgCl precipitado.
- e) a mistura de um dado volume de uma solução em que [Ag+] = 1,0 x10–6 mol L–1, com um volume igual de uma solução em que [Cl –] =1,0 x10–6 mol L–1, irá produzir precipitação de AgCl.
2009
(PRODUTO DE SOLUBILIDADE) (UNESP 2009) Os cálculos renais são usualmente constituídos por oxalatos minerais. A precipitação deste sal no organismo ocorre sempre que a concentração do íon oxalato aumenta muito no plasma sanguíneo. Uma amostra de plasma sanguíneo contém, entre outros solutos, as seguintes concentrações de cátions solúveis: [Mg+2] = 8,6 x 10–4 mol⋅L–1 e [Ca+2] = 2,5 x 10–3 mol⋅L–1. Determine a ordem em que cada íon precipita com a adição de oxalato de sódio sólido. Calcule a concentração molar de C2O42– quando a precipitação de cada um deles começar. Considere que não haja variação de volume com a adição de oxalato de sódio sólido.
Dados: KPS (MgC2O4) = 8,6 x 10–5 (a 25 ºC).
KPS (CaC2O4) = 2,6 x 10–9 (a 25 ºC).
RESPOSTA: O CaC2O4 será o primeiro a precipitar, quando a concentração de íons C2O42– atingir o valor de 1,04 x 10-6 mol/L. Continuando com a adição do oxalato de sódio, o MgC2O4 irá se precipitar quando a concentração dos íons C2O42– atingir o valor de 1,0 x 10-1 mol/L.
2008
(pH) (UNESP 2008) Em um laboratório, há um frasco no qual são despejados os resíduos para que sejam tratados antes do descarte. Inicialmente vazio e limpo, nesse frasco foram despejados 90 mL de uma solução aquosa de uma base forte, com pH = 9, e 10 mL de uma solução aquosa de ácido forte, pH = 3. Calcule o pH da solução resultante no frasco de resíduos.
RESPOSTA: pH = 4.
2007
(PRODUTO DE SOLUBILIDADE) (UNESP 2007) O iodeto de potássio pode ser utilizado para separar íons prata de uma solução aquosa, pois o iodeto de prata formado é muito pouco solúvel. Este sal pode ser utilizado para bombardear nuvens em épocas de seca e, assim, induzir chuvas. Suponha que o responsável por um laboratório receba uma encomenda de iodeto de prata e utilize soluções concentradas de nitrato de prata e de iodeto de potássio, a 25 ºC, como reagentes para preparar o produto. Após o surgimento do precipitado de interesse, qual deve ser a concentração de íons prata na solução resultante? Considere Ks do AgI = 8,1 × 10–17.
RESPOSTA: [Ag+] = 9 x 10-9 mol/L.
(PRODUTO DE SOLUBILIDADE) (UNESP 2007) O sal sulfato de cobre é muito utilizado na agricultura. Por ser bastante solúvel, a água da chuva pode transportá-lo com facilidade até os rios próximos à atividade agrícola ou ao lençol freático. Uma forma de monitorar a concentração de íons Cu2+ de uma amostra de água para fins de consumo humano consiste em produzir um precipitado que pode ser separado por filtração. Considerando que o valor de Ks para o CuS é igual a 9,0 × 10–36, determine a máxima concentração de íons Cu2+ em uma amostra de água tratada com ácido sulfídrico (H2S).
RESPOSTA: [Cu2+] = [S2-] = 3 X 10-18 mol/L.
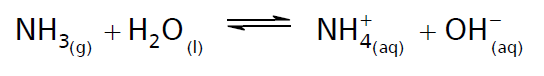
(HIDRÓLISE SALINA) (MAUÁ 2007) Soluções aquosas de hidróxido de amônio (NH4OH) podem ser adequadamente representadas pelo equilíbrio
- a) A solução representada pelo equilíbrio possui caráter ácido, básico ou neutro?
- b) Explique por que uma solução de NH4OH(aq) deve ser conservada em frasco fechado.
2006
(HIDRÓLISE SALINA) (UNESP 2006) A análise ácido-base de uma solução de concentração desconhecida é geralmente feita por titulação, procedimento no qual um volume medido do ácido é adicionado a um frasco, e um titulante, uma solução conhecida de base, é adicionado até que o ponto de equivalência seja atingido.
- a) Qual o valor de pH no ponto de equivalência em uma titulação de uma solução aquosa de HCl 0,10 M com uma solução aquosa de NaOH 0,10 M? Justifique.
- b) Dos indicadores a seguir, qual seria o mais apropriado para realizarmos a titulação de HCl com NaOH? Justifique.
 RESPOSTA: a) No ponto de equivalência o pH é 7,0, pois tanto o ácido quanto a base são fortes e não ocorre hidrólise salina; b) O indicador mais apropriado é a fenolftaleína, pois a faixa de viragem é a mais próxima do pH do ponto de equivalência.
RESPOSTA: a) No ponto de equivalência o pH é 7,0, pois tanto o ácido quanto a base são fortes e não ocorre hidrólise salina; b) O indicador mais apropriado é a fenolftaleína, pois a faixa de viragem é a mais próxima do pH do ponto de equivalência.
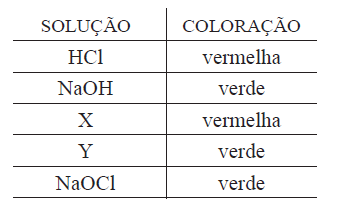
(HIDRÓLISE SALINA) (UNIFESP 2006) Extratos de muitas plantas são indicadores naturais ácido-base, isto é, apresentam colorações diferentes de acordo com o meio em que se encontram. Utilizando-se o extrato de repolho roxo como indicador, foram testadas soluções aquosas de HCl, NaOH, NaOCl, NaHCO3 e NH4Cl, de mesma concentração. Os resultados são apresentados na tabela
- a) Identifique as soluções X e Y. Justifique.
- b) Calcule, a 25ºC, o pH da solução de NaOCl 0,04 mol/L. Considere que, a 25ºC, a constante de hidrólise do íon ClO– é 2,5 x 10–7.
RESPOSTA: a) O extrato de repolho roxo, utilizado como indicador ácido-base, apresenta coloração verde quando o meio é básico.
A solução X é a de NH4Cl, pois a solução resultante é ácida (sal de ácido forte e base fraca).
![]() E a solução Y é a de NaHCO3, pois a solução resultante é básica (sal de ácido fraco e base forte).
E a solução Y é a de NaHCO3, pois a solução resultante é básica (sal de ácido fraco e base forte).
2005
(pH/DESLOCAMENTO DE EQUILÍBRIO) (UFSCAR) A acidose metabólica é causada pela liberação excessiva, na corrente sanguínea, de ácido láctico e de outras substâncias ácidas resultantes do metabolismo. Considere a equação envolvida no equilíbrio ácido-base do sangue e responda.
- a) Explique de que forma o aumento da taxa de respiração, quando se praticam exercícios físicos, contribui para a redução da acidez metabólica.
- b) O uso de diuréticos em excesso pode elevar o pH do sangue, causando uma alcalose metabólica. Explique de que forma um diurético perturba o equilíbrio ácido-base do sangue.
RESPOSTA: a) O aumento da respiração diminui a quantidade de CO2 do sangue, deslocando o equilíbrio no sentido dos reagentes. A diminuição da quantidade de H+ reduz a acidez metabólica; b) O diurético atua na retirada de água do organismo, deslocando o referido equilíbrio no sentido dos reagentes. A maior consumo na quantidade de íons H+ aumenta o pH do sangue.
2004
(pH) (UNESP 2004) O esmalte dos dentes é constituído por um material pouco solúvel em água. Seu principal componente é a hidroxiapatita [Ca5(PO4)3OH] e o controle do pH da saliva – normalmente muito próximo de 7 – é importante para evitar o desgaste desse esmalte, conforme o equilíbrio apresentado a seguir.
- a) Sabendo que, cerca de dez minutos após a ingestão de um refrigerante com açúcar, o pH da saliva pode alcançar, aproximadamente, o valor 5, e que pH = – log[H+], calcule quantas vezes a concentração de H+ na saliva nesta situação é maior do que o normal. Apresente seus cálculos.
- b) Explique, considerando o equilíbrio apresentado e o Princípio de Le Chatelier, o efeito da diminuição do pH sobre o esmalte dos dentes.
RESPOSTA: a) 100; b) A redução do pH desloca o equilíbrio no sentido dos produtos, pois aumento a concentração de íons H+. Esse deslocamento reduz a quantidade de hidroxiapatita, desgastando o esmalte dos dentes e, consequentemente aumentando a incidência de cáries.
(PRODUTO DE SOLUBILIDADE) (UNESP 2004) Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO42– ), para que a água esteja em conformidade com o padrão para consumo humano, é de 250 mg·L–1. A análise da água de uma fonte revelou a existência de íons sulfato numa concentração de 5·10–3 mol·L–1.
Massas molares: Ca = 40,0 g·mol–1; O = 16,0 g·mol–1; S = 32,0 g·mol–1.
- a) Verifique se a água analisada está em conformidade com o padrão para consumo humano, de acordo com o VMP pelo Ministério da Saúde para a concentração do íon sulfato. Apresente seus cálculos.
- b) Um lote de água com excesso de íons sulfato foi tratado pela adição de íons cálcio até que a concentração de íons SO42– atingisse o VMP. Considerando que o Kps para o CaSO4 é 2,6·10–5, determine o valor para a concentração final dos íons Ca2+ na água tratada. Apresente seus cálculos.
RESPOSTA: a) O valor do VMP em mol/L é igual a 2,6 x 10-3 mol/L. Como o valor da concentração dos íons sulfatos presentes na água mineral é superior ao valor máximo permitido, a água não está adequada para o consumo humano; b) 1,0 x 10-2 mol/L.
(PRODUTO DE SOLUBILIDADE) (UNESP 2004) O leite de magnésia, utilizado para combater a acidez estomacal, é uma suspensão de hidróxido de magnésio (Mg(OH)2) em água. O hidróxido de magnésio é um composto pouco solúvel em água, que apresenta a constante do Produto de Solubilidade (KPS), a 25°C, igual a 3,2 × 10–11.
- a) Calcule a solubilidade do Mg(OH)2 em água pura, expressa em mol/L. Considere desprezível a concentração de íons OH– proveniente da dissociação da água e KPS = [Mg2+] x [OH–]2.
- b) Explique, utilizando cálculos, o que acontece com a solubilidade do Mg(OH)2 em solução que apresente pH = 12. Admita que a concentração de íons OH– da dissociação do Mg(OH)2 seja desprezível nesse valor de pH.
RESPOSTA: a) 2 x 10-4 mol/L; b) De acordo com o Princípio de Le Chatelier, o aumento da concentração de íons OH- desloca o equilíbrio no sentido dos reagentes, diminuindo a solubilidade do hidróxido de magnésio.
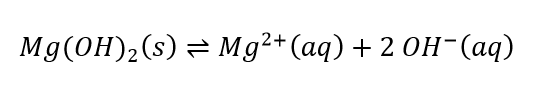 (EFEITO DO ÍON COMUM) (UFSCAR 2004) A água contendo íons como Ca2+, HCO3– e CO32-, em concentrações elevadas, é conhecida como água dura. A presença desses íons pode não ser prejudicial à saúde, mas torna a água imprópria para muitos usos domésticos e industriais. Para remoção do excesso de Ca2+, pode-se tratar a água dura em tanques de decantação, de acordo com os equilíbrios representados pelas equações:
(EFEITO DO ÍON COMUM) (UFSCAR 2004) A água contendo íons como Ca2+, HCO3– e CO32-, em concentrações elevadas, é conhecida como água dura. A presença desses íons pode não ser prejudicial à saúde, mas torna a água imprópria para muitos usos domésticos e industriais. Para remoção do excesso de Ca2+, pode-se tratar a água dura em tanques de decantação, de acordo com os equilíbrios representados pelas equações:
- a) O que acontece se, após o tratamento da água dura, for adicionada solução de HNO3 ao tanque de decantação? Justifique sua resposta.
- b) O que acontece se, durante o tratamento da água dura, for adicionada solução de NaOH? Justifique sua resposta.
RESPOSTA: a) A adição de HNO3, devido ao efeito do íon comum, aumenta a concentração de H3O+, deslocando as reações no sentindo dos reagentes e promovendo a dissolução do CaCO3 na solução; b) A adição de NaOH irá reduzir a quantidade de H3O+, que será neutralizado devido à presença dos íons OH–. Assim, os equilíbrios serão deslocados no sentido dos produtos e ocorrerá uma maior precipitação do CaCO3, acelerando o processo de tratamento da água dura.
2003
(HIDRÓLISE SALINA) (MAUÁ 2003) O carbonato de sódio (Na2CO3) é um composto utilizado na manufatura do vidro. Pergunta-se:
- a) Quantos mols de Na2CO3 existem em uma massa de 132 g de Na2CO3?
- b) O que se pode dizer a respeito do pH (meio ácido, básico ou neutro) de uma solução aquosa desse sal?
Massas molares: C = 12 g/mol/ O = 16,0 g/mol; Na = 23 g/mol.
(pH) (UNESP 2003) Dois comprimidos de aspirina, cada um com 0,36 g deste composto, foram dissolvidos em 200 mL de água.
- a) Calcule a concentração molar da aspirina nesta solução, em mol/L.
Dado: massa molar da aspirina = 180 g/mol.
- b) Considerando a ionização da aspirina segundo a equação
![]() e sabendo que ela se encontra 5% ionizada, calcule o pH desta solução.
e sabendo que ela se encontra 5% ionizada, calcule o pH desta solução.
RESPOSTA: a) 0,02 mol/L; b) pH = 3.
(HIDRÓLISE SALINA) (UNESP 2003) Quando se dissolvem sais em água, nem sempre a solução se apresenta neutra. Alguns sais podem reagir com a água e, como consequência, íons hidrogênio ou íons hidroxila ficam em excesso na solução, tornando-a ácida ou básica. Essa reação entre a água e pelo menos um dos íons formados na dissociação do sal denomina-se hidrólise.
- a) Na reação de neutralização do vinagre comercial (solução de ácido acético) com solução de hidróxido de sódio, obtém-se acetato de sódio (CH3COONa) aquoso como produto da reação. Escreva a reação de hidrólise do íon acetato, indicando se a hidrólise é ácida ou básica.
- b) Considerando que a constante de hidrólise para o íon acetato KH = 10–10 e a constante de autoprotólise da água Kw = 10–14, qual será o valor do pH de uma solução 0,01 mol/L de acetato de sódio?
RESPOSTA: a) Reação:
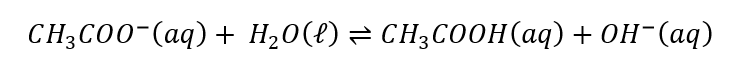 A hidrólise é ácida e o meio é básico;
A hidrólise é ácida e o meio é básico;
b) pH = 8.
(EFEITO DO ÍON COMUM) (UFSCAR 2003) Soluções aquosas de dicromato de potássio são alaranjadas, enquanto que soluções aquosas de cromato de potássio são amareladas. O equilíbrio químico dessas duas soluções pode ser representado pela mesma equação:
- a) Ao adicionarmos gotas de solução aquosa de hidróxido de sódio na solução de dicromato de potássio, o que acontecerá com a coloração dessa solução? Justifique.
- b) Considere o cromato de bário um sal insolúvel em água e o dicromato de bário solúvel. Se adicionarmos gotas de solução aquosa contendo íons Ba2+ numa solução de dicromato de potássio, haverá a formação de um precipitado. O que acontece com o precipitado se for adicionada solução aquosa de ácido clorídrico? Justifique.
RESPOSTA: a) A adição de NaOH irá consumir os íons H+, deslocando o equilíbrio no sentido dos produtos. Assim, a solução se torna amarelada.
b) A adição de ácido clorídrico aumenta a quantidade de íons H+, deslocando o equilíbrio no sentido dos reagentes. Isso faz com que a quantidade de íons cromato na solução seja reduzida e utilizando a reação de precipitação do cromato de bário, verificamos que a quantidade de precipitado reduz pois o equilíbrio é deslocado de modo a repor os íons cromato consumidos.
(HIDRÓLISE SALINA) (UFSCAR 2003) Para o combate da dengue, as Secretarias de Saúde orientam as pessoas para que não deixem água parada em vasos e plantas; estas devem ser regadas com solução de água sanitária contendo cerca de uma colher de sopa de água sanitária por litro de água. Um litro de água sanitária
contém cerca de 0,34 mol de hipoclorito de sódio (NaOCl).
- a) A solução de água sanitária é uma solução ácida? Justifique.
- b) Qual é o teor percentual em massa de NaOCl (massa molar 74,5 g/mol) na água sanitária que tem densidade igual a 1,0 g/mL?
RESPOSTA: a) Não, pois a água sanitária deriva de um ácido fraco e uma base forte. A solução resultante é básica; b) 2,33%.
2001
(pH) (UFSCAR 2001) O volume do estômago de um adulto varia de 50 mL quando vazio a 1 L quando cheio. Considerando-se que o volume do estômago é 450 mL e que seu conteúdo é uma solução aquosa com pH igual a 2, calcule
- a) quantos mols de H+ estão contidos no estômago;
- b) quantos gramas de hidrogenocarbonato de sódio serão necessários para neutralizar a acidez do estômago, supondo-se que todo H+ é proveniente do ácido clorídrico, um ácido forte.
(Massas molares em g/mol: Na = 23,0; H = 1,00; C = 12,0; O = 16,0; Cl = 35,4.)
RESPOSTA: a) 4,5 x 10-3 mol; b) 0,378 g de NaHCO3.
(EFEITO DO ÍON COMUM) (UFSCAR 2001) Quando se dissolve cloreto de cobalto (II) em ácido clorídrico, HCl (aq), ocorre o seguinte equilíbrio:
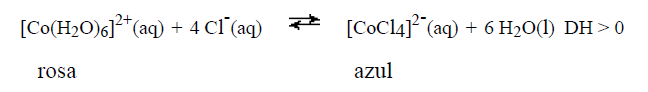 À temperatura ambiente, a cor dessa solução é violeta.
À temperatura ambiente, a cor dessa solução é violeta.
- a) O que acontece com a cor da solução quando ela é aquecida? Justifique a resposta.
- b) O que acontece com a cor da solução quando se adiciona mais ácido clorídrico? Justifique a resposta.
RESPOSTA: a) Quando ela é aquecida o equilíbrio é deslocado no sentido dos produtos, pois nesse sentido a reação é endotérmica. A coloração violeta vai se tornando mais azulada; b) Quando se adiciona mais ácido clorídrico, a concentração de Cl– aumenta (efeito do íon comum) e o equilíbrio é deslocado no sentido dos produtos, tornando a solução mais azulada.
EXERCÍCIOS EXTRAS