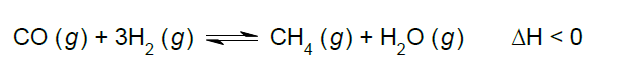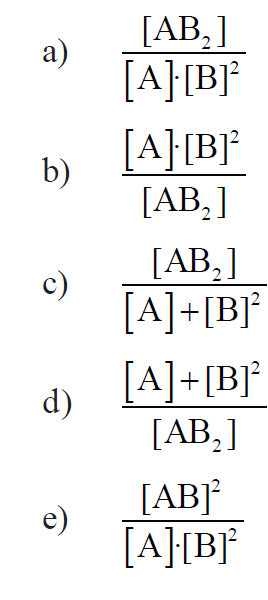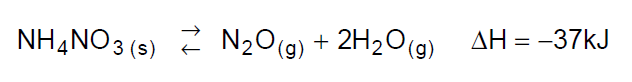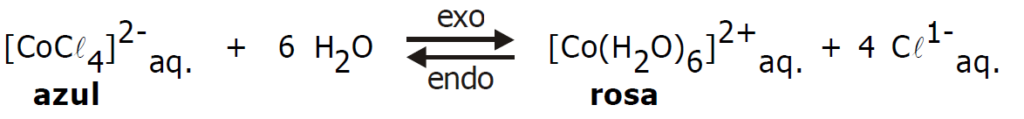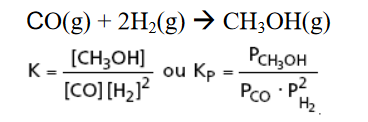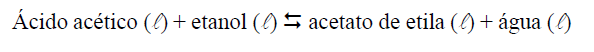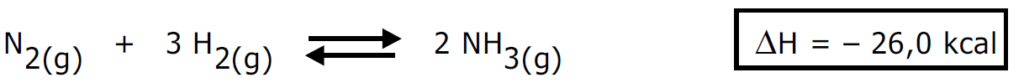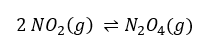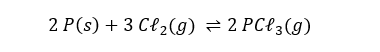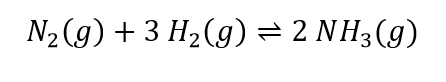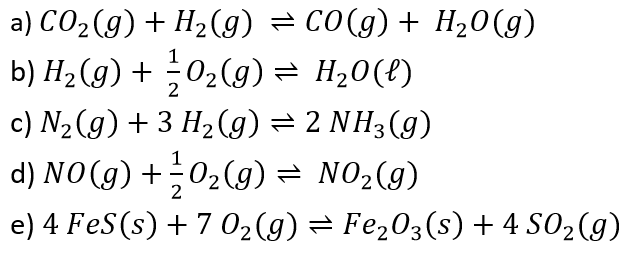CAIU NO ENEM!
D (ENEM 2015) Hipóxia ou mal das alturas consiste na diminuição de oxigênio O2 no sangue arterial do organismo. Por essa razão, muitos atletas apresentam mal-estar (dores de cabeça, tontura, falta de ar etc.) ao praticarem atividade física em altitudes elevadas. Nessas condições, ocorrerá uma diminuição na concentração de hemoglobina oxigenada (HbO2) em equilíbrio no sangue, conforme a relação:
Hb (aq) + O2 (aq) ⇄ HbO2 (aq)
Mal da montanha. Disponível em: www.feng.pucrs.br. Acesso em: 11 fev. 2015 (adaptado).
A alteração da concentração de hemoglobina oxigenada no sangue ocorre por causa do(a)
- a) elevação da pressão arterial.
- b) aumento da temperatura corporal.
- c) redução da temperatura do ambiente.
- d) queda da pressão parcial de oxigênio.
- e) diminuição da quantidade de hemácias.
CAIU NO VESTIBULAR!
2019
A (FCMSCSP 2019) A síntese do metano a partir da reação entre o gás monóxido de carbono e o gás hidrogênio é representada pelo equilíbrio
químico:
Para avaliar as alterações no sistema que resultassem no aumento da produção de metano, o sistema em equilíbrio passou por quatro testes, indicados na tabela:
 Resultaram no aumento da produção de metano no sistema apenas os testes de números
Resultaram no aumento da produção de metano no sistema apenas os testes de números
- a) 2 e 4.
- b) 1 e 3.
- c) 1 e 4.
- d) 2 e 3.
- e) 3 e 4.
2018
(CONSTANTE DE EQUILÍBRIO EM TERMOS DE CONCENTRAÇÃO – Kc) A (MACKENZIE 2018) Considerando-se o equilíbrio químico equacionado por A(g) + 2 B(g) ⇌ AB2(g), sob temperatura de 300 K, a alternativa que mostra a expressão correta da constante de equilíbrio em termos de concentração em mols por litro é
C (FGV SP 2018) O iodeto de hidrogênio, HI, é uma substância gasosa empregada em sínteses orgânicas. Uma das rotas de obtenção do HI pode ser feita, em um sistema fechado, por meio da reação do hidrogênio e do iodo como representado na equação
![]() A constante de equilíbrio dessa reação a 298 K é Keq = 794 Quando o compartimento reacional é aquecido a 700 K, é favorecida a formação de __________ , pois na equação, no sentido da direita, a reação é _____________. O valor da constante de equilíbrio da reação de formação do HI gasoso a 700 K é ___________ do que a 298 K.
A constante de equilíbrio dessa reação a 298 K é Keq = 794 Quando o compartimento reacional é aquecido a 700 K, é favorecida a formação de __________ , pois na equação, no sentido da direita, a reação é _____________. O valor da constante de equilíbrio da reação de formação do HI gasoso a 700 K é ___________ do que a 298 K.
As lacunas são preenchidas, correta e respectivamente, por:
- a) H2 e I2 … endotérmica … maior
- b) H2 e I2 … endotérmica … menor
- c) H2 e I2 … exotérmica … menor
- d) HI … endotérmica … menor
- e) HI … exotérmica … maior
2017
C (FUVEST 2017) A hemoglobina (Hb) é a proteína responsável pelo transporte de oxigênio. Nesse processo, a hemoglobina se transforma em oxi-hemoglobina (Hb(O2)n). Nos fetos, há um tipo de hemoglobina diferente da do adulto, chamada de hemoglobina fetal. O transporte de oxigênio pode ser representado pelo seguinte equilíbrio:
![]() em que Hb representa tanto a hemoglobina do adulto quanto a hemoglobina fetal.
em que Hb representa tanto a hemoglobina do adulto quanto a hemoglobina fetal.
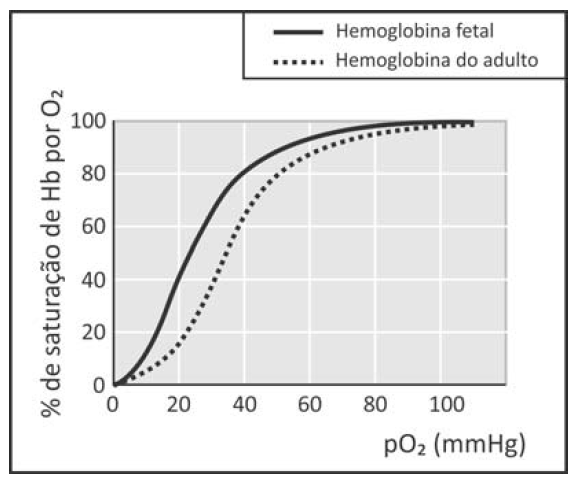
A figura mostra a porcentagem de saturação de Hb por O2 em função da pressão parcial de oxigênio no sangue humano, em determinado pH e em determinada temperatura.
A porcentagem de saturação pode ser entendida como:
Com base nessas informações, um estudante fez as seguintes afirmações:
- Para uma pressão parcial de O2 de 30 mmHg, a hemoglobina fetal transporta mais oxigênio do que a hemoglobina do adulto.
- Considerando o equilíbrio de transporte de oxigênio, no caso de um adulto viajar do litoral para um local de grande altitude, a concentração de Hb em seu sangue deverá aumentar, após certo tempo, para que a concentração de Hb(O2)n seja mantida.
- Nos adultos, a concentração de hemoglobina associada a oxigênio é menor no pulmão do que nos tecidos.
É correto apenas o que o estudante afirmou em
- a) I.
- b) II.
- c) I e II.
- d) I e III.
- e) II e III.
C (ESPCEX (AMAN) 2017) Os corais fixam-se sobre uma base de carbonato de cálcio (CaCO3). produzido por eles mesmos. O carbonato de cálcio em contato com a água do mar e com o gás carbônico dissolvido pode estabelecer o seguinte equilíbrio químico para a formação do hidrogenocarbonato de cálcio:
CaCO3 (s) + CO2 (g) + H2O (l) ⇄ Ca(HCO3)2 (aq)
Considerando um sistema fechado onde ocorre o equilíbrio químico da reação mostrada acima, assinale a alternativa correta.
- a) Um aumento na concentração de carbonato causará um deslocamento do equilíbrio no sentido inverso da reação, no sentido dos reagentes.
- b) A diminuição da concentração do gás carbônico não causará o deslocamento do equilíbrio químico da reação.
- c) Um aumento na concentração do gás carbônico causará um deslocamento do equilíbrio no sentido direto da reação, o de formação do produto.
- d) Um aumento na concentração de carbonato causará, simultaneamente, um deslocamento do equilíbrio nos dois sentidos da reação.
- e) Um aumento na concentração do gás carbônico causará um deslocamento do equilíbrio no sentido inverso da reação, no sentido dos reagentes.
A (UFJF-PISM 3 2017) Considere os seguintes equilíbrios que envolvem CO2 (g) e suas constantes de equilíbrio correspondentes:
CO2 (g) ⇄ CO (g) + ½ O2 (g) K1
2 CO (g) + O2 (g) ⇄ 2 CO2 (g) K2
Marque a alternativa que correlaciona as duas constantes de equilíbrio das duas reações anteriores.
- a) K2 = 1/(K1)2
- b) K2 = (K1)2
- c) K2 = K1
- d) K2 = 1/K1
- e) K2 = (K1)1/2
A (UECE 2017) Um estudante de química retirou água do seguinte sistema em equilíbrio:
2 NO2(g) + CH4 (g) ⇄ CO2 (g) + 2 H2O (l) + N2 (g)
Em seguida, esse aluno constatou acertadamente que
- a) a concentração de metano diminuiu.
- b) o equilíbrio se desloca para a esquerda.
- c) a concentração do dióxido de carbono diminuiu.
- d) a concentração do nitrogênio gasoso diminuiu.
B (MACKENZIE 2017) Em um balão de capacidade igual a 10 L, foram adicionados 1 mol da espécie A2(g) e 2 mols da espécie B2(g). Tais reagentes sofreram transformação de acordo com a equação a seguir:
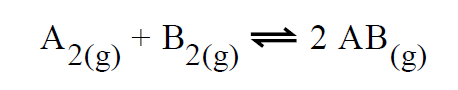 Considerando-se que, no estado de equilíbrio químico, a concentração da espécie AB(g) seja de 0,1 mol·L-1, a constante de equilíbrio (KC), para esse processo, é aproximadamente igual a
Considerando-se que, no estado de equilíbrio químico, a concentração da espécie AB(g) seja de 0,1 mol·L-1, a constante de equilíbrio (KC), para esse processo, é aproximadamente igual a
- a) 0,25
- b) 1,33
- c) 5,00
- d) 6,66
- e) 7,50
2016
A (UEMG 2016) Zuenir Ventura, em sua crônica “Bonito por Natureza”, coloca o seguinte texto sobre a Gruta do Lago Azul.
“O passeio vale todos os sacrifícios, se é que se pode falar assim. Porque o espetáculo de descida é quase alucinógeno: é um milagre que aquelas estalactites da finura de agulha que descem do teto da gruta possam se sustentar como se fossem gotas interrompidas.”
VENTURA, 2012, p.127.
A equação química que mostra a formação das estalactites está representada a seguir.
Ca2+ (aq) + 2 HCO3– (aq) ⇄ CaCO3 (s) + CO2 (g) + H2O (l)
É CORRETO afirmar que a formação das estalactites é favorecida na seguinte condição:
- a) Evaporação constante da água.
- b) Diminuição da concentração de íons Ca2+.
- c) Retirada de íons de bicarbonato.
- d) Abaixamento da temperatura no interior da caverna.
2015
B (FUVEST 2015) A Gruta do Lago Azul (MS), uma caverna composta por um lago e várias salas, em que se encontram espeleotemas de origem carbonática (estalactites e estalagmites), é uma importante atração turística. O número de visitantes, entretanto, é controlado, não ultrapassando 300 por dia. Um estudante, ao tentar explicar tal restrição, levantou as seguintes hipóteses:
- Os detritos deixados indevidamente pelos visitantes se decompõem, liberando metano, que pode oxidar os espeleotemas.
- O aumento da concentração de gás carbônico que é liberado na respiração dos visitantes, e que interage com a água do ambiente, pode provocar a dissolução progressiva dos espeleotemas.
- A concentração de oxigênio no ar diminui nos períodos de visita, e essa diminuição seria compensada pela liberação de O2 pelos espeleotemas.
O controle do número de visitantes, do ponto de vista da Química, é explicado por
- a) I, apenas.
- b) II, apenas.
- c) III, apenas.
- d) I e III, apenas.
- e) I, II e III.
2013
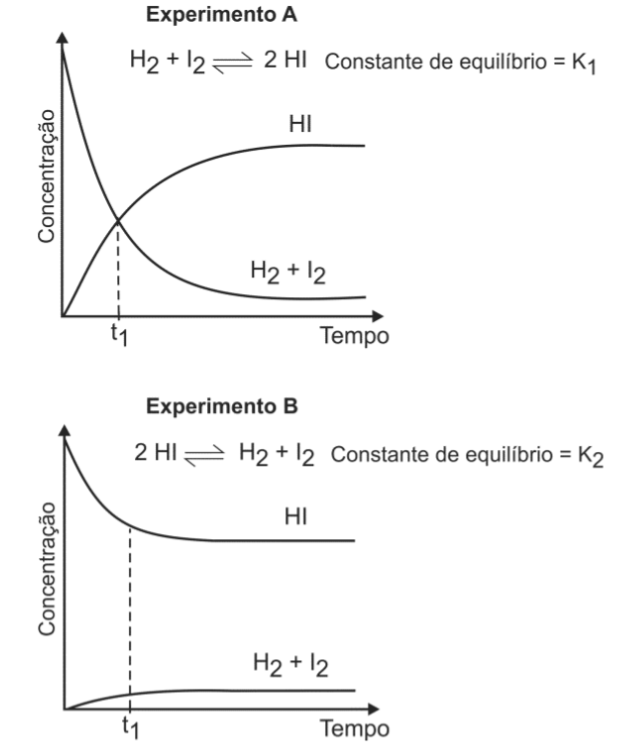
E (FUVEST 2013) A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em recipientes fechados, partindo-se de uma mistura equimolar de H2 e I2 (experimento A) ou somente de HI (experimento B).
Pela análise dos dois gráficos, pode-se concluir que
- a) no experimento A, ocorre diminuição da pressão total no interior do recipiente, até que o equilíbrio seja atingido.
- b) no experimento B, as concentrações das substâncias (HI, H2 e I2) são iguais no instante t1.
- c) no experimento A, a velocidade de formação de HI aumenta com o tempo.
- d) no experimento B, a quantidade de matéria (em mols) de HI aumenta até que o equilíbrio seja atingido.
- e) no experimento A, o valor da constante de equilíbrio (K1) é maior do que 1.
2009
(CONSTANTE DE EQUILÍBRIO EM TERMOS DE PRESSÃO – KP) (UNESP 2009) A produção de grafita artificial vem crescendo significativamente, uma vez que grafita natural de boa qualidade para uso industrial é escassa. Em atmosferas ricas em dióxido de carbono, a 1 000 ºC, a grafita reage segundo a reação:
![]() A 1 000 ºC, no estado de equilíbrio, as pressões parciais de CO e CO2 são 1,50 atm e 1,25 atm, respectivamente. Calcule o valor da constante de equilíbrio (Kp) para a reação nessa temperatura.
A 1 000 ºC, no estado de equilíbrio, as pressões parciais de CO e CO2 são 1,50 atm e 1,25 atm, respectivamente. Calcule o valor da constante de equilíbrio (Kp) para a reação nessa temperatura.
RESPOSTA: 1,8
2008
(DESLOCAMENTO DE EQUILÍBRIO) D (PUC MG 2008) Considere o equilíbrio:
É CORRETO afirmar que:
- a) o equilíbrio será deslocado para a esquerda quando a temperatura for diminuída.
- b) a reação de decomposição do nitrato de amônio sólido é endotérmica.
- c) um aumento na concentração de N2O(g) deslocará o equilíbrio para a direita.
- d) um aumento de pressão deslocará o equilíbrio para a esquerda.
2006
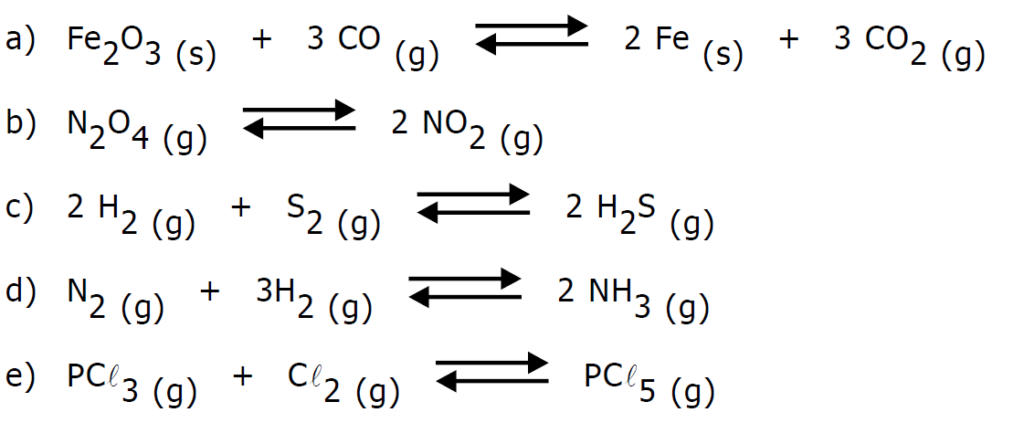
(DESLOCAMENTO DE EQUILÍBRIO) E (MACKENZIE 2006)
O aumento da produção de CCl4, no sistema em equilíbrio acima, pode ser obtido
- a) com a diminuição da quantidade de CHCl3.
- b) com o aumento da pressão total, a temperatura constante.
- c) com a diminuição da quantidade de Cl2.
- d) com o decréscimo da pressão total, a temperatura constante.
- e) com a diminuição da quantidade de HCl.
2005
(DESLOCAMENTO DE EQUILÍBRIO) A (MACKENZIE 2005) O equilíbrio químico que não será afetado pelo aumento ou diminuição da pressão é
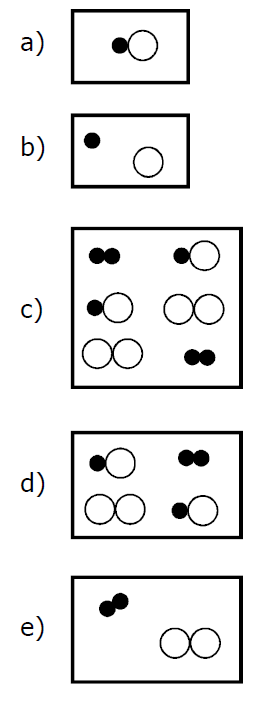
(EQUILÍBRIO) D (MACKENZIE 2005)
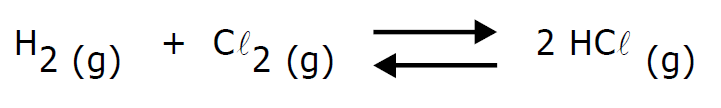 A reação acima ocorreu num sistema fechado, entre quantidades estequiométricas de reagentes. Após alcançado o equilíbrio, pode-se representar o sistema por
A reação acima ocorreu num sistema fechado, entre quantidades estequiométricas de reagentes. Após alcançado o equilíbrio, pode-se representar o sistema por
(DESLOCAMENTO DE EQUILÍBRIO) D (MACKENZIE 2005)
Essa equação representa a reação que ocorre no “galinho do tempo”, enfeite cuja superfície é impregnada por uma solução em que se estabelece o equilíbrio dado acima. O “galinho do tempo” indica, pela cor, como o tempo vai ficar.
Fazem-se as afirmações:
- Quando a umidade relativa do ar está alta, o galinho fica rosa.
- Quando a temperatura aumenta, o galinho fica azul.
- Quando o galinho fica azul, há indicativo de tempo bom, sem previsão de chuva.
Das afirmações,
- a) somente II está correta.
- b) somente I e III estão corretas.
- c) somente III está correta.
- d) I, II e III estão corretas.
- e) somente I e II estão corretas.
(Kc/Kp/DESLOCAMENTO DE EQUILÍBRIO) (UNESP 2005) O metanol é um produto com elevada toxidez, podendo provocar náusea, vômito, perturbação visual, confusão mental e conduzindo à morte em casos mais graves de intoxicação. Em alguns países ele é utilizado como combustível, em especial em competições automobilísticas, e pode ser obtido industrialmente pela reação do monóxido de carbono com o hidrogênio.
- a) Escreva a equação química para a reação do monóxido de carbono com o hidrogênio, produzindo o metanol, e a expressão para a constante de equilíbrio para esta reação no estado gasoso.
- b) Mantidas as demais condições constantes, qual o efeito esperado do aumento da pressão sobre a produção do metanol neste processo? Justifique.
RESPOSTA: a)
b) De acordo com o Princípio de Le Chatelier, o aumento da pressão favorece o lado de menor volume (produtos), favorecendo a formação do metanol.
2004
(DESLOCAMENTO DE EQUILÍBRIO) A (MACKENZIE 2004)
![]() Da hidrogenação catalítica do eteno, equacionada acima, fazem-se as afirmações:
Da hidrogenação catalítica do eteno, equacionada acima, fazem-se as afirmações:
- aumentando-se a pressão do sistema, aumenta a quantidade de etano produzido.
- aumentando-se a concentração de C2H4, diminui a quantidade de produto.
- a presença do catalisador não interfere no equilíbrio.
- aumentando-se a temperatura do sistema, o equilíbrio desloca-se no sentido endotérmico.
São corretas, somente:
- a) I, III e IV
- b) II e IV
- c) I e III
- d) I e II
- e) I, II e IV
(CONSTANTE DE EQUILÍBRIO EM TERMOS DE CONCENTRAÇÃO – Kc) (UNIFESP 2004) Ácido acético e etanol reagem reversivelmente, dando
acetato de etila e água.
A 100 ºC, a constante de equilíbrio vale 4.
- a) Calcule a quantidade, em mol, de ácido acético que deve existir no equilíbrio, a 100 ºC, para uma mistura inicial contendo 2 mol de acetato de etila e 2 mol de água.
- b) Partindo-se de 1,0 mol de etanol, para que 90% dele se transformem em acetato de etila, a 100º C, calcule a quantidade de ácido acético, em mol, que deve existir no equilíbrio. Justifique sua resposta com cálculos.
RESPOSTA: a) 2/3 de mol de ácido acético; b) 2,025 mol de ácido acético no equilíbrio.
2002
(DESLOCAMENTO DE EQUILÍBRIO) A (MACKENZIE 2002)
O rendimento da reação de obtenção da amônia diminui, se a:
- a) pressão do sistema diminuir.
- b) concentração do gás nitrogênio aumentar.
- c) concentração do gás hidrogênio aumentar.
- d) temperatura do sistema diminuir.
- e) pressão do sistema aumentar.
(DESLOCAMENTO DE EQUILÍBRIO) D (MACKENZIE 2002)
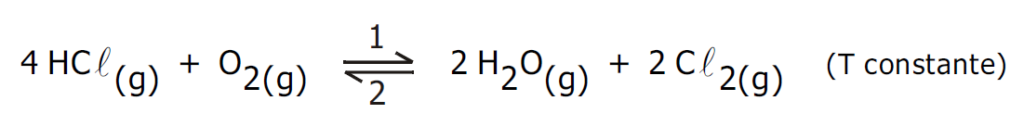 Da reação acima equacionada, pode-se afirmar que o equilíbrio:
Da reação acima equacionada, pode-se afirmar que o equilíbrio:
- a) desloca-se no sentido 2, se a pressão aumentar.
- b) desloca-se no sentido 1, se a concentração do Cl2 aumentar.
- c) desloca-se no sentido 1, se for adicionado um catalisador.
- d) desloca-se no sentido 2, se a concentração de gás oxigênio diminuir.
- e) não se altera, se a pressão diminuir.
EXERCÍCIOS EXTRAS
(CSA 2011 – BIB – U1) Em um recipiente de 10 L são colocados 184 g de NO2. Determine a quantidade, em mols, das substâncias que irão se encontrar em equilíbrio, sabendo-se que a constante de equilíbrio do processo abaixo vale Kc = 25, na temperatura da experiência.
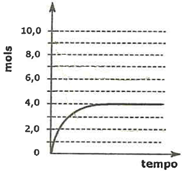
(CSA 2011 – BIB – U3a) Num recipiente de 2 litros são misturados 0,6 mol de P(s) com 1,4 mol de Cℓ2(g). A variação da quantidade de tricloreto de fósforo, em função do tempo, encontra-se representada abaixo:
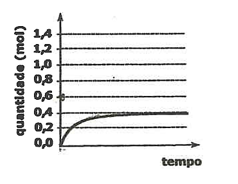 Determine a constante de equilíbrio (Kc) para a reação:
Determine a constante de equilíbrio (Kc) para a reação:
(CSA 2011 – BIB – U5b) Em um recipiente são colocadas quantidades equimolares de nitrogênio e hidrogênio gasosos. Sabendo-se que a pressão total inicial do sistema é 14 atm e que a pressão total no equilíbrio é de 10 atm, determine a constante de equilíbrio em termos de pressão da reação
A (CSA 2011 – BIB – U19) (UFRN) Sabendo-se que KP = KC (RT)∆n, podemos afirmar que KP = KC, para:
A (CSA 2011 – BIB – U20) (MACK 2002)
![]() O rendimento da reação de obtenção da amônia diminui, se a:
O rendimento da reação de obtenção da amônia diminui, se a:
- a) pressão do sistema diminuir.
- b) concentração do gás nitrogênio aumentar.
- c) concentração do gás hidrogênio aumentar.
- d) temperatura do sistema diminuir.
- e) pressão do sistema aumentar.
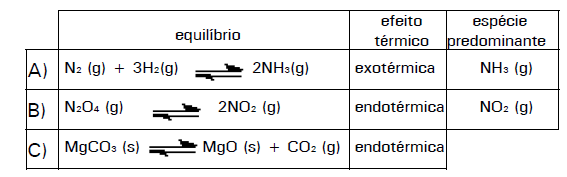
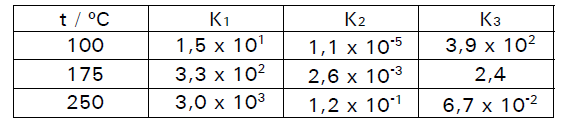
A (CSA 2011 – BIB – U21) (FUVEST 2002) Considere os equilíbrios abaixo e o efeito térmico da reação da esquerda para a direita, bem como a espécie predominante nos equilíbrios A e B, à temperatura de 175 °C.
O equilíbrio A foi estabelecido misturando-se, inicialmente, quantidades estequiométricas de N2(g) e H2(g). Os equilíbrios B e C foram estabelecidos a partir de, respectivamente, N2O4 e MgCO3 puros. A tabela abaixo traz os valores numéricos das constantes desses três equilíbrios, em função da temperatura, não necessariamente na mesma ordem em que os equilíbrios foram apresentados. As constantes referem-se a pressões parciais em atm.
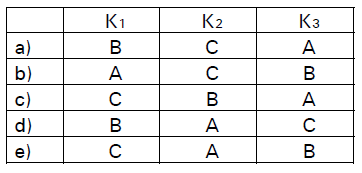
Logo, as constantes K1, K2 e K3 devem corresponder, respectivamente, a:
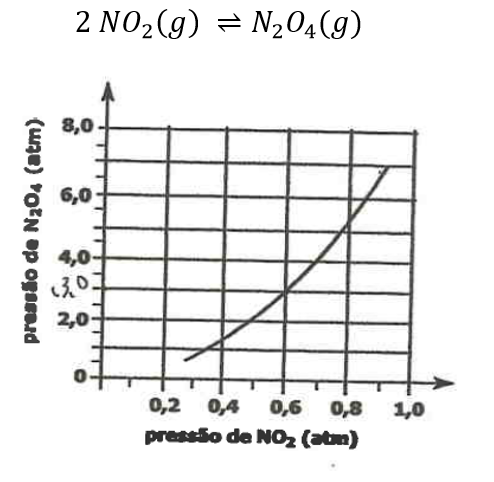
D (CSA 2011 – BIB – U22) (FUVEST 2000) No gráfico, estão os valores das pressões parciais de NO2 e de N2O4, para diferentes misturas desses dois gases, quando, a determinada temperatura, é atingido o equilíbrio:
Com os dados desse gráfico, pode-se calcular o valor da constante (KP) do equilíbrio atingido, naquela temperatura. Seu valor numérico é próximo de:
- a) 1
- b) 2
- c) 4
- d) 8
- e) 12
(CSA 2010 – BIB – U1) 84 g de nitrogênio são misturados com 64 g de oxigênio num recipiente, numa determinada temperatura. Sabendo-se que a constante de equilíbrio da reação:
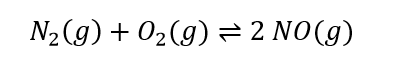 Nesta temperatura vale 12, determine a massa de óxido de nitrogênio obtida no equilíbrio.
Nesta temperatura vale 12, determine a massa de óxido de nitrogênio obtida no equilíbrio.
(CSA 2010 – BIB – U4) Em um recipiente de 10 litros são misturados 10 mol de enxofre sólido com 8 mol de oxigênio gasoso. A variação da quantidade de trióxido de enxofre até o estabelecimento do equilíbrio está representada no gráfico a seguir, de acordo com a equação:
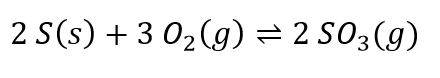 Acrescente a esse gráfico as curvas correspondentes às quantidades de reagentes envolvidas nessa reação e calcule o valor da constante de equilíbrio (KC) do processo, nessas condições.
Acrescente a esse gráfico as curvas correspondentes às quantidades de reagentes envolvidas nessa reação e calcule o valor da constante de equilíbrio (KC) do processo, nessas condições.