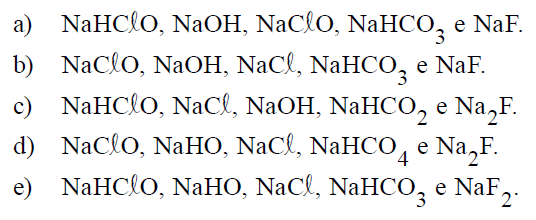QUÍMICA – LISTA DE EXERCÍCIOS SOBRE FUNÇÕES INORGÂNICAS
(ÁCIDOS/BASES/SAIS/ÓXIDOS)
CAIU NO ENEM!
CAIU NO VESTIBULAR!
2018
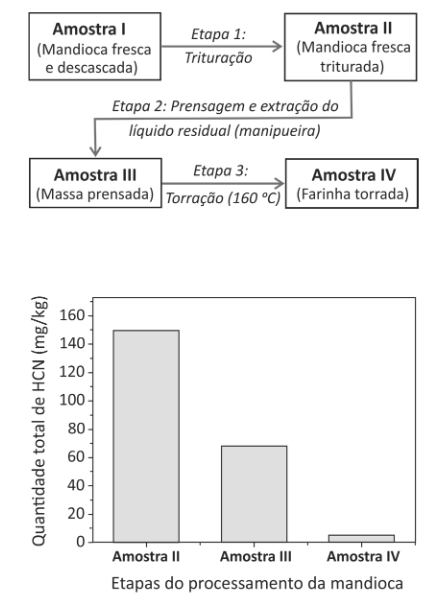
D (FUVEST 2018) A mandioca, uma das principais fontes de carboidratos da alimentação brasileira, possui algumas variedades conhecidas popularmente como “mandioca brava”, devido a sua toxicidade. Essa toxicidade se deve à grande quantidade de cianeto de hidrogênio (HCN) liberado quando o tecido vegetal é rompido.
Após cada etapa do processamento para a produção de farinha de mandioca seca, representado pelo esquema a seguir, quantificou se o total de HCN nas amostras, conforme mostrado no gráfico que acompanha o esquema.
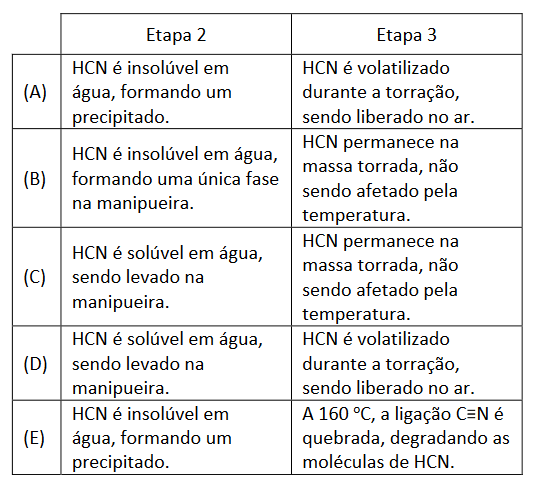
O que ocorre com o HCN nas Etapas 2 e 3?
D (MACKENZIE 2018) Indicadores são substâncias que mudam de cor na presença de íons H+ e OH– livres em uma solução. Justamente por esta propriedade, são usados para indicar o pH, ou seja, os indicadores “indicam” se uma solução é ácida ou básica. Esses indicadores podem ser substâncias sintéticas como a fenolftaleína e o azul de bromotimol, ou substâncias que encontramos em nosso cotidiano, como por exemplo, o suco de repolho roxo, que apresenta uma determinada coloração em meio ácido e uma outra coloração em meio básico. A tabela a seguir ilustra as cores características dessas substâncias nos intervalos ácido e básico.
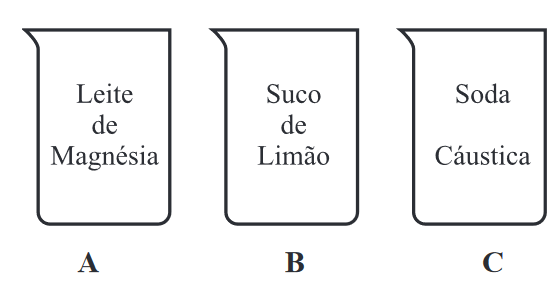
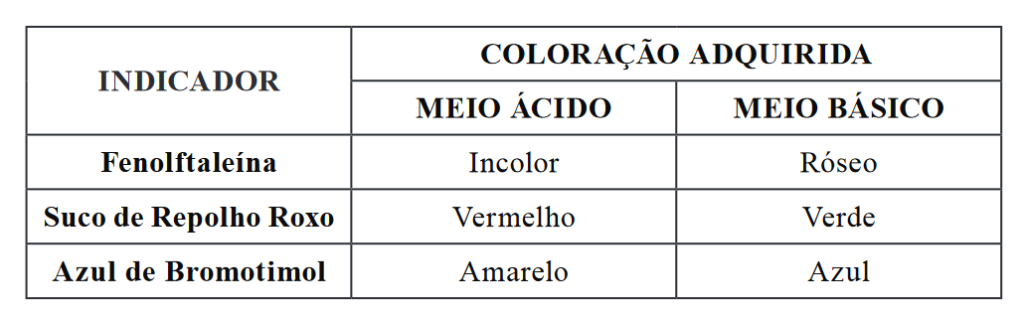 Assim, um estudante preparou três soluções aquosas concentradas de diferentes substâncias, de acordo com a ilustração abaixo.
Assim, um estudante preparou três soluções aquosas concentradas de diferentes substâncias, de acordo com a ilustração abaixo.
- a) róseo, vermelho e amarelo.
- b) incolor, verde e amarelo.
- c) incolor, verde e azul.
- d) róseo, vermelho e azul.
- e) incolor, vermelho e azul.
D (UFJF – PISM 1 2018) Os antiácidos são utilizados para aumentar o pH do estômago diminuindo dessa forma a acidez estomacal. O rótulo de um antiácido líquido indica que este contém Al(OH)3 (A) e Mg(OH)2 (B) em sua composição. Já outro antiácido, vendido em forma de comprimido sólido, apresenta em sua composição NaHCO3 (C) e Na2CO3 (D). Os nomes dos compostos citados são:
- a) (A) óxido de alumínio, (B) óxido de magnésio, (C) hidrogenocarbonato de sódio e (D) carbonato de sódio
- b) (A) óxido de alumínio, (B) óxido de magnésio, (C) carbonato de sódio e (D) bicarbonato de sódio
- c) (A) óxido de alumínio, (B) óxido de manganês, (C) bicarbonato de sódio e (D) carbonato de sódio
- d) (A) hidróxido de alumínio, (B) hidróxido de magnésio, (C) hidrogenocarbonato de sódio e (D) carbonato de sódio
- e) (A) hidróxido de alumínio, (B) hidróxido de manganês, (C) carbonato de sódio e (D) hidrogenocarbonato de sódio
A (UERJ 2018) O cloreto de sódio, principal composto obtido no processo de evaporação da água do mar, apresenta a fórmula química NaCl.
Esse composto pertence à seguinte função química:
- a) sal
- b) base
- c) ácido
- d) óxido
2017
A (UFJF – PISM 1 2017) Um estudante foi ao laboratório e realizou uma série de experimentos para identificar um determinado composto químico. As observações sobre esse composto estão descritas abaixo:
 Baseado nas observações feitas pelo estudante, pode-se afirmar que o composto analisado é:
Baseado nas observações feitas pelo estudante, pode-se afirmar que o composto analisado é:
- a) HCl
- b) NaOH
- c) NaCl
- d) I2
- e) CH4
D (UFJF – PISM 1 2017)Sais inorgânicos constituídos por cátions e ânions de carga unitária dissociam-se quase completamente, já sais contendo cátions e ânions com uma carga ≥ 2 estão muito menos dissociados. Com base nessa informação, marque a alternativa na qual está o sal cuja solução deve apresentar a maior quantidade de íon metálico livre.
- a) Fluoreto de magnésio.
- b) Sulfato de sódio.
- c) Nitrato de alumínio.
- d) Cloreto de potássio.
- e) Fosfato de lítio.
2016
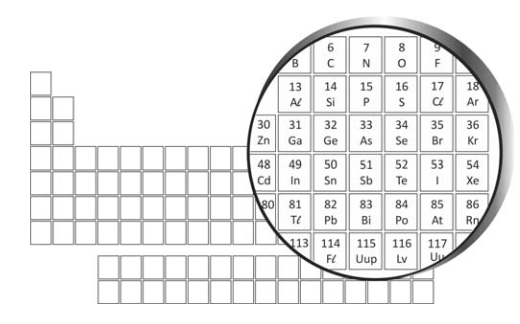
D (FUVEST 2016) O fleróvio (Fl ) é um elemento químico artificial, de número atômico 114. Na tabela periódica, está situado imediatamente abaixo do elemento de número atômico 82, que é o chumbo (Pb), como é mostrado na figura a seguir:
Até o momento, só foi possível sintetizar poucos átomos de fleróvio na forma dos isótopos 288 e 289, pela fusão dos elementos plutônio e cálcio em um acelerador de partículas. Para o fleróvio-289, o processo de síntese pode ser representado pela equação nuclear a seguir:
![]() Considere as seguintes afirmações:
Considere as seguintes afirmações:
- A aparência macroscópica do fleróvio é desconhecida, mas, provavelmente, será a de um sólido metálico.
- Na formação do fleróvio-288, por processo análogo ao da síntese do fleróvio-289, são liberados 3 prótons.
- No grupo da tabela periódica ao qual pertence o fleróvio, há elementos que formam óxidos covalentes.
É correto o que se afirma apenas em
- a) I
- b) II
- c) III
- d) I e III
- e) II e III
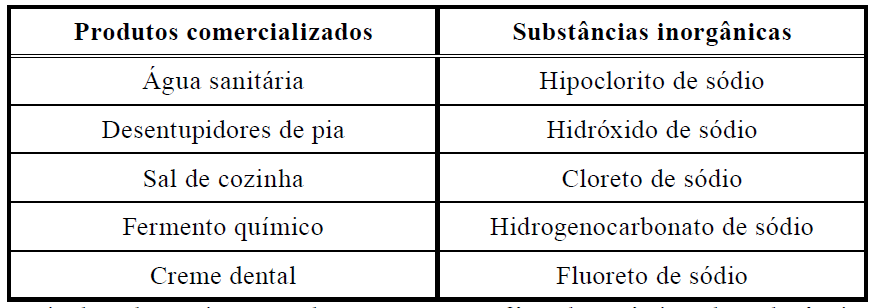
B (MACKENZIE 2016) Alguns produtos comercializados no mercado têm como principais componentes substâncias inorgânicas, nas quais o elemento químico sódio encontra-se presente. Na tabela abaixo, segue a relação de algumas dessas substâncias.
Assinale a alternativa na qual encontram-se as fórmulas químicas das substâncias inorgânicas presentes nos produtos comercializados, na ordem que aparecem na tabela, de cima para baixo.
C (UFJF – PISM 1 2016) O cientista Svante August Arrhenius estudou o efeito de passagem de corrente elétrica na migração de espécies eletricamente carregadas. Assinale a alternativa que descreve a situação na qual ocorre condução de corrente elétrica.
- a) Substância iônica no estado sólido.
- b) Substância molecular não ionizada em solução.
- c) Substância iônica em solução.
- d) Substância molecular no estado gasoso.
- e) Substância molecular em estado sólido.
C (UFJF – PISM 1 2016) Os metais de transição constituem o grande bloco da parte central da Tabela Periódica. Os óxidos formados por metais de transição são muito importantes na indústria de pigmentos de tintas. Assinale a alternativa que contém apenas óxidos de metais de transição do bloco d da Tabela Periódica.
- a) CdS e Fe2O3
- b) Al2O3 e Na2O
- c) Cr2O3 e Co2O3
- d) ZnO e Mn3(PO4)2
- e) Ti2O e Al2O3
2014
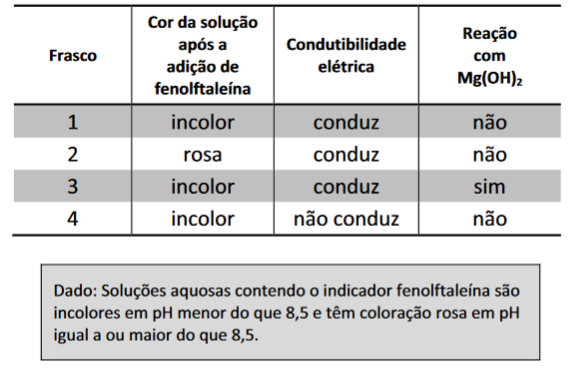
B (FUVEST 2014) Em um laboratório químico, um estudante encontrou quatro frascos (1, 2, 3 e 4) contendo soluções aquosas incolores de sacarose, KCl, HCl e NaOH, não necessariamente nessa ordem. Para identificar essas soluções,fez alguns experimentos simples, cujos resultados são apresentados na tabela a seguir:
- a) HCl, NaOH, KCl e sacarose.
- b) KCl, NaOH, HCl e sacarose.
- c) HCl, sacarose, NaOH e KCl.
- d) KCl, sacarose, HCl e NaOH.
- e) NaOH, HCl, sacarose e KCl.
2012
E (UFJF – PISM 1 2012) Um aluno do curso de química recebeu um frasco contendo uma amostra desconhecida. Para identificar essa substância, ele realizou diferentes experimentos e observou que:
I. quando dissolvida em água, conduzia corrente elétrica;
II. possuía como um dos constituintes um metal alcalino terroso;
III. era um sal.
Baseado nessas informações, pode-se afirmar que a amostra era o(a):
- a) cloreto de sódio.
- b) óxido de cálcio.
- c) ácido clorídrico.
- d) sacarose.
- e) sulfato de magnésio.
2010
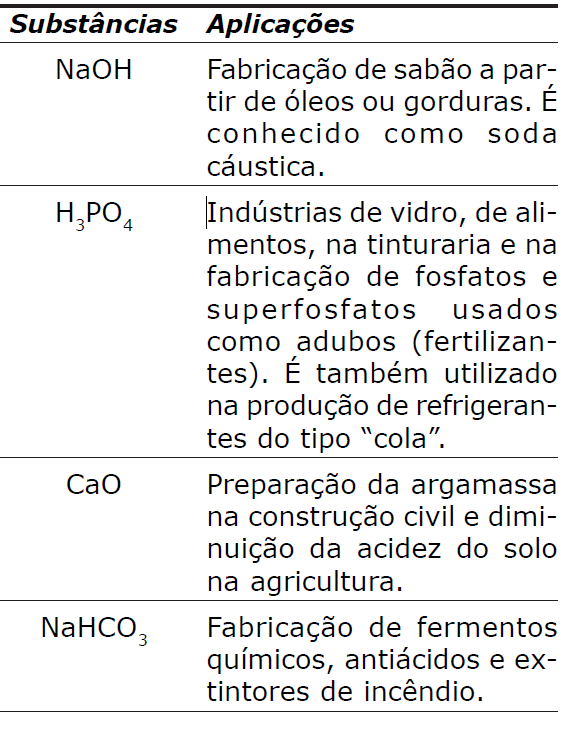
E (UTFPR 2010) A tabela a seguir relaciona algumas substâncias químicas e suas aplicações frequentes no cotidiano.
Estas substâncias, ordenadas de cima para baixo, pertencem, respectivamente, às funções:
- a) base, sal, ácido e óxido.
- b) sal, base, ácido e óxido.
- c) base, óxido, ácido e sal.
- d) ácido, base, sal e óxido.
- e) base, ácido, óxido e sal.
C (UFJF – PISM 1 2010) Para testar se um material é ou não condutor de corrente elétrica, pode-se utilizar uma montagem experimental, conforme apresentado a seguir. É importante lembrar que, na realização do experimento, não há contato direto entre as extremidades desencapadas.
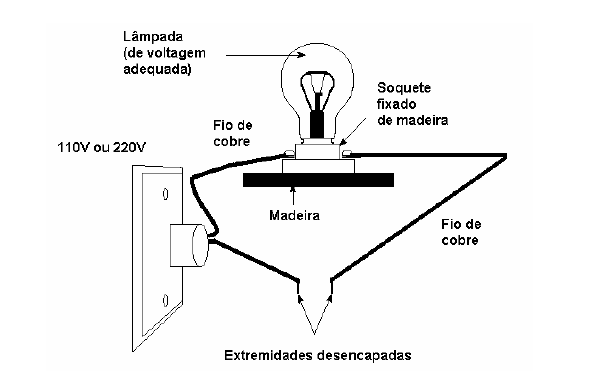
Ao colocarmos, simultaneamente, ambas as extremidades desencapadas do fio de cobre em um único recipiente, a lâmpada acenderá quando o recipiente contiver:
- a) água pura no estado líquido, porque a água é um composto iônico.
- b) uma solução aquosa de sacarose (C12H22O11), porque a sacarose é um composto molecular que se dissocia quando dissolvida em água, formando íons.
- c) uma solução aquosa de ácido clorídrico, porque esse é um composto molecular que se dissocia quando dissolvido em água, formando íons.
- d) etanol (CH3CH2OH), porque esse é um composto iônico.
- e) cloreto de sódio no estado sólido, porque esse sal é um composto iônico.
2009
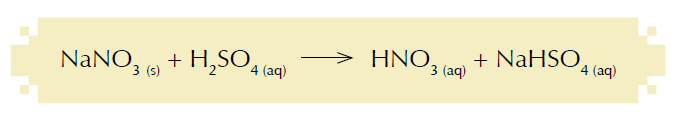 Escreva os nomes dos reagentes empregados nesse processo e apresente a fórmula estrutural plana do ácido nítrico.
Escreva os nomes dos reagentes empregados nesse processo e apresente a fórmula estrutural plana do ácido nítrico.- a) Ácido é toda substância que, em solução aquosa, sofre dissociação iônica, liberando como único cátion o H–.
- b) O hidróxido de sódio, em solução aquosa, sofre ionização, liberando como único tipo de cátion o H+.
- c) Óxidos anfóteros não reagem com ácidos ou com bases.
- d) Os peróxidos apresentam na sua estrutura o grupo (O2)-2, no qual cada átomo de oxigênio apresenta número de oxidação (NOX) igual a -4 (menos quatro).
- e) Sais são compostos capazes de se dissociar na água liberando íons, mesmo que em pequena porcentagem, dos quais pelo menos um cátion é diferente de H3O+ e pelo menos um ânion é diferente de OH–.
E (ESPCEX 2009) Um professor de Química, durante uma aula experimental, pediu a um de seus alunos que fosse até o armário e retornasse trazendo, um por um, nesta ordem: um oxiácido inorgânico; um diácido; um sal de metal alcalino; uma substância que, após aquecimento, pode gerar dióxido de carbono (CO2(g)); e um sal ácido.
Assinale a alternativa que corresponde à sequência de fórmulas moleculares que atenderia corretamente ao pedido do professor.
a) H2SO3, H3BO3, CaSO4, NaHCO3, Ca(Cl)ClO
b) H3PO3, H2SO4, NaClO, HClO2, CaSO4·2 H2O
c) H2CO3, H2SO4, Na2CO3, MgCO3, Al(OH)2Cl
d) H2S, H2CO3, Ca3(PO4)2, H2CO3, NaLiSO4
e) HClO4, H2CO3, Na2CO3, CaCO3, NaHCO3
D (ESPCEX 2009) Analise as afirmações I, II, III e IV abaixo referente(s) à(s) característica(s) e/ou informação(ões) sobre algumas substâncias, nas condições ambientes:
I- A substância é a principal componente do sal de cozinha e pode ser obtida pela evaporação da água do mar. Dentre seus muitos usos podemos citar: a produção de soda cáustica e a conservação de carnes.
II- A substância é classificada como composta, e pode fazer parte da chuva ácida. Dentre seus muitos usos, podemos citar: utilização em baterias de automóveis e na produção de fertilizantes, como o sulfato de amônio.
III-A substância em solução aquosa é vendida em drogarias e utilizada como antisséptico e alvejante. Algumas pessoas utilizam essa substância para clarear pelos e cabelos.
IV-A substância é classificada como simples, tem seu ponto de ebulição igual a -195,8 0C, é a mais abundante no ar atmoférico e reage com o gás hidrogênio produzindo amônia.
As substâncias que correspondem às afirmações I, II, III e IV são, respectivamente,
- a) cloreto de sódio, ácido sulfúrico, permanganato de potássio, dióxido de enxofre
- b) cloreto de sódio,ácido clorídrico, peróxido de hidrogênio, dióxido de carbono
- c) cloreto de sódio, ácido muriático, óxido férrico, gás oxigênio
- d) cloreto de sódio, ácido sulfúrico, peróxido de hidrogênio, gás nitrogênio
- e) sulfato de alumínio, ácido muriático, óxido ferroso, gás nitrogênio