CAIU NO ENEM!
CAIU NO VESTIBULAR!
2019
E (FCMSCSP 2019) Na lata de um desodorante do tipo spray há as seguintes advertências: Não coloque essa embalagem no fogo ou no incinerador. Não exponha essa embalagem ao sol nem a temperaturas superiores a 50 ºC. Pode explodir, se aquecido.
A razão da possível explosão é o aumento de pressão à qual fica sujeito o conteúdo da lata devido ao aquecimento. Para ilustrar esse aumento, considere que uma lata de desodorante cujo conteúdo esteja a uma pressão de 2 × 105 Pa a 27 ºC seja atirada em uma fogueira, de modo que sua temperatura atinja 177 ºC. Considerando que o volume da lata seja constante e que seu conteúdo seja um gás ideal, a pressão à qual esse gás fica submetido devido a esse aquecimento sofre um aumento de
- a) 10%.
- b) 30%.
- c) 20%.
- d) 40%.
- e) 50%.
2018
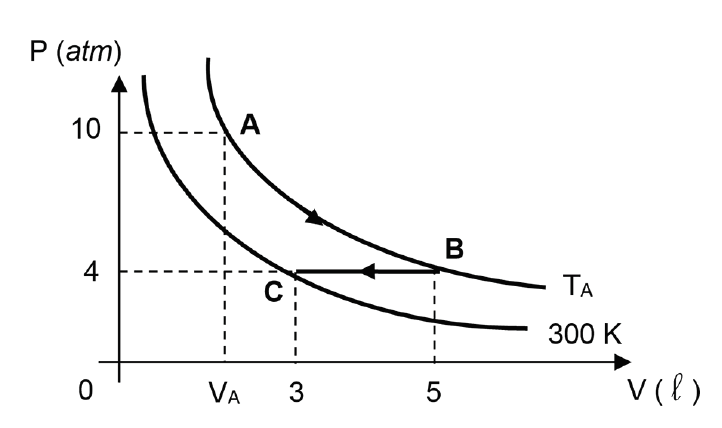
D (MACKENZIE 2018) A figura abaixo representa duas isotérmicas em que certa massa gasosa, inicialmente no estado A, sofre uma transformação atingindo o estado B, que por sua vez sofre uma transformação, atingindo o estado C. A temperatura TA e o volume VA são iguais a
- a) 200 K e 5 L.
- b) 300 K e 2 L.
- c) 400 K e 4 L.
- d) 500 K e 2 L.
- e) 500 K e 4 L.
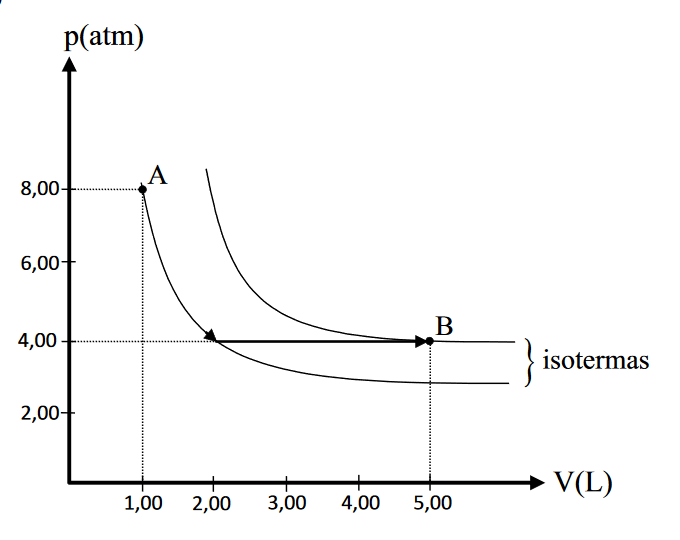
E (MACKENZIE 2018) Um gás perfeito, que tem um volume de 12,0 L, encontra-se no interior de um frasco sob pressão de 3,00 atm e com temperatura de 200 K. Inicialmente, o gás sofre uma transformação isotérmica, de tal forma que sua pressão passa a ser de 9,00 atm, a seguir, o gás sofre uma transformação segundo a lei de Gay-Lussac, atingindo uma temperatura de 500 K. Os volumes, após as duas transformações, respectivamente, são iguais a
- a) 10,0 L e 4,00 L.
- b) 4,00 L e 2,00 L.
- c) 10,0 L e 2,00 L.
- d) 2,00 L e 4,00 L.
- e) 4,00 L e 10,0 L.
- a) 7,5
- b) 9,0
- c) 15,0
- d) 37,5
D (UFRGS 2018) Utilizados em diversas áreas de pesquisa, balões estratosféricos são lançados com seu invólucro impermeável parcialmente cheio de gás, para que possam suportar grande expansão à medida em que se elevam na atmosfera. Um balão, lançado ao nível do mar, contém gás hélio à temperatura de 27°C, ocupando um volume inicial Vi. O balão sobe e atinge uma altitude superior a 35 km, onde a pressão do ar é 0,005 vezes a pressão ao nível do mar e a temperatura é -23 °C. Considerando que o gás hélio se comporte como um gás ideal, qual é, aproximadamente, a razão Vf/Vi, entre os volumes final Vf e inicial Vi?
- a) 426.
- b) 240.
- c) 234.
- d) 167.
- e) 17.
2017
E (UDESC 2017) Uma certa quantidade de gás ideal está no estado inicial de pressão, volume e temperatura dados, respectivamente, por Po , Vo e To. Este gás é comprimido isobaricamente até que o seu volume se reduza à metade. A seguir, a pressão é aumentada isocoricamente até o dobro de sua pressão inicial.
Considerando a informação, ao final do processo, o gás:
- a) volta ao seu estado inicial.
- b) apresenta o dobro da temperatura inicial.
- c) apresenta o mesmo volume inicial.
- d) apresenta a mesma pressão inicial.
- e) apresenta a mesma temperatura inicial.
C (FGV SP 2017) Ao ser admitido no interior da câmara de combustão do motor de uma motocicleta, o vapor de etanol chega a ocupar o volume de 120 cm3 sob pressão de 1,0 atm e temperatura de 127 °C. Após o tempo de admissão, o pistão sobe, o volume ocupado por essa mistura diminui para 20 cm3, e a pressão aumenta para 12 atm. Considerando a mistura um gás ideal e desprezando perdas de calor devido à rápida compressão, a temperatura do gás resultante desse processo no interior da câmara passa a ser, em °C, de
- a) 473.
- b) 493.
- c) 527.
- d) 573.
- e) 627.
2016
A (FUVEST 2016) Uma garrafa tem um cilindro afixado em sua boca, no qual um êmbolo pode se movimentar sem atrito, mantendo constante a massa de ar dentro da garrafa, como ilustra a figura.
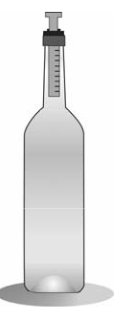 Inicialmente, o sistema está em equilíbrio à temperatura de 27°C. O volume de ar na garrafa é igual a 600 cm3 e o êmbolo tem uma área transversal igual a 3 cm2. Na condição de equilíbrio, com a pressão atmosférica constante, para cada 1 °C de aumento de temperatura do sistema, o êmbolo subirá aproximadamente
Inicialmente, o sistema está em equilíbrio à temperatura de 27°C. O volume de ar na garrafa é igual a 600 cm3 e o êmbolo tem uma área transversal igual a 3 cm2. Na condição de equilíbrio, com a pressão atmosférica constante, para cada 1 °C de aumento de temperatura do sistema, o êmbolo subirá aproximadamente
- a) 0,7 cm
- b) 14 cm
- c) 2,1 cm
- d) 30 cm
- e) 60 cm
B (UFRGS 2016) Assinale a alternativa que preenche corretamente as lacunas do enunciado abaixo, na ordem em que aparecem.
Segundo a Teoria Cinética dos Gases, um gás ideal é constituído de um número enorme de moléculas cujas dimensões são desprezíveis, comparadas às distâncias médias entre elas. As moléculas movem-se continuamente em todas as direções e só há interação quando elas colidem entre si.
Nesse modelo de gás ideal, as colisões entre as moléculas são …….., e a energia cinética total das moléculas …….. .
- a) elásticas – aumenta
- b) elásticas – permanece constante
- c) elásticas – diminui
- d) inelásticas – aumenta
- e) inelásticas – diminui
D (UFRGS 2016) Nos gráficos I e II abaixo, p representa a pressão a que certa massa de gás ideal está sujeita, T a sua temperatura e V o volume por ela ocupado.
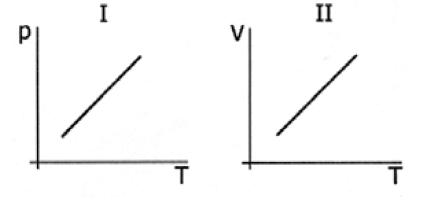 Escolha a alternativa que identifica de forma correta as transformações sofridas por esse gás, representadas, respectivamente, em I e II.
Escolha a alternativa que identifica de forma correta as transformações sofridas por esse gás, representadas, respectivamente, em I e II.
- a) Isobárica e isocórica.
- b) Isotérmica e isocórica.
- c) Isotérmica e isobárica.
- d) Isocórica e isobárica.
- e) Isocórica e isotérmica.
2015
C (UERJ 2015) Um mergulhador precisa encher seu tanque de mergulho, cuja capacidade é de 1,42 x 10-2 m3 a uma pressão de 140 atm e sob temperatura constante. O volume de ar, em m3, necessário para essa operação, à pressão atmosférica de 1 atm, é aproximadamente igual a:
- a) 1/4
- b) 1/2
- c) 2
- d) 4
- a) 600 K
- b) 800 K
- c) 750 K
- d) 650 K
- e) 700 K
2014
B (UECE 2014) Considere um gás ideal que passa por dois estados, através de um processo isotérmico reversível. Sobre a pressão P e o volume V desse gás, ao longo desse processo, é correto afirmar-se que
- a) PV é crescente de um estado para outro.
- b) PV é constante.
- c) PV é decrescente de um estado para outro.
- d) PV é inversamente proporcional à temperatura do gás.
B (UECE 2014) Seja um recipiente metálico fechado e contendo ar comprimido em seu interior. Considere desprezíveis as deformações no recipiente durante o experimento descrito a seguir: a temperatura do ar comprimido é aumentada de 24 °C para 40 °C. Sobre esse gás, é correto afirmar-se que
- a) sua pressão permanece constante, pois já se trata de ar comprimido.
- b) sua pressão aumenta.
- c) sua energia interna diminui, conforme prevê a lei dos gases ideais.
- d) sua energia interna permanece constante, pois o recipiente não muda de volume e não há trabalho realizado pelo sistema.
C (UDESC 2014) Um sistema fechado, contendo um gás ideal, sofre um processo termodinâmico isobárico, provocando mudança de temperatura de 200°C para 400°C. Assinale a alternativa que representa a razão aproximada entre o volume final e o inicial do gás ideal.
- a) 1,5
- b) 0,5
- c) 1,4
- d) 2,0
- e) 1,0
2013
E (FATEC 2013) Uma das atrações de um parque de diversões é a barraca de tiro ao alvo, onde espingardas de ar comprimido lançam rolhas contra alvos, que podem ser derrubados.
Ao carregar uma dessas espingardas, um êmbolo comprime 120 mL de ar atmosférico sob pressão de 1 atm, reduzindo seu volume para 15 mL. A pressão do ar após a compressão será, em atm,
Admita que o ar se comporte como um gás ideal e que o processo seja isotérmico.
- a) 0,2.
- b) 0,4.
- c) 4,0.
- d) 6,0.
- e) 8,0.
2012
C (AFA 2012) Um motorista calibra os pneus de seu carro com uma pressão de 30 libras/pol2 a uma temperatura de 27 °C Após uma viagem, a temperatura deles subiu para 47 °C Desprezando-se a variação de volume dos pneus e sabendo-se que 10% da massa de ar contida em um dos pneus escapou pela válvula durante a viagem, a pressão do ar neste pneu, ao término desta viagem, em libras/pol2 é de aproximadamente
- a) 25
- b) 26
- c) 29
- d) 32
E (PUC RJ 2012) Um processo acontece com um gás ideal que está dentro de um balão extremamente flexível em contato com a atmosfera. Se a temperatura do gás dobra ao final do processo, podemos dizer que:
- a) a pressão do gás dobra, e seu volume cai pela metade.
- b) a pressão do gás fica constante, e seu volume cai pela metade.
- c) a pressão do gás dobra, e seu volume dobra.
- d) a pressão do gás cai pela metade, e seu volume dobra.
- e) a pressão do gás fica constante, e seu volume dobra.
E (UFPR 2012) Segundo a teoria cinética, um gás é constituído por moléculas que se movimentam desordenadamente no espaço do reservatório onde o gás está armazenado. As colisões das moléculas entre si e com as paredes do reservatório são perfeitamente elásticas. Entre duas colisões sucessivas, as moléculas descrevem um MRU. A energia cinética de translação das moléculas é diretamente proporcional à temperatura do gás. Com base nessas informações, considere as seguintes afirmativas:
- As moléculas se deslocam todas em trajetórias paralelas entre si.
- Ao colidir com as paredes do reservatório, a energia cinética das moléculas é conservada.
- A velocidade de deslocamento das moléculas aumenta se a temperatura do gás for aumentada.
Assinale a alternativa correta.
- a) Somente a afirmativa 1 é verdadeira.
- b) Somente a afirmativa 2 é verdadeira.
- c) Somente a afirmativa 3 é verdadeira.
- d) Somente as afirmativas 1 e 2 são verdadeiras.
- e) Somente as afirmativas 2 e 3 são verdadeiras.
A (ESPCEX (AMAN) 2012) Para um gás ideal ou perfeito temos que:
- a) as suas moléculas não exercem força uma sobre as outras, exceto quando colidem.
- b) as suas moléculas têm dimensões consideráveis em comparação com os espaços vazios entre elas.
- c) mantido o seu volume constante, a sua pressão e a sua temperatura absoluta são inversamente proporcionais.
- d) a sua pressão e o seu volume, quando mantida a temperatura constante, são diretamente proporcionais.
- e) sob pressão constante, o seu volume e a sua temperatura absoluta são inversamente proporcionais.
2011
D (FUVEST 2011) Um laboratório químico descartou um frasco de éter, sem perceber que, em seu interior, havia ainda um resíduo de 7,4 g de éter, parte no estado líquido, parte no estado gasoso. Esse frasco, de 0,8 L de volume, fechado hermeticamente, foi deixado sob o sol e, após um certo tempo, atingiu a temperatura de equilíbrio T = 37 °C, valor acima da temperatura de ebulição do éter. Se todo o éter no estado líquido tivesse evaporado, a pressão dentro do frasco seria
- a) 0,37 atm.
- b) 1,0 atm.
- c) 2,5 atm.
- d) 3,1 atm.
- e) 5,9 atm.
(UEM 2011) Assinale o que for correto.
01) O volume de uma dada massa gasosa será inversamente proporcional à pressão exercida sobre ela, se a temperatura desse gás for mantida constante.
02) Mantida constate a pressão de uma massa gasosa, o volume dessa massa gasosa é diretamente proporcional a sua temperatura absoluta.
04) O número de moléculas em volumes iguais de gases diferentes à mesma temperatura e pressão é o mesmo.
08) Não existe relação entre a energia cinética das moléculas de um gás e a temperatura do gás.
16) A pressão exercida por um gás sobre as paredes do recipiente que o contém é consequência das contínuas e incessantes colisões das moléculas desse gás contra as paredes do recipiente.
RESPOSTA: 01 + 02 + 04 + 16 = 23
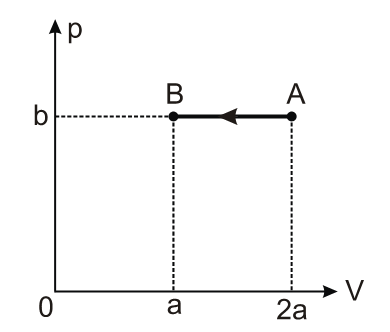
D (EEWB 2011) Considere a compressão isobárica AB sofrida por uma amostra de gás perfeito e representada no diagrama pressão x volume, mostrado abaixo.
Admita que no estado A, a temperatura do gás perfeito seja igual a 127 ºC. A temperatura atingida pelo gás ao atingir o estado B vale:
- a) 473 K
- b) 400 °C
- c) 200 °F
- d) – 73 °C
C (IFSP 2011) No alto de uma montanha a 8 °C, um cilindro munido de um êmbolo móvel de peso desprezível possui 1 litro de ar no seu interior. Ao levá-lo ao pé da montanha, cuja pressão é de 1 atmosfera, o volume do cilindro se reduz a 900 cm3 e sua temperatura se eleva em 6 °C. A pressão no alto da montanha é aproximadamente, em atm, de
- a) 0,66.
- b) 0,77.
- c) 0,88.
- d) 0,99.
- e) 1,08.
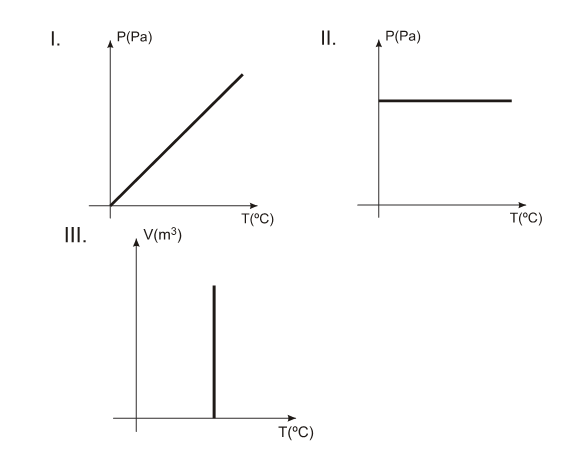
A (UDESC 2011) Uma dada massa gasosa, que está limitada em um cilindro por um êmbolo móvel, sofre as transformações representadas pelos seguintes gráficos:
Assinale a alternativa que contém a correta classificação das três transformações apresentadas acima.
- a) isovolumétrica / II. isobárica / III. isotérmica.
- b) isotérmica / II. isobárica / III. isovolumétrica.
- c) isobárica / II. isovolumétrica / III. isotérmica.
- d) isovolumétrica / II. isotérmica / III. isobárica.
- e) I. isobárica / II. isotérmica / III. isovolumétrica.
2010
A (ESPCEX 2010) O gráfico da pressão (P) em função do volume (V) no desenho abaixo representa as transformações sofridas por um gás ideal. Do ponto A até o ponto B, o gás sofre uma transformação isotérmica, do ponto B até o ponto C, sofre uma transformação isobárica e do ponto C até o ponto A, sofre uma transformação isovolumétrica. Considerando TA , TB e TC as temperaturas absolutas do gás nos pontos A, B e C, respectivamente, pode-se afirmar que:
- a) TA = TB e TB < TC
- b) TA = TB e TB > TC
- c) TA = TC e TB > TA
- d) TA = TC e TB < TA
- e) TA = TB = TC
2009
E (ESPCEX 2009) Em um experimento de aquecimento de gases, observa-se que um determinado recipiente totalmente fechado resiste a uma pressão interna máxima de 2,4.104 N/m2. No seu interior, há um gás perfeito com temperatura de 230 K e pressão de 1,5.104 N/m2. Desprezando a dilatação térmica do recipiente, podemos afirmar que a máxima temperatura que o gás pode atingir, sem romper o recipiente, é de
- a) 243 K
- b) 288 K
- c) 296 K
- d) 340 K
- e) 368 K
2008
A (ACAFE 2008-1) A Lei de Boyle afirma que o produto da pressão e volume é constante; assim, se a pressão duplicar, o volume terá que ser dividido à metade. Num mergulho a 30 m de profundidade, ocorre a denominada “espremedura”, que tende a colapsar o tórax e traz severa dor e dano físico. Podemos deduzir, com isso, que a profundidade de 30 m excede o limite para mergulho seguro com respiração retida. Considere, agora, um indivíduo que começa com 4 litros de gás nos pulmões sob pressão atmosférica normal de 1 atmosfera e calcule em quanto esse volume será reduzido se ele for 30 m abaixo da superfície. Para esse cálculo, considere que o mergulhador começa na superfície com 1 atmosfera e que, para cada 10 m de descida, é acrescentada 1 atmosfera de pressão. Assinale a alternativa que apresenta em quanto será reduzido o volume de oxigênio desse indivíduo:
- a) 3,0 litros.
- b) 1,0 litro.
- c) 2,0 litros.
- d) 2,5 litros.
- e) 1,5 litros.