QUÍMICA – LISTA DE EXERCÍCIOS SOBRE GEOMETRIA MOLECULAR E POLARIDADE
CAIU NO ENEM!
CAIU NO VESTIBULAR!
2019
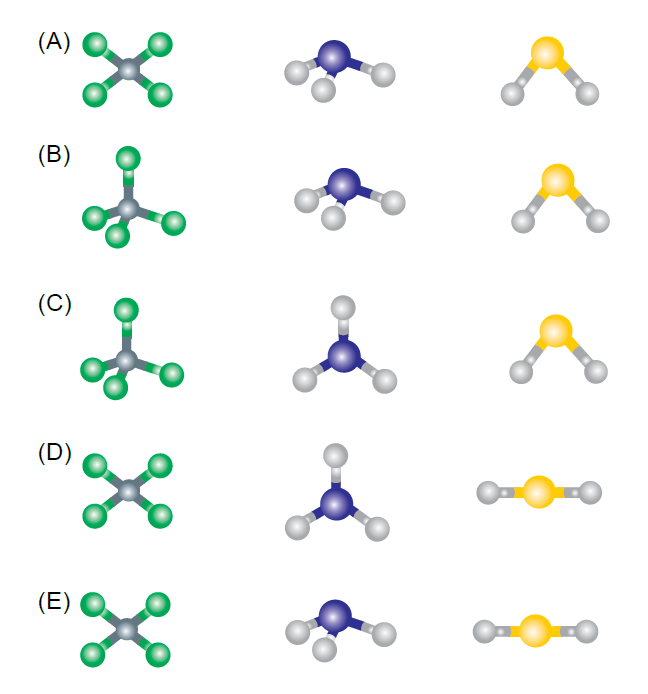
B (FCMSCSP 2019) O tetracloreto de carbono (CCl4), a amônia (NH3) e o sulfeto de hidrogênio (H2S) são substâncias moleculares que apresentam, respectivamente, as seguintes formas geométricas:
2016
D (UFRGS 2016) O dióxido de enxofre, em contato com o ar, forma trióxido de enxofre que, por sua vez, em contato com a água, forma ácido sulfúrico. Na coluna da esquerda, abaixo, estão listadas 5 substâncias envolvidas nesse processo. Na coluna da direita, características das moléculas dessa substância.
| 1 – SO2
2 – SO3 3 – H2SO4 4 – H2O 5 – O2 |
( ) tetraédrica, polar
( ) angular, polar ( ) linear, apolar ( ) trigonal, apolar |
A sequência correta de preenchimento dos parênteses, de cima para baixo, é
- a) 1 – 4 – 3 – 2.
- b) 2 – 3 – 5 – 1.
- c) 2 – 3 – 4 – 5.
- d) 3 – 1 – 5 – 2.
- e) 3 – 4 –2 – 1.
2012
D (UFJF – PISM 1 2012) A água é conhecida como solvente universal por ser capaz de dissolver diversas substâncias. Por isso, a água que normalmente usamos é raramente pura e pode apresentar propriedades diferentes daquelas encontradas no laboratório. Entretanto, há muitos compostos que são essencialmente insolúveis em água.
A figura a seguir mostra a geometria da molécula de água com seus respectivos ângulo e comprimento de ligação.
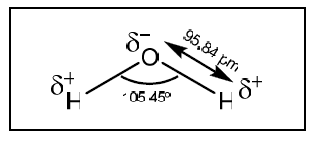
Sobre a molécula de água e suas propriedades, assinale a alternativa CORRETA.
- a) Um cátion qualquer deve interagir com a molécula de água através do seu polo positivo.
- b) A água dissolve qualquer composto apolar.
- c) O ângulo mostrado na figura está incorreto, pois deveria ser exatamente de 180°.
- d) A geometria da água é angular, devido aos pares de elétrons não ligantes (isolados) presentes no átomo de oxigênio.
- e) A polaridade da água é praticamente nula, uma vez que os vetores dos dipolos das ligações O-H se cancelam mutuamente.
A (UFJF – PISM 1 2012) A água sanitária é uma solução aquosa de hipoclorito de sódio (NaClO) com teor de cloro ativo (Cl2), sendo usada, frequentemente, como desinfetante e agente alvejante. Sobre as moléculas de NaClO e Cl2, é CORRETO afirmar que:
- a) Cl2 apresenta ligação covalente e geometria linear.
- b) Cl2 apresenta ligação iônica e é uma molécula apolar.
- c) NaClO apresenta ligação iônica e esse composto é classificado como hidrogeno-sal.
- d) NaClO apresenta apenas ligações covalentes.
- e) Cl2 e NaClO apresentam ligação iônica.