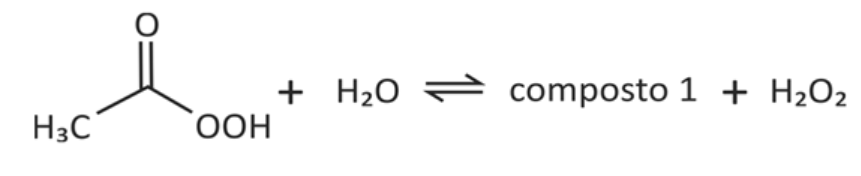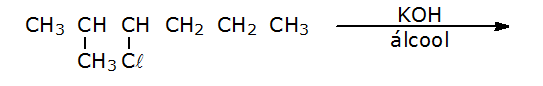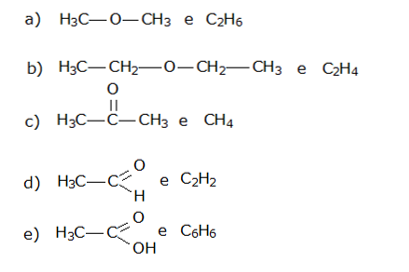CAIU NO ENEM!
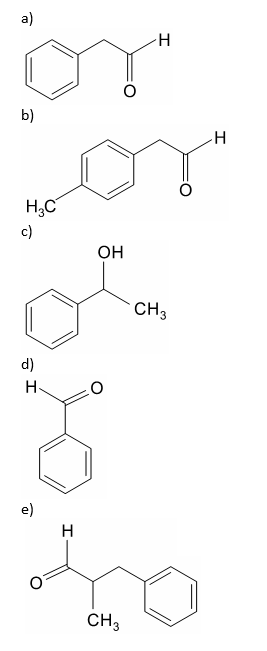
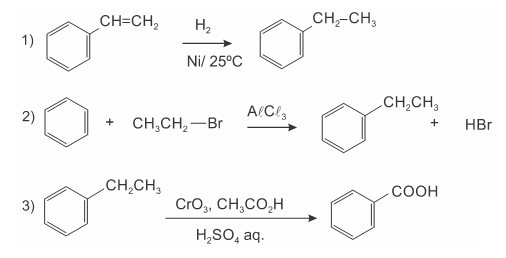
A (ENEM 2015) O permanganato de potássio (KMnO4) é um agente oxidante forte muito empregado tanto em nível laboratorial quanto industrial. Na oxidação de alcenos de cadeia normal, como o 1-fenil-1-propeno ilustrado na figura, o KMnO4 é utilizado para a produção de ácidos carboxílicos.
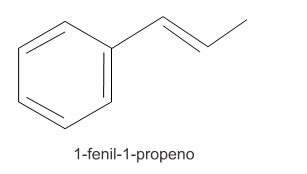 Os produtos obtidos na oxidação do alceno representado, em solução aquosa de KMnO4 são:
Os produtos obtidos na oxidação do alceno representado, em solução aquosa de KMnO4 são:
- a) Ácido benzoico e ácido etanoico.
- b) Ácido benzoico e ácido propanoico.
- c) Ácido etanoico e ácido 2-feniletanoico.
- d) Ácido 2-feniletanoico e ácido metanoico.
- e) Ácido 2-feniletanoico e ácido propanoico.
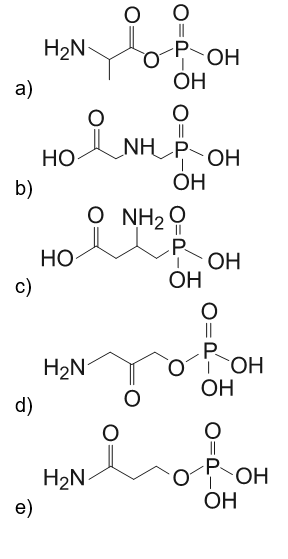
B (ENEM 2013) O glifosato (C3H8NO5P) é um herbicida pertencente ao grupo químico das glicinas, classificado como não seletivo. Esse composto possui os grupos funcionais carboxilato, amino e fosfonato. A degradação do glifosato no solo é muito rápida e realizada por grande variedade de microrganismos, que usam o produto como fonte de energia e fósforo. Os produtos da degradação são o ácido aminometilfosfônico (AMPA) e o N-metilglicina (sarcosina):
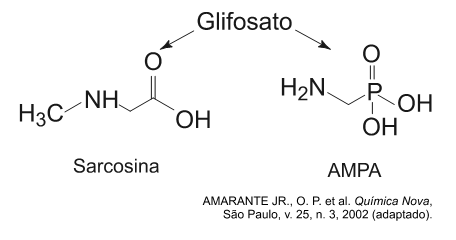 A partir do texto e dos produtos de degradação apresentados, a estrutura química que representa o glifosato é:
A partir do texto e dos produtos de degradação apresentados, a estrutura química que representa o glifosato é:
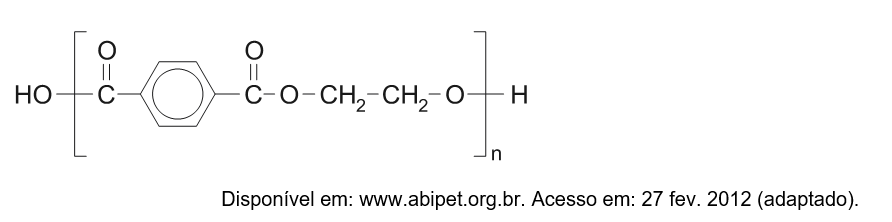
D (ENEM 2013) O uso de embalagens plásticas descartáveis vem crescendo em todo o mundo, juntamente com o problema ambiental gerado por seu descarte inapropriado. O politereftalato de etileno (PET), cuja estrutura é mostrada, tem sido muito utilizado na indústria de refrigerantes e pode ser reciclado e reutilizado. Uma das opções possíveis envolve a produção de matérias-primas, como o etilenoglicol (1,2-etanodiol), a partir de objetos compostos de PET pós-consumo.
Com base nas informações do texto, uma alternativa para a obtenção de etilenoglicol a partir do PET é a
- a) solubilização dos objetos.
- b) combustão dos objetos.
- c) trituração dos objetos.
- d) hidrólise dos objetos.
- e) fusão dos objetos.
A (ENEM 2012) A própolis é um produto natural conhecido por suas propriedades anti-inflamatórias e cicatrizantes. Esse material contém mais de 200 compostos identificados até o momento. Dentre eles, alguns são de estrutura simples, como é o caso do C6H5CO2CH2CH3, cuja estrutura está mostrada a seguir.
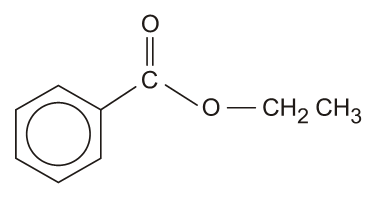 O ácido carboxílico e o álcool capazes de produzir o éster em apreço por meio da reação de esterificação são, respectivamente,
O ácido carboxílico e o álcool capazes de produzir o éster em apreço por meio da reação de esterificação são, respectivamente,
- a) ácido benzoico e etanol.
- b) ácido propanoico e hexanol.
- c) ácido fenilacético e metanol.
- d) ácido propiônico e cicloexanol.
- e) ácido acético e álcool benzílico.
D (ENEM 2012) Em uma planície, ocorreu um acidente ambiental em decorrência do derramamento de grande quantidade de um hidrocarboneto que se apresenta na forma pastosa à temperatura ambiente. Um químico ambiental utilizou uma quantidade apropriada de uma solução de para-dodecil-benzenossulfonato de sódio, um agente tensoativo sintético, para diminuir os impactos desse acidente.
Essa intervenção produz resultados positivos para o ambiente porque
- a) promove uma reação de substituição no hidrocarboneto, tornando-o menos letal ao ambiente.
- b) a hidrólise do para-dodecil-benzenossulfonato de sódio produz energia térmica suficiente para vaporizar o hidrocarboneto.
- c) a mistura desses reagentes provoca a combustão do hidrocarboneto, o que diminui a quantidade dessa substância na natureza.
- d) a solução de para-dodecil-benzenossulfonato possibilita a solubilização do hidrocarboneto.
- e) o reagente adicionado provoca uma solidificação do hidrocarboneto, o que facilita sua retirada do ambiente.
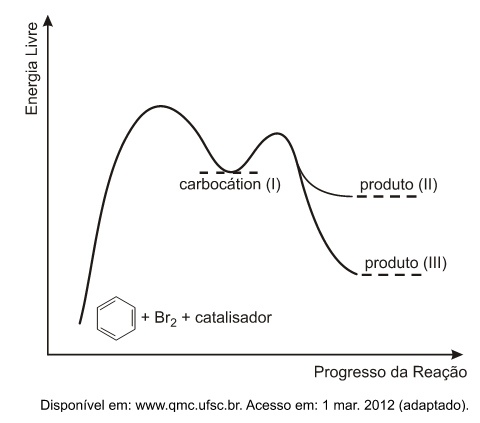
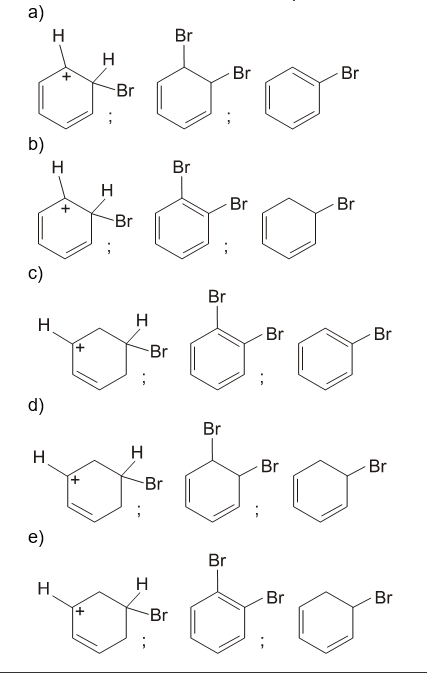
A (ENEM 2012) O benzeno é um hidrocarboneto aromático presente no petróleo, no carvão e em condensados de gás natural. Seus metabólitos são altamente tóxicos e se depositam na medula óssea e nos tecidos gordurosos. O limite de exposição pode causar anemia, câncer (leucemia) e distúrbios do comportamento. Em termos de reatividade química, quando um eletrófilo se liga ao benzeno, ocorre a formação de um intermediário, o carbocátion. Por fim, ocorre a adição ou substituição eletrofílica.
Disponível em: www.sindipetro.org.br. Acesso em: 1 mar. 2012 (adaptado).
Com base no texto e no gráfico do progresso da reação apresentada, as estruturas químicas encontradas em I, II e III são, respectivamente:
A (ENEM 2012) Há milhares de anos o homem faz uso da biotecnologia para a produção de alimentos como pães, cervejas e vinhos. Na fabricação de pães, por exemplo, são usados fungos unicelulares, chamados de leveduras, que são comercializados como fermento biológico. Eles são usados para promover o crescimento da massa, deixando-a leve e macia.
O crescimento da massa do pão pelo processo citado é resultante da
- a) liberação de gás carbônico.
- b) formação de ácido lático.
- c) formação de água.
- d) produção de ATP.
- e) liberação de calor.
D (ENEM 2011) Para evitar o desmatamento da Mata Atlântica nos arredores da cidade de Amargosa, no Recôncavo da Bahia, o Ibama tem atuado no sentido de fiscalizar, entre outras, as pequenas propriedades rurais que dependem da lenha proveniente das matas para a produção da farinha de mandioca, produto típico da região. Com isso, pequenos produtores procuram alternativas como o gás de cozinha, o que encarece a farinha. Uma alternativa viável, em curto prazo, para os produtores de farinha em Amargosa, que não cause danos à Mata Atlântica nem encareça o produto é a
- a) construção, nas pequenas propriedades, de grandes fornos elétricos para torrar a mandioca.
- b) plantação, em suas propriedades, de árvores para serem utilizadas na produção de lenha.
- c) permissão, por parte do Ibama, da exploração da Mata Atlântica apenas pelos pequenos produtores.
- d) construção de biodigestores, para a produção de gás combustível a partir de resíduos orgânicos da região.
- e) coleta de carvão de regiões mais distantes, onde existe menor intensidade de fiscalização do Ibama.
CAIU NO VESTIBULAR!
2019
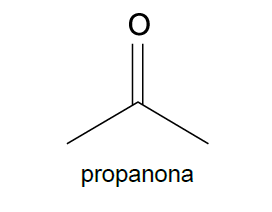
E (FCMSCSP 2019) A propanona é um solvente muito empregado na indústriaquímica e é o principal componente do removedor de esmalte
de unhas. A combustão completa de 1 mol desta substância libera 604 kJ de energia por mol de CO2 produzido.
Na combustão completa de 1 mol de propanona, a energia liberada para cada mol de O2 consumido é
- a) 220 kJ.
- b) 805 kJ.
- c) 906 kJ.
- d) 403 kJ.
- e) 453 kJ.
2018
E (FMABC 2018) Nem mesmo as profundezas dos oceanos, consideradas as áreas mais intocadas do planeta, estão livres da influência humana. Amostras de anfípodas, crustáceos semelhantes aos camarões, coletadas a profundidades que variavam de 7 mil a 10 mil metros em duas áreas do Oceano Pacífico, revelaram níveis elevados de dois produtos químicos: os bifenilpoliclorados, usados por décadas em fluidos de refrigeração; e os bifenilpolibromados, empregados como retardadores da propagação de chamas em tintas, tecidos e materiais da indústria automobilística e aeronáutica.
(Adaptado de: Revista Pesquisa Fapesp, março de 2017)
A estrutura do tetrabromobisfenol A, um exemplo de bifenilpolibromado, está representada a seguir.
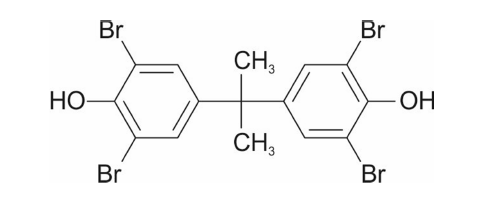 A reação típica para a formação do tetrabromobisfenol A, partindo do bisfenol A, é de
A reação típica para a formação do tetrabromobisfenol A, partindo do bisfenol A, é de
- a) condensação.
- b) hidrólise.
- c) esterificação.
- d) adição.
- e) substituição.
E (FUVEST 2018) Uma das substâncias utilizadas em desinfetantes comerciais é o perácido de fórmula CH3CO3H. A formulação de um dado desinfetante encontrado no comércio consiste em uma solução aquosa na qual existem espécies químicas em equilíbrio, como representado a seguir. (Nessa representação, a fórmula do composto 1 não é apresentada.)
Ao abrir um frasco desse desinfetante comercial, é possível sentir o odor característico de um produto de uso doméstico.
Esse odor é de
- a) amônia, presente em produtos de limpeza, como limpa vidros.
- b) álcool comercial, ou etanol, usado em limpeza doméstica.
- c) acetato de etila, ou etanoato de etila, presente em removedores de esmalte.
- d) cloro, presente em produtos
- e) ácido acético, ou ácido etanoico, presente no vinagre.
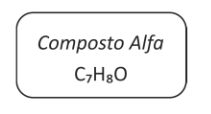
B (FUVEST 2018) Em um laboratório químico, foi encontrado um frasco de vidro contendo um líquido incolor e que apresentava o seguinte rótulo:
Para identificar a substância contida no frasco, foram feitos os seguintes testes:
- Dissolveram se alguns mililitros do líquido do frasco em água, resultando uma solução neutra. A essa solução, adicionaram se uma gota de ácido e uma pequena quantidade de um forte oxidante. Verificou se a formação de um composto branco insolúvel em água fria, mas solúvel em água quente. A solução desse composto em água quente apresentou pH = 4.
- O sólido branco, obtido no teste anterior, foi dissolvido em etanol e a solução foi aquecida na presença de um catalisador. Essa reação produziu benzoato de etila, que é um éster aromático, de fórmula C9H10O2.
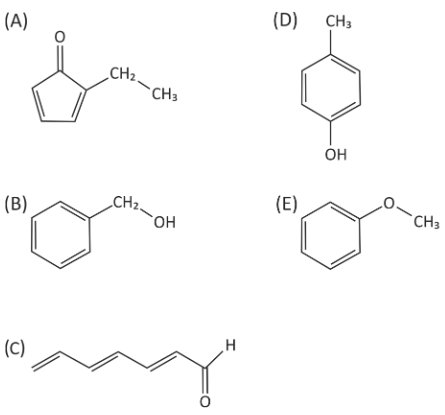
Com base nos resultados desses testes, concluiu se que o Composto Alfa é:
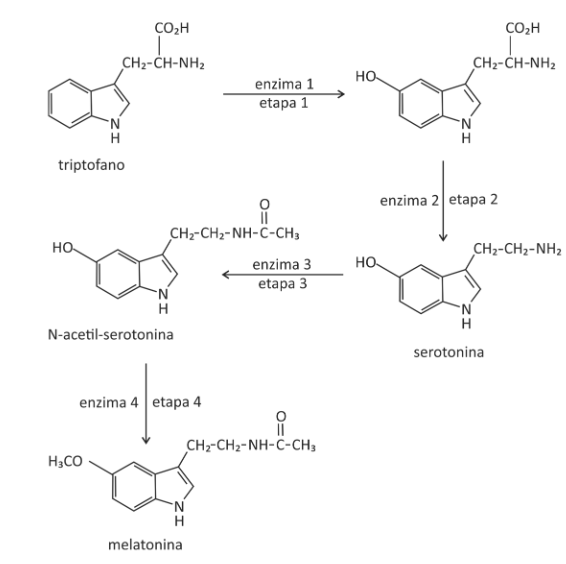
A (FUVEST 2018) O hormônio melatonina é responsável pela sensação de sonolência. Em nosso organismo, a concentração de melatonina começa a aumentar ao anoitecer, atinge o máximo no meio da noite e decresce com a luz do dia. A melatonina é sintetizada a partir do aminoácido triptofano, em quatro etapas catalisadas por diferentes enzimas, sendo que a enzima 3 é degradada em presença de luz.
Considere as seguintes afirmações a respeito desse processo:
- Na etapa 2, há perda de dióxido de carbono e, na etapa 3, a serotonina é transformada em uma amida.
- A manipulação de objetos que emitem luz, como celulares e tablets, pode interromper ou tornar muito lento o processo de transformação da serotonina em N acetil serotonina.
- O aumento da concentração de triptofano na corrente sanguínea pode fazer com que a pessoa adormeça mais lentamente ao anoitecer.
É correto o que se afirma em
- a) I e II, apenas.
- b) I e III, apenas.
- c) II e III, apenas.
- d) III, apenas.
- e) I, II e III.
B (UNICAMP 2018) No Brasil, cerca de 12 milhões de pessoas sofrem de diabetes mellitus, uma doença causada pela incapacidade do corpo em produzir insulina ou em utilizá-la adequadamente. No teste eletrônico para determinar a concentração da glicose sanguínea, a glicose é transformada em ácido glucônico e o hexacianoferrato(III) é transformado em hexacianoferrato(II), conforme mostra o esquema a seguir.
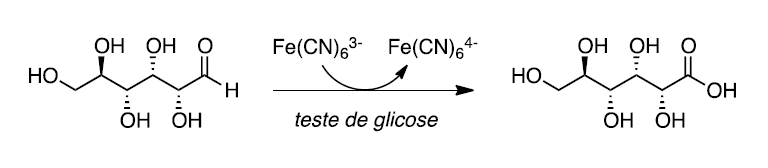
Em relação ao teste eletrônico, é correto afirmar que
- a) a glicose sofre uma reação de redução e o hexacianoferrato(III) sofre uma reação de oxidação.
- b) a glicose sofre uma reação de oxidação e o hexacianoferrato(III) sofre uma reação de redução.
- c) ambos, glicose e hexacianoferrato(III), sofrem reações de oxidação.
- d) ambos, glicose e hexacianoferrato(III), sofrem reações de redução.
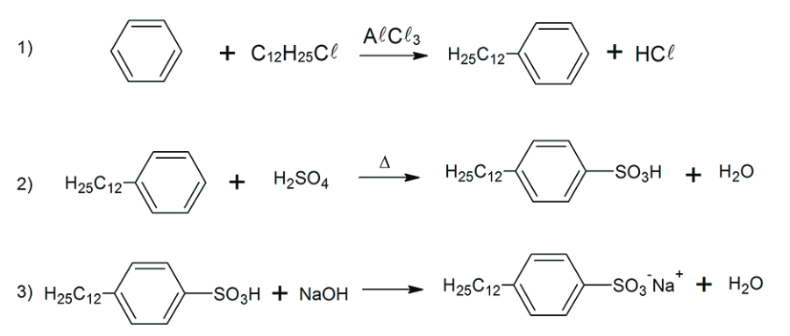
D (MACKENZIE 2018) Os detergentes são substâncias orgânicas sintéticas que possuem como principal característica a capacidade de promover limpeza por meio de sua ação emulsificante, isto é, a capacidade de promover a dissolução de uma substância. Abaixo, estão representadas uma série de equações de reações químicas, envolvidas nas diversas etapas de síntese de um detergente, a partir do benzeno, realizadas em condições ideais de reação.
- A equação 1 representa uma alquilação de Friedel-Crafts.
- A equação 2 é uma reação de substituição, que produz um ácido meta substituído.
- A equação 3 trata-se de uma reação de neutralização com a formação de uma substância orgânica de característica anfipática.
- a) apenas a afirmação I está correta.
- b) apenas a afirmação II está correta.
- c) apenas a afirmação III está correta.
- d) apenas as afirmações I e III estão corretas.
- e) todas as afirmações estão corretas.
B (FCMSCSP 2018) O etanol é uma importante matéria-prima da indústria química. A figura mostra três produtos obtidos a partir do etanol submetido a três diferentes processos com seus reagentes e condições experimentais necessários.
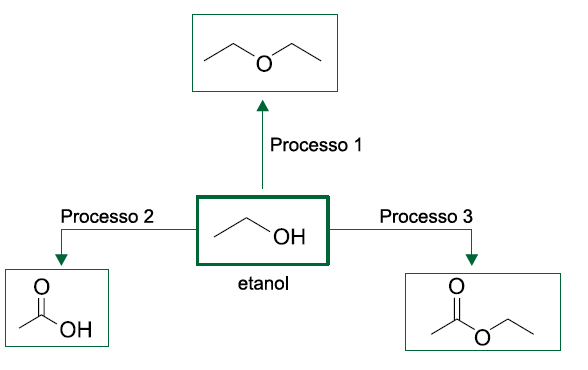
A reação de desidratação intermolecular e a reação de esterificação ocorrem, respectivamente, nos processos
- a) 1 e 2.
- b) 1 e 3.
- c) 2 e 1.
- d) 2 e 3.
- e) 3 e 1.
A (FCMSCSP 2018) A vitamina B6 (fórmula molecular C8H11O3N), conhecida como piridoxina, está presente em alimentos como carne bovina, gema de ovo e leite. A massa de gás carbônico produzida na combustão completa de 0,5 mol de piridoxina é
- a) 176 g.
- b) 220 g.
- c) 264 g.
- d) 308 g.
- e) 440 g.
E (FGV SP 2018) Na equação, representa-se a reação da interação da molécula orgânica, substância I, com o hidrogenocarbonato de sódio em meio aquoso.
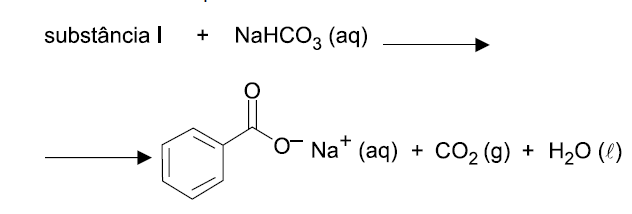 É correto afirmar que a substância I apresenta o grupo funcional característico da função orgânica
É correto afirmar que a substância I apresenta o grupo funcional característico da função orgânica
- a) éter.
- b) éster.
- c) álcool.
- d) aldeído.
- e) ácido carboxílico.
2017
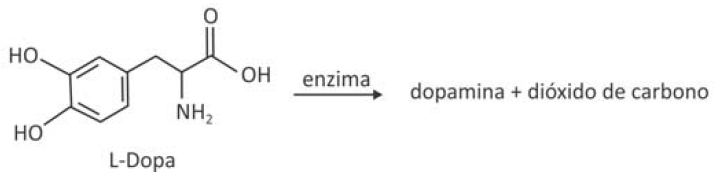
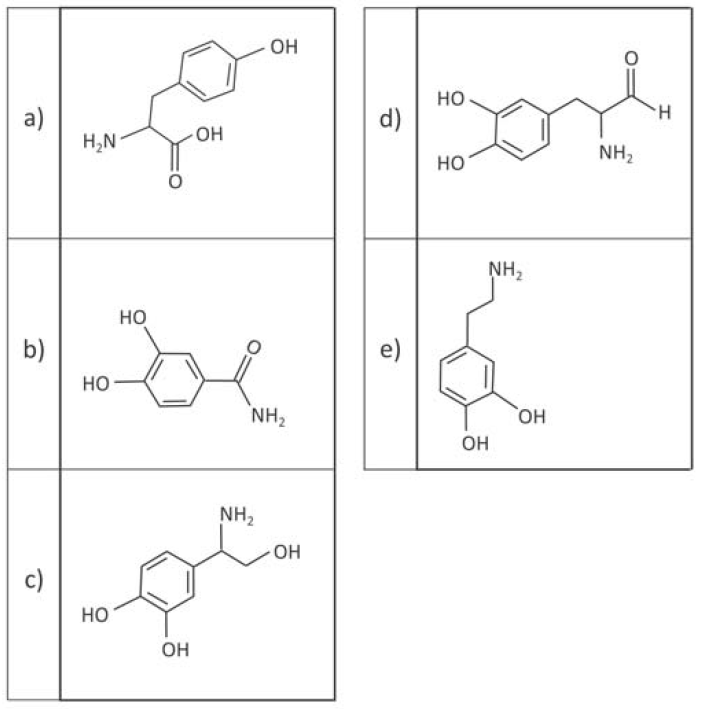
E (FUVEST 2017) A dopamina é um neurotransmissor importante em processos cerebrais. Uma das etapas de sua produção no organismo humano é a descarboxilação enzimática da L-Dopa, como esquematizado:
Sendo assim, a fórmula estrutural da dopamina é:
C (MACKENZIE 2017) A respeito da combustão completa de 1 mol de gás propano, no estado padrão, são feitas as seguintes afirmações:
- Trata-se de um processo endotérmico.
- Ocorre com liberação de energia para o meio externo.
- Há a formação de 3 mols de dióxido de carbono e 4 mols de água.
- São consumidos 5 mols de gás oxigênio.
Analisando-se as afirmações acima, estão corretas somente
- a) I e II.
- b) I, II e III.
- c) II, III e IV.
- d) I, III e IV.
- e) II e IV.
2016
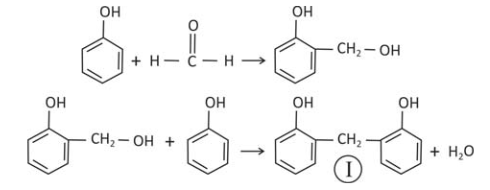
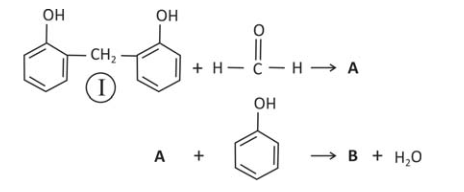
B (FUVEST 2016) Fenol e metanal (aldeído fórmico), em presença de um catalisador, reagem formando um polímero que apresenta alta resistência térmica. No início desse processo, pode-se formar um composto com um grupo —CH2OH ligado no carbono 2 ou no carbono 4 do anel aromático. O esquema a seguir apresenta as duas etapas iniciais do processo de polimerização para a reação no carbono 2 do fenol.
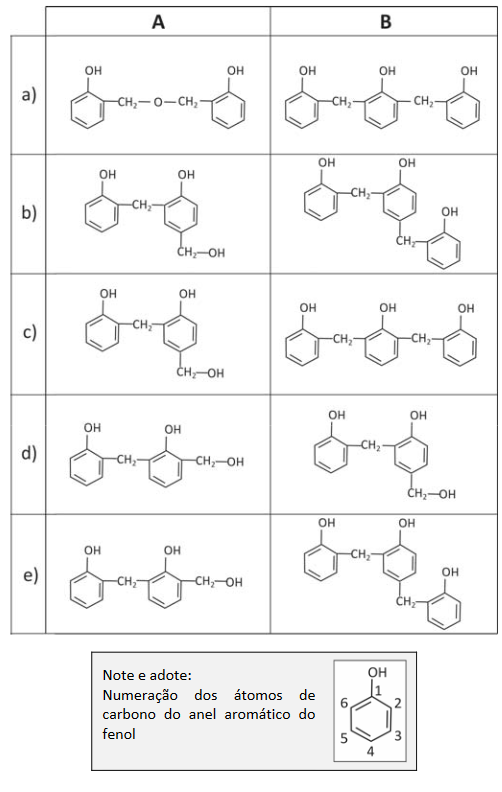
Considere que, na próxima etapa desse processo de polimerização, a reação com o metanal ocorra no átomo de carbono 4 de um dos anéis de I. Assim, no esquema
A e B podem ser, respectivamente,
A (FUVEST 2016) Um aldeído pode ser transformado em um aminoácido pela sequência de reações:
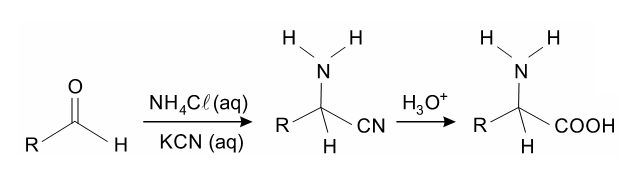 O aminoácido N-metil-fenilalanina pode ser obtido pela mesma sequência reacional, empregando-se, em lugar do cloreto de amônio o reagente
O aminoácido N-metil-fenilalanina pode ser obtido pela mesma sequência reacional, empregando-se, em lugar do cloreto de amônio o reagente
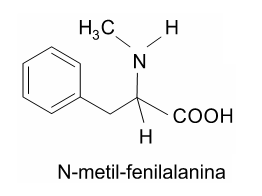 Nessa transformação, o aldeído que deve ser empregado é
Nessa transformação, o aldeído que deve ser empregado é
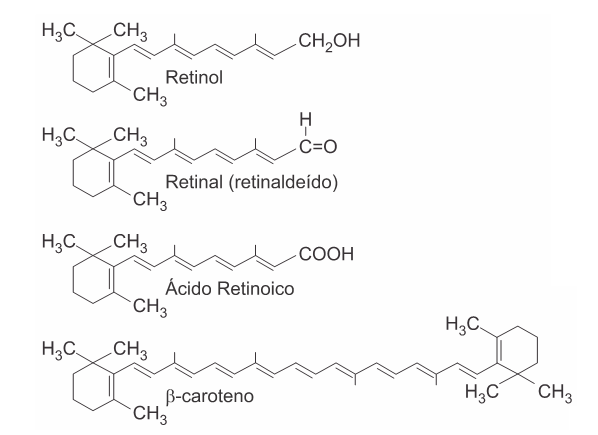
A (PUC SP 2016) O β-caroteno é um corante antioxidante presente em diversos vegetais amarelos ou laranja, como a cenoura, por exemplo. Em nosso organismo, o β-caroteno é um importante precursor do retinal e do retinol (vitamina A), substâncias envolvidas no metabolismo da visão.
Sobre as reações envolvidas no metabolismo do retinol foram feitas as seguintes afirmações:
- β-caroteno retinal e retinol são classificados, respectivamente, como hidrocarboneto, aldeído e álcool.
- O retinol sofre oxidação ao ser transformado em retinal.
- Retinal é um isômero de função do retinol.
- O retinal é reduzido ao se transformar em ácido retinoico.
Estão corretas APENAS as afirmações:
- a) I e II.
- b) II e III.
- c) I e IV.
- d) II e IV.
C (UNISC 2016) A síntese da substância 1 (óleo essencial de banana) é obtida através da reação clássica conhecida com esterificação de Fischer.
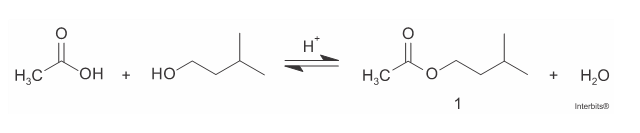 Em relação à reação apresentada, podemos afirmar que
Em relação à reação apresentada, podemos afirmar que
- a) os reagentes empregados são aldeído e éter.
- b) a reação não pode ser conduzida em meio ácido.
- c) o produto orgânico obtido é denominado de etanoato de isoamila.
- d) o álcool é denominado de acordo com a IUPAC, 2-metilbutan-4-ol.
- e) os reagentes empregados são cetona e éster.
C (IMED 2016) Analise a Reação Orgânica abaixo:
- a) Adição.
- b) Ozonólise.
- c) Eliminação.
- d) Substituição.
- e) Desidratação.
C (UPF 2016) Correlacione cada reação indicada na coluna 1 com o produto que deve ser formado nesta, indicado na coluna 2.
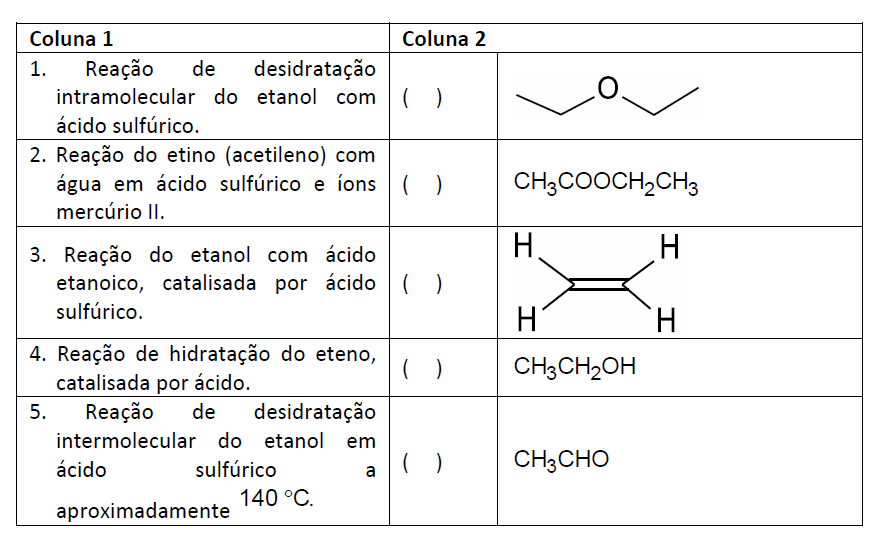 A sequência correta de preenchimento dos parênteses, de cima para baixo, é:
A sequência correta de preenchimento dos parênteses, de cima para baixo, é:
- a) 1 – 4 – 3 – 5 – 2.
- b) 3 – 5 – 1 – 2 – 4.
- c) 5 – 3 – 1 – 4 – 2.
- d) 1 – 4 – 5 – 3 – 2.
- e) 4 – 3 – 5 – 1 – 2.
C (UECE 2016) O cloro ficou muito conhecido devido a sua utilização em uma substância indispensável a nossa sobrevivência: a água potável. A água encontrada em rios não é recomendável para o consumo, sem antes passar por um tratamento prévio. Graças à adição de cloro, é possível eliminar todos os microrganismos patogênicos e tornar a água potável, ou seja, própria para o consumo. Em um laboratório de química, nas condições adequadas, fez-se a adição do gás cloro em um determinado hidrocarboneto, que produziu o 2,3-diclorobutano. Assinale a opção que corresponde à fórmula estrutural desse hidrocarboneto.
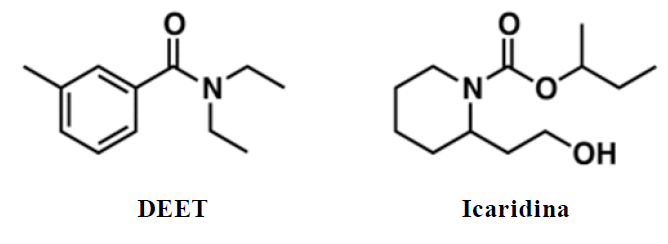
E (MACKENZIE 2016) A epidemia de dengue no Brasil, transmitida pelo mosquito Aedes aegypti e mais recentemente os casos de microcefalia, causado pela disseminação do Zika vírus, vem preocupando a população brasileira e principalmente as gestantes. Na tentativa de evitar o contato com o mosquito, os repelentes desapareceram das prateleiras das farmácias, mas a eficácia não está no uso de um repelente qualquer. Os médicos alertam que o repelente eficaz contra o Aedes aegypti deve conter um princípio ativo chamado icaridina. A Organização Mundial de Saúde (OMS) acrescenta também outros princípios ativos eficazes, o DEET e IR3535. Assim, de acordo com as fórmulas estruturais do DEET e da icaridina, abaixo representadas, são feitas as seguintes afirmações:
I. O DEET possui três carbonos terciários e um grupo funcional amida.
II. A fórmula molecular da icaridina é C12H22NO3.
III. A molécula de icaridina possui enantiômeros.
IV. A hidrólise ácida do DEET forma um ácido carboxílico e uma amina secundária.
É correto dizer que apenas as afirmações
- a) II, III e IV são verdadeiras.
- b) I e II são verdadeiras.
- c) I, II e III são verdadeiras.
- d) II e IV são verdadeiras.
- e) III e IV são verdadeiras.
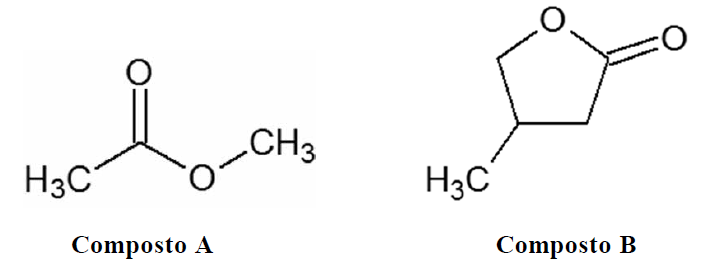
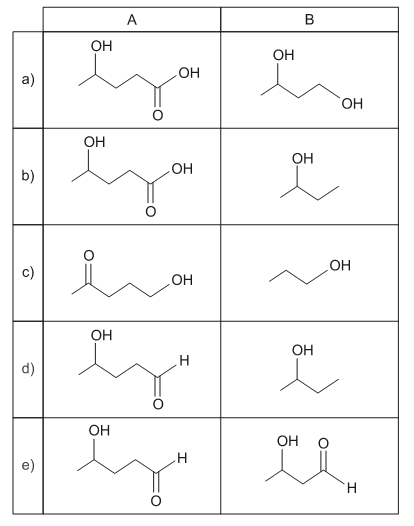
D (MACKENZIE 2016) Abaixo estão representadas as fórmulas estruturais dos compostos A e B, obtidos por meio de duas sínteses orgânicas distintas e em condições adequadas.
Assim, a alternativa que traz, respectivamente, considerando as condições adequadas para tal, os reagentes orgânicos utilizados na obtenção dos compostos A e B é
- a) A: etanol e ácido acético; B: ácido butanoico e etanol.
- b) A: ácido metanoico e etanol; B: isopropano e ácido acético.
- c) A: metanol e ácido etanoico; B: ácido butanoico e etanol.
- d) A: ácido acético e metanol; B: ácido 4-hidroxi-3-metilbutanoico.
- e) A: etanol e metanol; B: ácido 4-hidroxi-3-metilbutanoico.
E (FGV SP 2016) O hidrogênio para células a combustível de uso automotivo poderá ser obtido futuramente a partir da reação de reforma do etanol. Atualmente, nessa reação, são gerados subprodutos indesejados: etanal (I) e etanoato de etila (II). Porém, pesquisadores da UNESP de Araraquara verificaram que, com o uso de um catalisador adequado, a produção de hidrogênio
do etanol poderá ser viabilizada sem subprodutos.
(Revista Pesquisa Fapesp, 234, agosto de 2015. Adaptado)
A reação da transformação de etanol no subproduto I e a substância que reage com o etanol para formação do subproduto II são, correta e respectivamente,
- a) substituição e etanal.
- b) redução e etanal.
- c) redução e ácido acético.
- d) oxidação e etanal.
- e) oxidação e ácido acético.
2015
B (UEPA 2015) Analise as reações e seus produtos orgânicos abaixo, para responder à questão.
Quanto à classificação das reações acima, é correto afirmar que as mesmas são, respectivamente:
- a) reação de substituição, reação de adição e reação de oxidação.
- b) reação de hidrogenação, reação de alquilação e reação de oxidação.
- c) reação de substituição, reação de eliminação e reação de oxidação.
- d) reação de hidrogenação, reação de alquilação e reação de combustão.
- e) reação de hidrogenação, reação de alquilação e reação de eliminação.
B (UERN 2015) A reação de substituição entre o gás cloro e o propano, em presença de luz ultravioleta, resulta como produto principal, o composto:
- a) 1-cloropropeno.
- b) 2-cloropropano.
- c) 1-cloropropano.
- d) 2-cloropropeno.
D (FUVEST 2015) O 1,4-pentanodiol pode sofrer reação de oxidação em condições controladas, com formação de um aldeído A, mantendo o número de átomos de carbono da cadeia. O composto A formado pode, em certas condições, sofrer reação de descarbonilação, isto é, cada uma de suas moléculas perde CO, formando o composto B. O esquema a seguir representa essa sequência de reações:
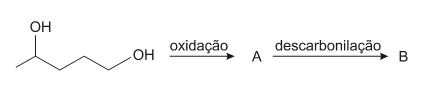 Os produtos A e B dessas reações são:
Os produtos A e B dessas reações são:
A (FUVEST 2015) Parte do solo da bacia amazônica é naturalmente pobre em nutrientes e, consequentemente, pouco apropriada para a agricultura comercial. Por outro lado, em certas porções desse território, são encontradas extensões de terra rica em carvão e nutrientes (sob a forma de compostos de fósforo e cálcio), os quais não resultaram da decomposição microbiana da vegetação. Esse tipo de solo é popularmente chamado de “terra preta”.
Dentre as hipóteses a seguir, formuladas para explicar a ocorrência da “terra preta”, a mais plausível seria a da
- a) decomposição gradativa de restos de peixes e caça e deposição da fuligem gerada pela queima de madeira, empregada no cozimento de alimentos.
- b) decomposição microbiana de afloramentos de petróleo, seguida pela combustão completa dos produtos dessa decomposição.
- c) reação dos carbonatos e fosfatos, existentes na vegetação morta, com chuvas que apresentam pH menor do que 4 (chuva ácida).
- d) oxidação, durante a respiração noturna, do carbono contido nos vegetais da floresta amazônica.
- e) decomposição térmica de calcário, produzindo óxido de cálcio e carvão.
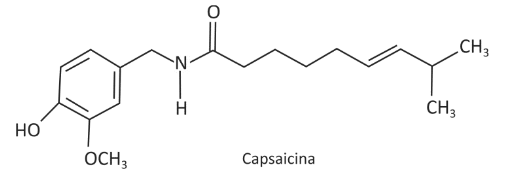
A (FUVEST 2015) A ardência provocada pela pimenta dedo-de-moça é resultado da interação da substância capsaicina com receptores localizados na língua, desencadeando impulsos nervosos que se propagam até o cérebro, o qual interpreta esses impulsos na forma de sensação de ardência. Esse tipo de pimenta tem, entre outros efeitos, o de estimular a sudorese no organismo humano.
Considere as seguintes afirmações:
- Nas sinapses, a propagação dos impulsos nervosos, desencadeados pelo consumo dessa pimenta, se dá pela ação de neurotransmissores.
- Ao consumir essa pimenta, uma pessoa pode sentir mais calor pois, para evaporar, o suor libera calor para o corpo.
- A hidrólise ácida da ligação amídica da capsaicina produz um aminoácido que é transportado até o cérebro, provocando a sensação de ardência.
É correto apenas o que se afirma em
- a) I.
- b) II.
- c) I e II.
- d) II e III.
- e) I e III.
2014
C (FUVEST 2014 – INTERDISCIPLINAR) Uma jovem estudante quis demonstrar para sua mãe o que é uma reação química. Para tanto, preparou, em cinco copos, as seguintes soluções:
 Em seguida, começou a fazer misturas aleatórias de amostras das soluções contidas nos copos, juntando duas amostras diferentes a cada vez. Qual é a probabilidade de que ocorra uma reação química ao misturar amostras dos conteúdos de dois dos cinco copos?
Em seguida, começou a fazer misturas aleatórias de amostras das soluções contidas nos copos, juntando duas amostras diferentes a cada vez. Qual é a probabilidade de que ocorra uma reação química ao misturar amostras dos conteúdos de dois dos cinco copos?- a) 1/10
- b) 1/8
- c) 1/5
- d) 1/3
- e) 1/2
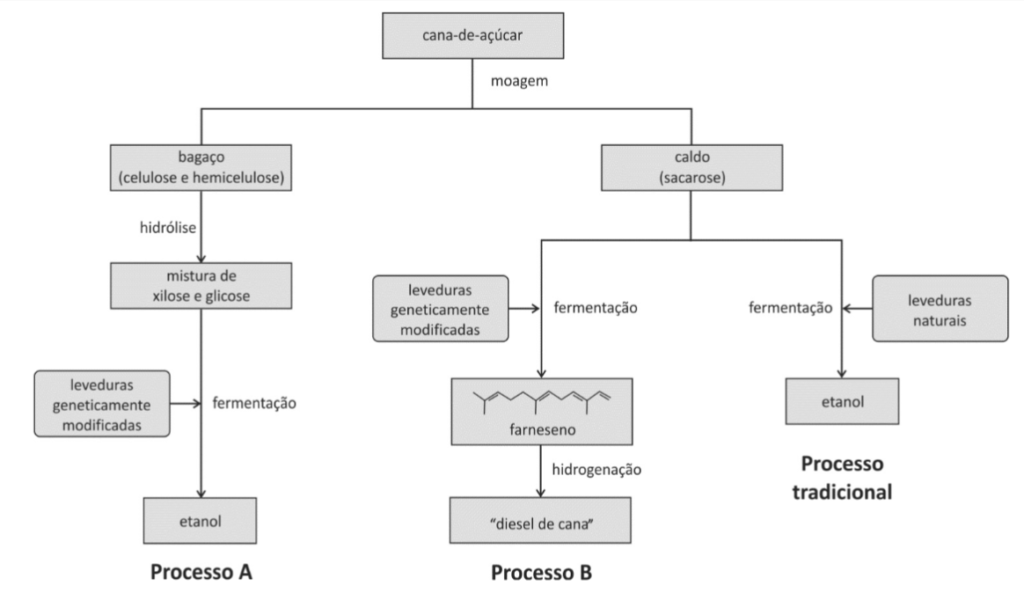
B (FUVEST 2014) No processo tradicional, o etanol é produzido a partir do caldo da cana-de-açúcar por fermentação promovida por leveduras naturais, e o bagaço de cana é desprezado. Atualmente, leveduras geneticamente modificadas podem ser utilizadas em novos processos de fermentação para a produção de biocombustíveis. Por exemplo, no processo A, o bagaço de cana, após hidrólise da celulose e da hemicelulose, também pode ser transformado em etanol. No processo B, o caldo de cana, rico em sacarose, é transformado em farneseno que, após hidrogenação das ligações duplas, se transforma no“diesel de cana”. Esses três processos de produção de biocombustíveis podem ser representados por:
- a) No Processo A, a sacarose é transformada em celulose por micro-organismos transgênicos.
- b) O Processo A, usado em conjunto com o processo tradicional, permite maior produção de etanol por hectare cultivado.
- c) O produto da hidrogenação do farneseno não deveria ser chamado de“diesel”, pois não é um hidrocarboneto.
- d) A combustão do etanol produzido por micro-organismos transgênicos não é poluente, pois não produz dióxido de carbono.
- e) O Processo B é vantajoso em relação ao Processo A, pois a sacarose é matéria-prima com menor valor econômico do que o bagaço de cana.
2013
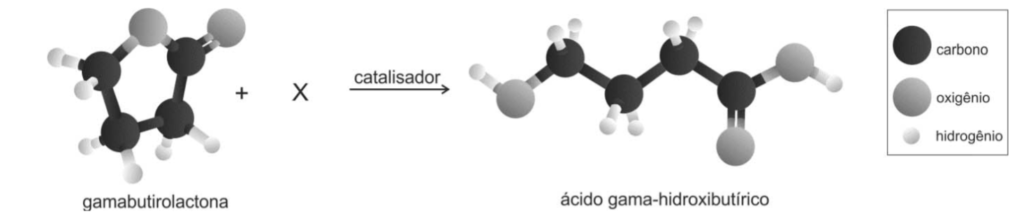
C (FUVEST 2013) O ácido gama-hidroxibutírico é utilizado no tratamento do alcoolismo. Esse ácido pode ser obtido a partir da gamabutirolactona, conforme a representação a seguir:
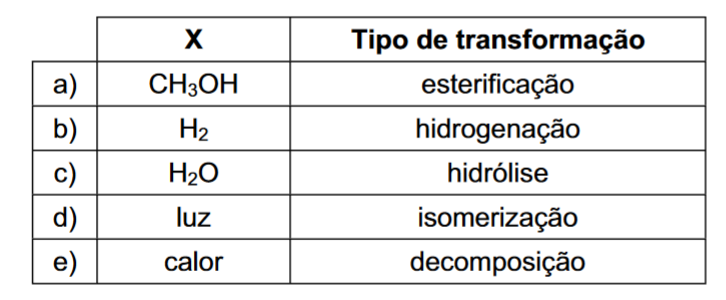
Assinale a alternativa que identifica corretamente X (de modo que a representação respeite a conservação da matéria) e o tipo de transformação que ocorre quando a gamabutirolactona é convertida no ácido gamahidroxibutírico.
2010
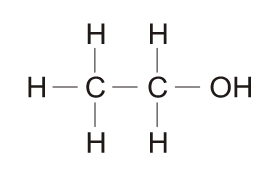
B (UFF 2010) O álcool etílico pode ser encontrado tanto em bebidas alcoólicas quanto em produtos de uso doméstico e tem a seguinte estrutura química:
A diferença entre esses produtos comerciais está na concentração do etanol. Enquanto uma latinha de cerveja possui cerca de 6% do álcool, um litro do produto doméstico possui cerca de 96%, ou seja, uma concentração muito maior. Caso a energia acumulada, pelo consumo exagerado de algumas bebidas alcoólicas, não seja gasta, pode resultar, então, na famosa “barriga de cerveja”. O álcool altera o funcionamento normal do metabolismo.
Em relação aos alcoóis, é correto afirmar que:
- a) o etanol é menos ácido do que o propano.
- b) uma reação do 2-propanol com ácido sulfúrico e aquecimento pode levar a uma reação de eliminação (desidratação).
- c) a oxidação do etanol na presença de ar atmosférico e sob ação de catalisador produz propanona e água.
- d) o 2-propanol tem ponto de ebulição menor do que o etanol.
- e) o éter etílico não pode ser obtido a partir do etanol.
EXERCÍCIOS EXTRAS
(CSA 2013 – BIA – U2b) A oxidação enérgica de um alcadieno liberou gás carbônico e originou acetona e ácido propanodióico. Deduza a estrutura e o nome desse alcadieno.
(CSA 2013 – BIA – U6) Equacione as reações:
– desidratação intramolecular do butan-2-ol
– hidratação do acetileno
– nitração do benzaldeído
– oxidação branda do but-2-eno
A (CSA 2013 – BIA – U11) (UFRGS) Na obtenção do álcool etílico a partir da cana-de-açúcar, beterraba, frutas ou cereais, uma das etapas consiste na:
- a) fermentação de glicídios.
- b) oxidação de lipídios.
- c) condensação de aminoácidos.
- d) condensação de glicídios.
- e) fermentação de lipídios.
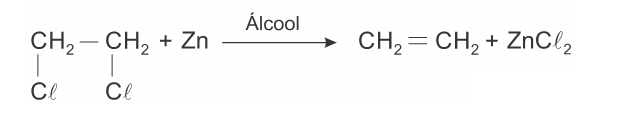
C (CSA 2013 – BIA – U15) (UNIFOR) A reação de Wurtz pode ser genericamente representada pela equação:
![]() Por esse processo o cloroetano produz:
Por esse processo o cloroetano produz:
- a) etano
- b) propano
- c) butano
- d) pentano
- e) hexano
A (CSA 2013 – BIA – U17) A fermentação da glicose (C6H12O6) origina etanol e gás carbônico. A massa de álcool que pode ser obtida a partir de 36 g de glicose corresponde a:
(Dados: massas atômicas: H = 1; C = 12; O = 16)
- a) 18,4 g
- b) 9,2 g
- c) 46,0 g
- d) 36,8 g
- e) 92,0 g
B (CSA 3 – 2012 – BIA – S16) No organismo humano, a vitamina A (retinol), é transformado numa substância que é a responsável pela visão:
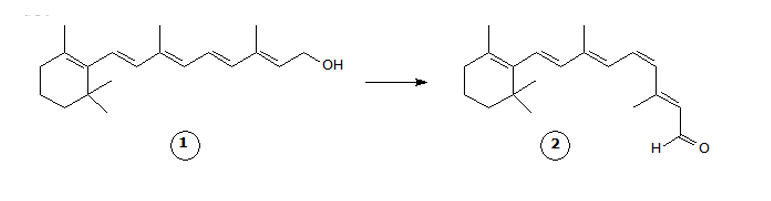 Na transformação do retinol (estrutura 1) em 2, ocorrem reações
Na transformação do retinol (estrutura 1) em 2, ocorrem reações
- a) de isomerização e redução.
- b) de isomerização e oxidação.
- c) de redução e esterificação.
- d) de redução e oxidação.
- e) de eliminação e hidratação.
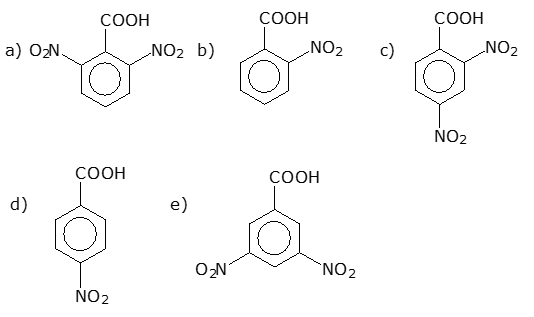
E (CSA 3 – 2012 – BIA – S19) (UFPB) Na reação de um mol de ácido benzóico com dois mols de ácido nítrico, na presença de ácido sulfúrico, forma-se
D (CSA 3 – 2012 – BIA – S20) (CESGRANRIO) A hidratação do propino, catalisada por ácido, produz principalmente:
- a) propan-1-ol
- b) propan-2-ol
- c) propan-1-al
- d) propan-2-ona
- e) ácido propanóico
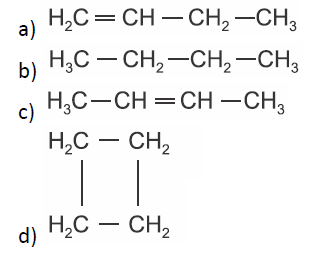
C (CSA 3 – 2012 – BIA – S21) (UFLA) Na reação de desidroalogenação
B (CSA 3 – 2012 – BIA – S24) (FUVEST) Os poliésteres são polímeros fabricados por condensação de dois monômeros diferentes, em sucessivas reações de esterificação. Dentre os pares de monômeros abaixo,
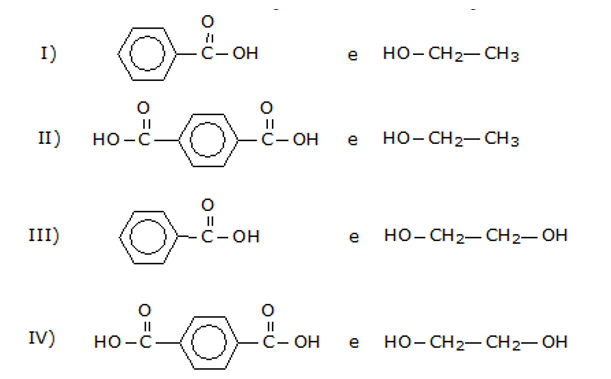 poliésteres podem ser formados
poliésteres podem ser formados
- a) por todos os pares.
- b) apenas pelo par IV
- c) apenas pelos pares II e III.
- d) apenas pelos pares I e IV.
- e) apenas pelos pares II, III e IV.
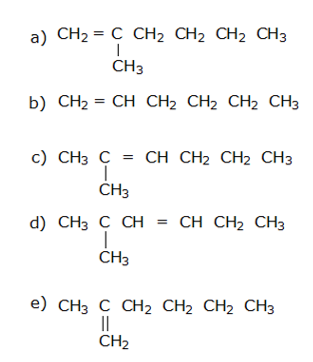
B (CSA 3 – 2012 – BIA – S25) (UNESP) O “éter sulfúrico” é obtido industrialmente pela desidratação do etanol, em presença de H2SO4. A mesma reação, ocorrendo em temperaturas mais elevadas, produz o alceno correspondente. O éter e o alceno têm, respectivamente, as fórmulas:
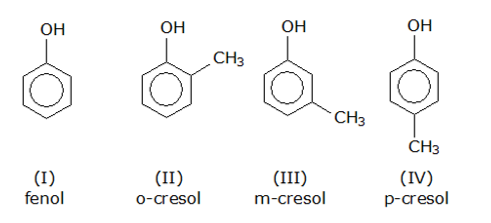
E (CSA 3 – 2012 – BIA – S26) (UFF) Os fenóis são compostos orgânicos oxigenados. Muitos são utilizados como desinfetantes para uso doméstico e alguns são os principais constituintes do carvão mineral. Indica-se, a seguir, as estruturas de componentes do carvão mineral, alguns dos quais estão presentes no desinfetante conhecido por “creolina”.
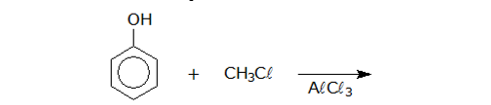 Nesta reação, os produtos principais são os que apresentam suas estruturas indicadas por:
Nesta reação, os produtos principais são os que apresentam suas estruturas indicadas por:
- a) I e II
- b) I e IV
- c) II e III
- d) III e IV
- e) II e IV
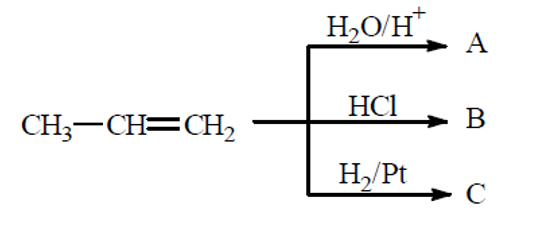
E (CSA 2011 – BIB – U7) (FURG 2007) Observe o esquema reacional abaixo:
Sobre estes compostos, é correto afirmar que todas as reações são de:
- a) adição, sendo os produtos respectivamente: A = 1-propanol; B = 1-cloro-propano e C = propano.
- b) substituição, sendo os produtos respectivamente: A = 1-butanol; B = 2-cloropropano e C = propano.
- c) substituição, sendo os produtos respectivamente: A = 1-hidróxi-2-propeno; B = 2-cloro-1-propeno e C = propeno.
- d) adição, sendo os produtos respectivamente: A = 1,2-propanodiol; B = 1,2-dicloro-propano e C = propano.
- e) adição, sendo os produtos respectivamente: A = 2-propanol; B = 2-cloro-propano e C = propano.
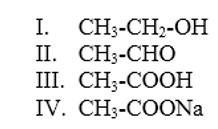
C (CSA 2011 – BIB – U9) Dados os compostos abaixo, assinale a alternativa incorreta.
- a) Os nomes dos compostos I, II, III e IV são, respectivamente, etanol, etanal, ácido etanoico e etanoato de sódio.
- b) A oxidação do composto I leva ao composto II, e a oxidação do composto II leva ao composto III.
- c) O etanol pode ser reduzido a ácido acético e esse procedimento é utilizado na produção do vinagre.
- d) O composto IV pode ser obtido por meio da reação do composto III com NaOH.
- e) O Composto I só possui ligações simples e os demais possuem uma ligação dupla cada.