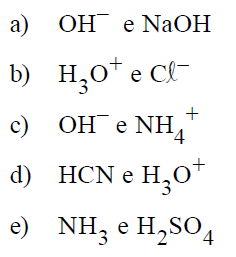QUÍMICA – LISTA DE EXERCÍCIOS SOBRE REAÇÕES ÁCIDO-BASE
(ÁCIDOS E BASES DE ARHENIUS, BROWNSTED-LOWRY E LEWIS)
CAIU NO ENEM!
CAIU NO VESTIBULAR!
2017
A (FGV SP 2017) A teoria ácido-base de Brönsted-Lowry tem grande importância e aplicação na química, pois ela pode ser útil para elucidar mecanismos de reações e, portanto, otimizar suas condições para aplicações em processos industriais.
Considere as reações:
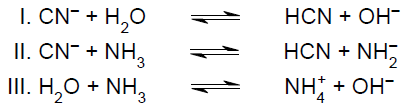 De acordo com essa teoria ácido-base, o cianeto, em I e II, e a amônia, em II e III, são classificados, respectiva e corretamente, como:
De acordo com essa teoria ácido-base, o cianeto, em I e II, e a amônia, em II e III, são classificados, respectiva e corretamente, como:
- a) base, base, ácido, base.
- b) base, base, base, ácido.
- c) base, ácido, base, ácido.
- d) ácido, ácido, base, ácido.
- e) ácido, base, ácido, base.
2016
B (MACKENZIE 2016) Em 1920, o cientista dinamarquês Johannes N. Brönsted e o inglês Thomas M. Lowry propuseram, independentemente, uma nova definição de ácido e base diferente do conceito até então utilizado de Arrhenius. Segundo esses cientistas, ácido é uma espécie química (molécula ou íon) capaz de doar próton (H+) em uma reação. Já, a base é uma espécie química (molécula ou íon) capaz de receber próton (H+) em uma reação. Abaixo está representada uma reação com a presença de ácidos e bases de acordo com a teoria ácido-base de Brönsted-Lowry.
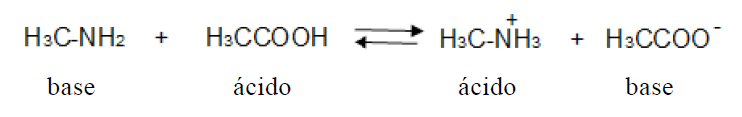 De acordo com essas informações, assinale a alternativa que possui, respectivamente, um ácido e uma base de Brönsted-Lowry.
De acordo com essas informações, assinale a alternativa que possui, respectivamente, um ácido e uma base de Brönsted-Lowry.
2015
E (UFJF – PISM 1 2015) De acordo com as teorias de Arrhenius, Brönsted-Lowry e Lewis, diferentes substâncias podem ser reconhecidas como ácidos ou bases. Assinale a alternativa que apresenta substâncias classificadas como ácidos de acordo com as teorias de Arrhenius, Brönsted-Lowry e Lewis, respectivamente.
- a) HCl, H2SO4, NH3
- b) NH3, HCl, HCN
- c) H2SO4, CN–, NH4+
- d) NaOH, CH3COO–, SO42–
- e) H2SO4, HCl, NH4+
2014
B (UFJF – PISM 1 2014) Solos ácidos são, de um modo geral, impróprios para o cultivo de vegetais. É possível corrigir a acidez pela adição de calcário (CaCO3). A reação que ocorre para essa correção é apresentada abaixo.
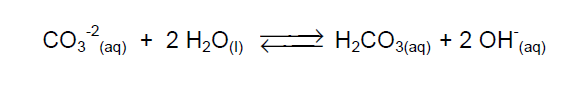 Com base nessas informações, assinale a alternativa que apresenta a afirmação INCORRETA.
Com base nessas informações, assinale a alternativa que apresenta a afirmação INCORRETA.
- a) Nesse processo, o carbonato atua como uma base de Bronsted.
- b) Uma solução de carbonato muda o papel de tornassol azul para rosa.
- c) Algumas gotas de fenolftaleína tornam essa solução rosa.
- d) A água, nesse processo, atua com um ácido de Bronsted.
- e) O carbonato de cálcio é um sal.
2013
B (UFJF – PISM 1 2013) Considerando a teoria ácido-base de Brönsted-Lowry, sabe-se que um par conjugado ácido-base é aquele par formado por espécies químicas que diferem entre si por um íon H+. Observando as reações abaixo, avalie as afirmações de I a IV.
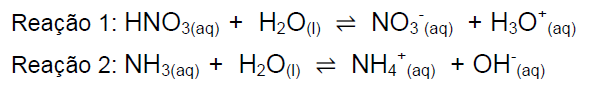 I) Na reação 1, a água atua como uma base de Brönsted-Lowry, enquanto que na reação 2 a água atua como um ácido de Brönsted-Lowry.
I) Na reação 1, a água atua como uma base de Brönsted-Lowry, enquanto que na reação 2 a água atua como um ácido de Brönsted-Lowry.
II) NH3 é uma base de Brönsted-Lowry.
III) NH3 e NH4+ formam um par conjugado.
IV) O íon NO3– é uma base de Brönsted-Lowry e forma um par conjugado com o HNO3.
Marque a alternativa CORRETA.
- a) Nenhuma afirmação está correta.
- b) Todas as afirmações estão corretas.
- c) As afirmações I e III estão corretas.
- d) As afirmações I, II e III estão corretas.
- e) As afirmações II, III e IV estão corretas.