CAIU NO ENEM!
CAIU NO VESTIBULAR!
2018
E (UFPR 2018) Em Termodinâmica, estudamos processos importantes que fazem parte de ciclos utilizados em máquinas térmicas, alguns dos quais de grande relevância tecnológica, além de científica. Com relação ao que ocorre com um gás ideal, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) Em todo processo isovolumétrico, também chamado de isocórico, o trabalho realizado pelo gás é nulo.
( ) Em todo processo adiabático, a energia interna do gás é constante.
( ) Em todo processo isobárico, não há trocas de calor entre o gás e o meio externo.
( ) Em todo processo isotérmico, a temperatura do gás aumenta quando há realização de trabalho sobre ele.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
- a) V – V – V – V.
- b) F – V – F – F.
- c) F – V – F – V.
- d) F – F – V – F.
- e) V – F – F – F.
2017
B (UFRGS 2017) Observe a figura abaixo.
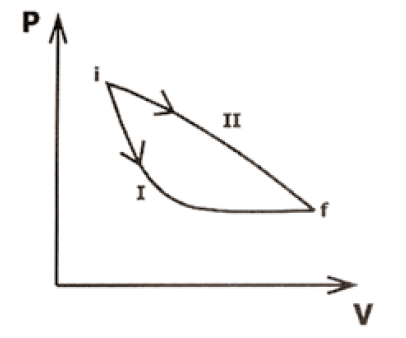
A figura mostra dois processos, I e II, em um diagrama pressão (P) x volume (V) ao longo dos quais um gás ideal pode ser levado do estado inicial i para o estado final f. Assinale a alternativa que preenche corretamente as lacunas do enunciado abaixo, na ordem em que aparecem.
De acordo com a 1ª Lei da Termodinâmica, a variação da energia interna é …….. nos dois processos. O trabalho WI realizado no processo I é …….. que o trabalho WII realizado no processo II.
- a) igual — maior
- b) igual — menor
- c) igual — igual
- d) diferente — maior
- e) diferente — menor
E (UDESC 2017) Considere as afirmações com relação à Termodinâmica.
I. A energia interna de uma dada quantidade de gás ideal depende apenas da temperatura.
II. Quando um sistema pode ir do estado (1) para o estado (2) por vários processos diferentes, a quantidade de calor absorvida pelo sistema será a mesma para todos os processos.
III. Quando um sistema pode ir do estado (1) para o estado (2) por vários processos diferentes, a variação da entropia do sistema será a mesma para todos os processos.
IV. Quando um sistema pode ir do estado (1) para o estado (2) por vários processos diferentes, a variação da energia interna do sistema será a mesma para todos os processos.
V. Quando um sistema pode ir do estado (1) para o estado (2) por vários processos diferentes, a quantidade de trabalho realizado sobre o sistema será a mesma para todos os processos.
Assinale a alternativa correta.
- a) Somente as afirmativas I, II e IV são verdadeiras.
- b) Somente as afirmativas III e V são verdadeiras.
- c) Somente as afirmativas II e V são verdadeiras.
- d) Somente as afirmativas I, III e V são verdadeiras.
- e) Somente as afirmativas I, III e IV são verdadeiras.
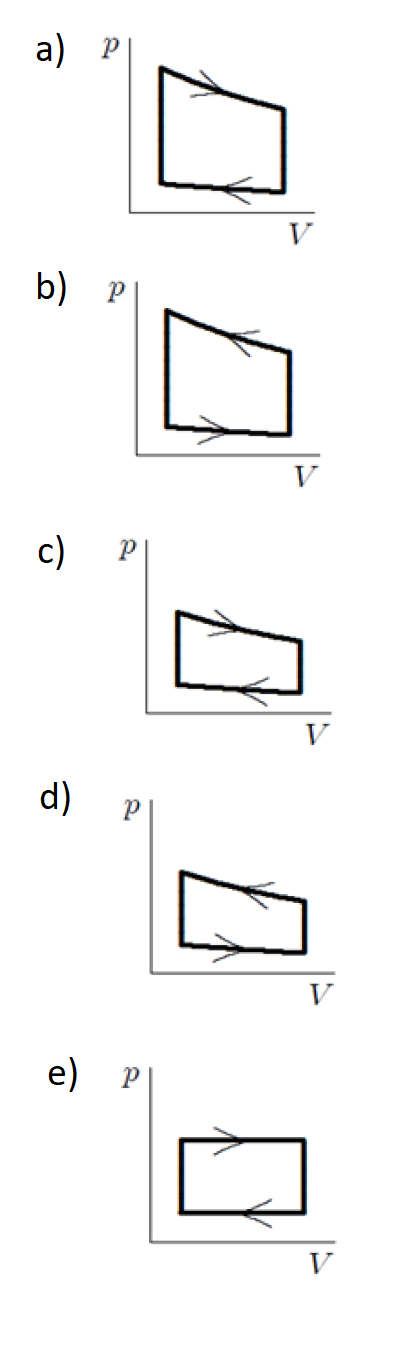
A (UDESC 2017) A figura mostra cinco gráficos da pressão em função do volume para um certo gás submetido a cinco processos cíclicos diferentes.
Assinale a alternativa que representa o ciclo termodinâmico no qual o gás realiza a maior quantidade de trabalho possível.
2016
(SEGUNDA LEI) A (UFRGS 2016) Uma máquina térmica, representada na figura abaixo, opera na sua máxima eficiência, extraindo calor de um reservatório em temperatura Tq = 527 °C, e liberando calor para um reservatório em temperatura Tf = 327 °C.
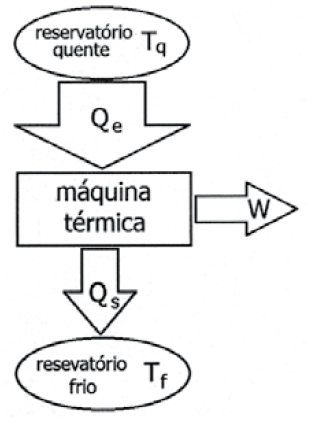 Para realizar um trabalho (W) de 600 J, o calor absorvido deve ser de
Para realizar um trabalho (W) de 600 J, o calor absorvido deve ser de
- a) 2400 J.
- b) 1800 J.
- c) 1581 J.
- d) 967 J.
- e) 800 J.
(SEGUNDA LEI) E (UDESC 2016) Analise as proposições em relação às informações sobre os motores a combustão, usados em automóveis.
I. Automóveis mais potentes conseguem transformar a maior parte da energia fornecida pelo combustível em trabalho.
II. O rendimento máximo de um motor a gasolina está próximo de 30%, mesmo reduzindo as perdas de energia em seu interior – independentemente do fabricante e do modelo do carro.
III. O trabalho externo necessário para comprimir a substância de operação nos pistões deve ser maior que o trabalho resultante da expansão dessa substância.
IV. É possível reaproveitar a maior parte do calor transferido para a fonte fria para gerar trabalho.
V. Ao produzir um movimento ordenado, há um aumento da entropia do ambiente ao redor do automóvel.
Assinale a alternativa correta.
- a) Somente as afirmativas I e II são verdadeiras.
- b) Somente as afirmativas II, IV e V são verdadeiras.
- c) Somente as afirmativas III e IV são verdadeiras.
- d) Somente as afirmativas I e III são verdadeiras.
- e) Somente as afirmativas II e V são verdadeiras.
B (UDESC 2016) Com relação à termodinâmica, analise as proposições.
I. Todas as substâncias aumentam de volume quando a temperatura delas aumenta.
II. Analisando o calor específico de um corpo, pode-se saber como é a taxa de aquecimento ou de resfriamento dele.
III. Correntes de convecção são geradas devido à variação de energia interna de um gás em um recipiente fechado.
IV. Uma transformação adiabática ocorre sem trocas de energia térmica entre o sistema e o meio externo e, consequentemente, sem variação de temperatura.
Assinale a alternativa correta.
- a) Somente as afirmativas I e III são verdadeiras.
- b) Somente a afirmativa II é verdadeira.
- c) Somente as afirmativas II, III e IV são verdadeiras.
- d) Somente as afirmativas II e IV são verdadeiras.
- e) Somente a afirmativa IV é verdadeira.
(SEGUNDA LEI) B (UDESC 2016) Uma máquina a vapor foi projetada para operar entre duas fontes térmicas, a fonte quente e a fonte fria, e para trabalhar segundo o ciclo de Carnot. Sabe-se que a temperatura da fonte quente é de 127 °C e que a máquina retira, a cada ciclo, 600J desta fonte, alcançando um rendimento máximo igual a 0,25. O trabalho realizado pela máquina, por ciclo, e a temperatura da fonte fria são, respectivamente:
- a) 240 J e 95 °C
- b) 150 J e 27 °C
- c) 15 J e 95 °C
- d) 90 J e 27 °C
- e) 24 J e 0 °C
2015
C (FUVEST 2015) O desenvolvimento de teorias científicas, geralmente, tem forte relação com contextos políticos, econômicos, sociais e culturais mais amplos. A evolução dos conceitos básicos da Termodinâmica ocorre, principalmente, no contexto
- a) da Idade Média.
- b) das grandes navegações.
- c) da Revolução Industrial.
- d) do período entre as duas grandes guerras mundiais.
- e) da Segunda Guerra Mundial.
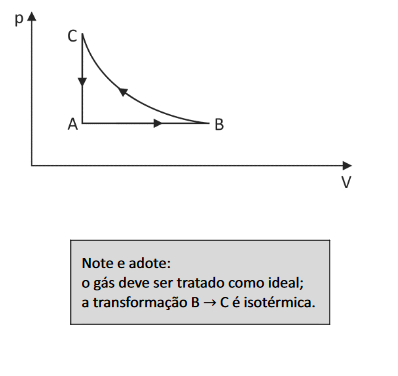
(PRIMEIRA LEI) E (FUVEST 2015) Certa quantidade de gás sofre três transformações sucessivas, A-B, B-C e C-A, conforme o diagrama p-V apresentado na figura abaixo. A respeito dessas transformações, afirmou-se o seguinte:
- O trabalho total realizado no ciclo ABCA é nulo.
- A energia interna do gás no estado C é maior que no estado A.
- Durante a transformação A՜B, o gás recebe calor e realiza trabalho.
Está correto apenas o que se afirma em
- a) I.
- b) II.
- c) III.
- d) I e II.
- e) II e III.
C (UDESC 2015) Analise as proposições com relação às leis da termodinâmica.
I. A variação da energia interna de um sistema termodinâmico é igual à soma da energia na forma de calor fornecida ao sistema e do trabalho realizado sobre o sistema.
II. Um sistema termodinâmico isolado e fechado aumenta continuamente sua energia interna.
III. É impossível realizar um processo termodinâmico cujo único efeito seja a transferência de energia térmica de um sistema de menor temperatura para um sistema de maior temperatura.
Assinale a alternativa correta.
- a) Somente as afirmativas I e II são verdadeiras.
- b) Somente as afirmativas II e III são verdadeiras.
- c) Somente as afirmativas I e III são verdadeiras.
- d) Somente a afirmativa II é verdadeira.
- e) Todas as afirmativas são verdadeiras.
2013
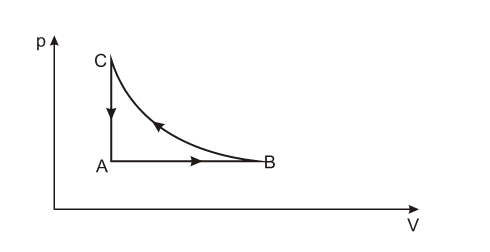
(PRIMEIRA LEI) E (FUVEST 2015) Certa quantidade de gás sofre três transformações sucessivas, A → B, B → C e C → A, conforme o diagrama p x V apresentado na figura abaixo.
A respeito dessas transformações, afirmou-se o seguinte:
- O trabalho total realizado no ciclo ABCA é nulo.
- A energia interna do gás no estado C é maior que no estado A.
- Durante a transformação A → B, o gás recebe calor e realiza trabalho.
Está correto o que se afirma em:
- a) I
- b) II
- c) III
- d) I e II
- e) II e III
(PRIMEIRA LEI) A (CFTMG 2014) O trabalho realizado em um ciclo térmico fechado é igual a 100 J e, o calor envolvido nas trocas térmicas é igual a 1000 J e 900 J, respectivamente, com fontes quente e fria.
A partir da primeira Lei da Termodinâmica, a variação da energia interna nesse ciclo térmico, em joules, é
- a) 0
- b) 100
- c) 800
- d) 900
- e) 1000
(PRIMEIRA LEI) D (UERN 2013) A variação da energia interna de um gás perfeito em uma transformação isobárica foi igual a 1200 J. Se o gás ficou submetido a uma pressão de 50 N/m2 e a quantidade de energia que recebeu do ambiente foi igual a 2000 J, então, a variação de volume sofrido pelo gás durante o processo foi
- a) 10 m3.
- b) 12 m3.
- c) 14 m3.
- d) 16 m3.
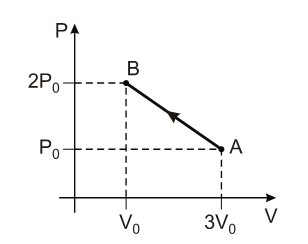
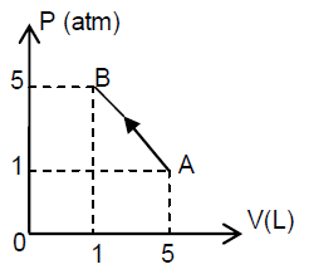
(PRIMEIRA LEI) A (UFRGS 2013) Uma amostra de gás ideal evolui de um estado A para um estado B, através de um processo, em que a pressão P e o volume V variam conforme o gráfico abaixo.
Considere as seguintes afirmações sobre esse processo.
- A temperatura do gás diminuiu.
- O gás realizou trabalho positivo.
- Este processo é adiabático.
Quais estão corretas?
- a) Apenas I.
- b) Apenas II.
- c) Apenas III.
- d) Apenas I e III.
- e) I, II e III.
C (UFRN 2013) A biomassa é uma das principais fontes de energia renovável e, portanto, máquinas que a utilizam como combustível para geração de energia são importantes do ponto de vista ambiental. Um exemplo bastante comum é o uso da biomassa com o objetivo de acionar uma turbina a vapor para gerar trabalho. A figura a seguir mostra, esquematicamente, uma usina termoelétrica simplificada. Nessa termoelétrica, a queima da biomassa na fornalha produz calor, que aquece a água da caldeira e gera vapor a alta pressão. O vapor, por sua vez, é conduzido por tubulações até a turbina que, sob a ação deste, passa a girar suas pás.
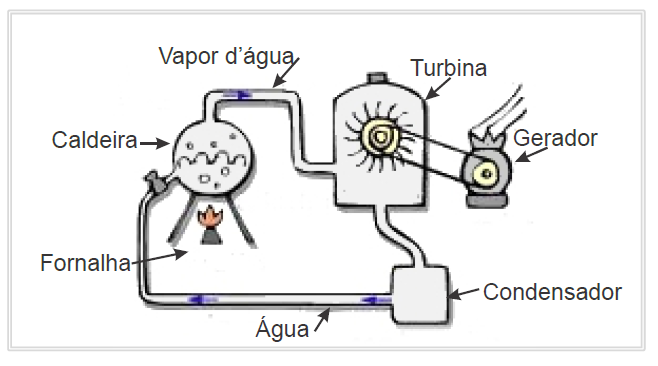 Considere desprezíveis as perdas de calor devido às diferenças de temperatura entre as partes dessa máquina térmica e o ambiente. Nesse contexto, a variação da energia interna da água da caldeira
Considere desprezíveis as perdas de calor devido às diferenças de temperatura entre as partes dessa máquina térmica e o ambiente. Nesse contexto, a variação da energia interna da água da caldeira
- a) é maior que a soma do calor a ela fornecido pela queima da biomassa com o trabalho realizado sobre a turbina.
- b) é igual à soma do calor a ela fornecido pela queima da biomassa com o trabalho realizado sobre a turbina.
- c) é igual à diferença entre o calor a ela fornecido pela queima da biomassa e o trabalho realizado sobre a turbina.
- d) é maior que a diferença entre calor a ela fornecido pela queima da biomassa e o trabalho realizado sobre a turbina.
2012
(PRIMEIRA LEI) (UEM 2012) Um cilindro com pistão, contendo uma amostra de gás ideal, comprime a amostra de maneira que a temperatura, tanto do cilindro com pistão quanto da amostra de gás ideal, não varia. O valor absoluto do trabalho realizado nessa compressão é de 400 J. Sobre o exposto, assinale o que for correto.
01) O trabalho é positivo, pois foi realizado sobre o gás.
02) A transformação é denominada adiabática.
04) A energia interna do gás aumentou, pois este teve seu volume diminuído.
08) O gás ideal cedeu uma certa quantidade de calor à vizinhança.
16) A quantidade de calor envolvida na compressão de gás foi de 200 J.
RESPOSTA: 08
(PRIMEIRA LEI) C (UPF 2012) Uma amostra de um gás ideal se expande duplicando o seu volume durante uma transformação isobárica e adiabática. Considerando que a pressão experimentada pelo gás é 5 x 106 Pa e seu volume inicial 2 x 10-5 m3, podemos afirmar:
- a) O calor absorvido pelo gás durante o processo é de 25 cal.
- b) O trabalho efetuado pelo gás durante sua expansão é de 100 cal.
- c) A variação de energia interna do gás é de –100 J.
- d) A temperatura do gás se mantém constante.
- e) Nenhuma das anteriores.
(PRIMEIRA LEI) (UEM 2012) Sobre as transformações termodinâmicas que podem ocorrer com um gás ideal confinado em um cilindro com pistão, assinale o que for correto.
01) Um gás ideal realiza trabalho ao se expandir, empurrando o pistão contra uma pressão externa.
02) Em uma transformação adiabática ocorre troca de calor com a vizinhança.
04) A energia interna de uma amostra de gás ideal não varia, quando este sofre uma transformação isovolumétrica.
08) Quando o gás ideal sofre uma compressão, o trabalho é realizado por um agente externo sobre o gás ideal.
16) O gás ideal não realiza trabalho em uma transformação isovolumétrica.
RESPOSTA: 01 + 08 + 16 = 25.
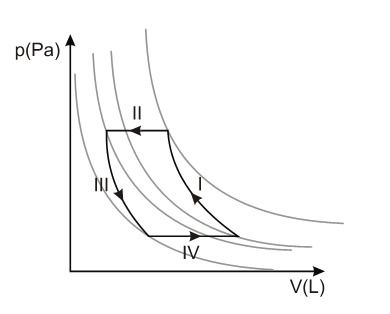
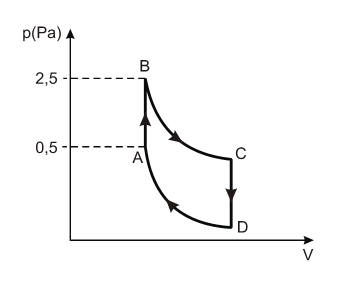
(PRIMEIRA LEI) D (IFSC 2012) Você já se perguntou como funciona a geladeira? De que maneira ela consegue diminuir a temperatura dos alimentos? Pelo menos sabe, do ponto de vista físico, explicar o que acontece? A geladeira é uma máquina térmica fria, que transforma trabalho em calor. Como máquina térmica, ela respeita um ciclo de transformações (duas isobáricas e duas adiabáticas), como mostra a figura abaixo.
Identifique em qual transformação a temperatura do gás atinge o seu menor valor. Assinale a alternativa CORRETA.
- a) Transformação IV – expansão isobárica.
- b) Transformação I – compressão adiabática.
- c) Transformação II – compressão isobárica.
- d) Transformação III – expansão adiabática.
- e) Transformação III – compressão adiabática.
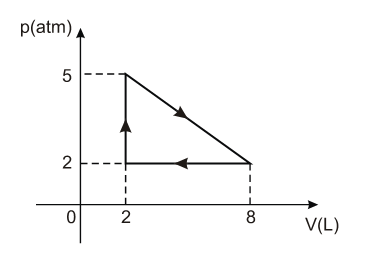
(PRIMEIRA LEI) A (UERN 2012) Considere a transformação cíclica de um gás perfeito representada no gráfico.
A variação da energia interna e o trabalho em cada ciclo são, respectivamente, iguais a
- a) 0 e 900 J.
- b) 900 J e 0.
- c) – 900 J e 0.
- d) 0 e – 900 J.
A (FEI 2011) Em um cilindro de acionamento de uma porta, um gás ideal à pressão de 2 atm sofre uma transformação isobárica e seu volume varia de 20 litros para 100 litros. Desprezando-se as perdas, qual é o trabalho realizado pelo gás?
- a) 160 atm x L
- b) 180 atm x L
- c) 200 atm x L
- d) 140 atm x L
- e) 120 atm x L
E (FEI 2012) A transformação AB realizada por um gás está representada no gráfico abaixo. Nestas condições, qual é o trabalho realizado pelo gás?
- a) 10 atm.L
- b) –8 atm.L
- c) 8 atm.L
- d) 12 atm.L
- e) –12 atm.L
A (IFMG 2012) Um gás em uma máquina térmica sofre uma transformação cíclica conforme o gráfico pressão (p) versus volume (V) abaixo:
Podemos afirmar que o trabalho realizado pelo gás em um ciclo completo vale:
- a) 1600 J.
- b) 1400 J.
- c) 800 J.
- d) 4200 J.
A (IFMG 2012) Um engenheiro afirma que construiu uma máquina térmica que realiza um trabalho equivalente a 1/3 do calor liberado para a fonte fria. O rendimento dessa máquina é de, aproximadamente:
- a) 25%.
- b) 33%.
- c) 66%.
- d) 75%.
E (PUC CAMP 2012) A Revolução Industrial nos trouxe o desenvolvimento das máquinas térmicas, como, por exemplo, uma locomotiva a vapor.
Determinada máquina térmica que funciona em ciclos com frequência de 20 ciclos/s, recebe 800 J de calor de uma fonte quente enquanto rejeita 600 J de calor para uma fonte fria em cada ciclo. Está correto afirmar que:
- a) O período de funcionamento da máquina é de 0,5 s.
- b) O trabalho realizado pela máquina vale 200 J, independentemente do tempo de funcionamento da máquina.
- c) A principal característica de uma máquina térmica é seu alto rendimento.
- d) O rendimento dessa máquina é 75%.
- e) A potência útil da máquina é de 40 kW.
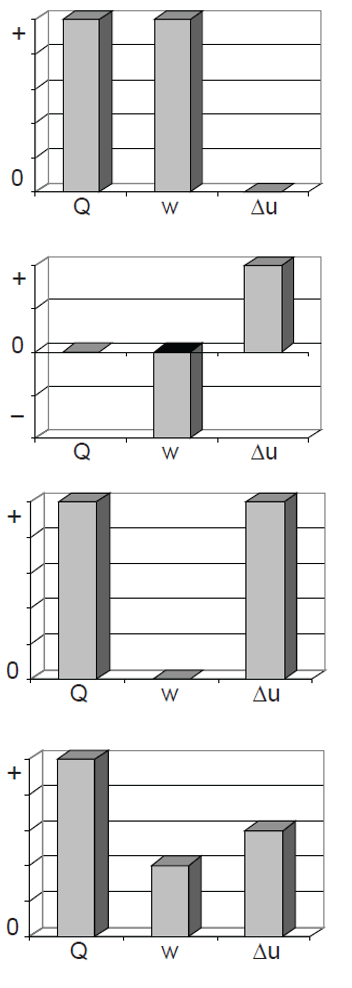
D (PUC RS 2012) Os histogramas a seguir mostram o calor Q e o trabalho W trocados por um gás com o meio externo, bem como a variação da sua energia interna “U. O gás segue a equação geral dos gases (Pv = nRT) nos processos termodinâmicos apresentados.
De acordo com os respectivos histogramas, em ordem de apresentação, de cima para baixo, os processos podem ser:
- a) adiabático – isotérmico – isovolumétrico – isobárico
- b) adiabático – isovolumétrico – isotérmico – isobárico
- c) isotérmico – isobárico – isovolumétrico – adiabático
- d) isotérmico – adiabático – isovolumétrico – isobárico
- e) isobárico – isotérmico – adiabático – isovolumétrico
D (UEMG 2012) A temperatura de um sistema pode ser alterada, quando ele troca trabalho ou calor com sua vizinhança. Seja um sistema constituído por um gás no interior de um cilindro, dotado de êmbolo móvel. Assinale, abaixo, a alternativa com a descrição CORRETA da situação em que a temperatura do sistema irá diminuir:
- a) O sistema recebe uma quantidade de calor maior que o trabalho que ele realiza numa expansão.
- b) O êmbolo é comprimido bruscamente.
- c) O gás sofre uma expansão, realizando trabalho, enquanto recebe uma quantidade de calor de mesmo valor que o trabalho realizado.
- d) O trabalho realizado pelo sistema é maior que a quantidade de calor que ele recebe da vizinhança.
2011
(PRIMEIRA LEI) (UEPG 2011) A 1ª lei da termodinâmica pode ser entendida como uma afirmação do princípio da conservação da energia. Sua expressão analítica é dada por ∆U = Q – τ, onde ∆U corresponde à variação da energia interna do sistema, Q e τ, respectivamente, calor trocado e trabalho realizado.
Sobre a 1ª lei da termodinâmica aplicada a transformações abertas, assinale o que for correto.
01) O sistema pode receber trabalho sem fornecer calor e sua energia interna aumenta.
02) O sistema pode receber calor sem realizar trabalho e sua energia interna aumenta.
04) O sistema pode, simultaneamente, receber calor e trabalho e sua energia interna aumenta.
08) O sistema pode realizar trabalho sem receber calor e sua energia interna diminui.
16) O sistema pode fornecer calor sem receber trabalho e sua energia interna diminui.
RESPOSTA: 01 + 02 + 04 + 08 + 16 = 31
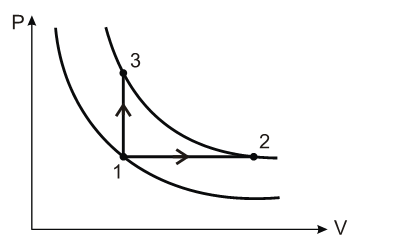
(PRIMEIRA LEI) D (UFSM 2011) A invenção e a crescente utilização de máquinas térmicas, a partir da revolução industrial, produziram, ao longo de dois séculos, impactos ecológicos de proporções globais. Para compreender o funcionamento das máquinas térmicas, é necessário estudar os processos de expansão e compressão dos gases no seu interior. Em certas condições, todos os gases apresentam, aproximadamente, o mesmo comportamento. Nesse caso, são denominados gases ideais. Considere o diagrama pressão (P) x volume (V) para um gás ideal, sendo as curvas isotermas.
Analise, então, as afirmativas:
- A energia interna do estado 1 é maior do que a energia interna do estado 2.
- No processo 1→3, o gás não realiza trabalho contra a vizinhança.
- No processo 1→2, o gás recebe energia e também fornece energia para a vizinhança.
Está(ão) correta(s)
- a) apenas I.
- b) apenas II.
- c) apenas III.
- d) apenas II e III.
- e) I, II e III.
(PRIMEIRA LEI) (UFPE 2011) Um gás ideal se transforma de acordo com o ciclo termodinâmico mostrado abaixo no diagrama pressão versus volume. Os processos AB e CD são isovolumétricos, e os processos BC e DA são isotérmicos. Qual a razão TC/TD entre as respectivas temperaturas absolutas do gás nos pontos C e D?
RESPOSTA: 5
D (PUC RJ 2011) Em um processo termodinâmico, uma quantidade de n moles de um gás ideal é aquecida por uma quantidade de calor Q = 1000 J e realiza trabalho igual a W. Ao fim do processo termodinâmico, o sistema retorna à temperatura inicial, ou seja, à energia inicial. Calcule o trabalho realizado.
- a) 1000 nJ.
- b) 0 J.
- c) 2000 J.
- d) 1000 J.
- e) 500 J.
B (UDESC 2011) Um gás em uma câmara fechada por um êmbolo móvel recebe lentamente 12,5 cal de uma fonte de calor. Nesse processo, o gás sofre uma expansão isobárica, à pressão de 5,0 x 105 N/m2, de tal maneira que sua temperatura aumenta de 300 K para 900 K. Sabendo que inicialmente a energia interna do gás era de 15,0 J, e seu volume era de 20,0 cm3, a energia interna final corresponde a:
- a) 30 % da energia inicial
- b) 300 % da energia inicial
- c) – 30 % da energia inicial
- d) – 50 % da energia inicial
- e) 50 % da energia inicial
B (UEFS 2011) Referindo-se ao estado final de um gás ideal que foi expandido adiabaticamente, é correto afirmar:
- a) A temperatura do gás aumenta.
- b) A temperatura do gás diminui.
- c) A energia interna do gás aumenta.
- d) A energia interna do gás se mantém constante.
- e) A variação da energia interna do gás é igual à quantidade de calor trocado com o meio exterior.
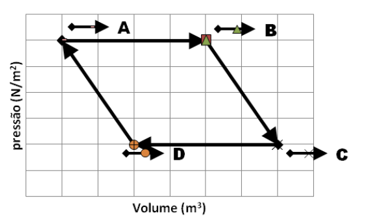
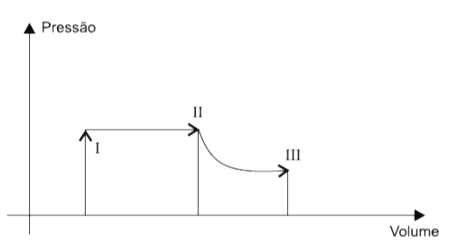
C (UFES 2011) A análise da figura, que representa sucessivas transformações realizadas por uma massa gasosa, permite afirmar que as transformações I, II e III são, respectivamente,
- a) isobárica – isocórica – isotérmica.
- b) isobárica – isotérmica – isocórica.
- c) isocórica – isobárica – isotérmica.
- d) isotérmica – isobárica – isocórica.
- e) adiabática – isobárica – isocórica.
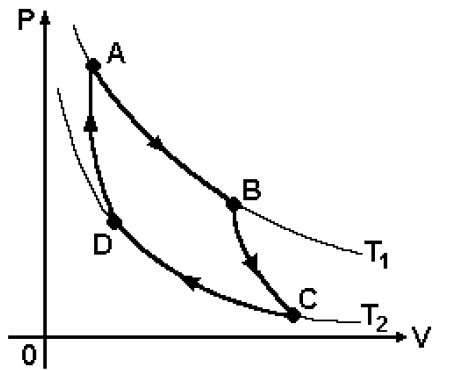
C (IFMG 2011) Considere o ciclo de Carnot a seguir, para um dado gás ideal.
- a) A temperatura do gás diminui durante a expansão adiabática.
- b) O gás recebe calor de um dos reservatórios térmicos durante a expansão isotérmica.
- c) A energia interna do gás diminui durante a compressão isotérmica.
- d) Ao final de cada ciclo, o gás retorna à temperatura inicial.
2010
D (UFRN 2010) A transformação termodinâmica b → c, ilustrada no diagrama PV da figura a seguir, constitui um dos processos do ciclo Otto, utilizado em motores de combustão interna de automóveis a gasolina. No diagrama, P representa a pressão na câmara de combustão, e V o volume da câmara.
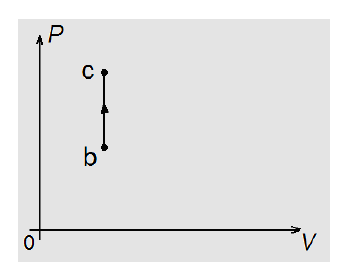 Esse processo ocorre quando, no instante da queima da mistura ar-gasolina contida na câmara de combustão, fornece-se calor ao sistema, produzindo-se:
Esse processo ocorre quando, no instante da queima da mistura ar-gasolina contida na câmara de combustão, fornece-se calor ao sistema, produzindo-se:
- a) aumento da pressão interna, com variação do volume da câmara.
- b) diminuição da pressão interna, sem variação do volume da câmara.
- c) diminuição da pressão interna, com variação do volume da câmara.
- d) aumento da pressão interna, sem variação do volume da câmara.
2009
B (ESPCEX 2009) Podemos afirmar que, para um gás ideal, ao final de toda transformação cíclica,
- a) o calor total trocado pelo gás é nulo.
- b) a variação da energia interna do gás é nula.
- c) o trabalho realizado pelo gás é nulo.
- d) a pressão interna do gás diminui.
- e) o volume interno do gás aumenta.
B (UFRN 2009) Até o século XVIII, pensava-se que uma máquina térmica, operando numa condição mínima de atrito, poderia converter em trabalho útil praticamente toda a energia térmica a ela fornecida.
Porém, Sadi Carnot (1796-1832) mostrou que, em se tratando da energia fornecida a uma máquina térmica, a fração máxima que pode ser convertida em trabalho útil depende da diferença de temperatura entre a fonte quente e a fonte fria e é dada por:
, onde T1 é a temperatura da fonte fria, e T2 é a temperatura da fonte quente.
Dessas afirmações, pode-se concluir que uma máquina térmica
- a) pode converter em trabalho útil toda a energia térmica a ela fornecida, mesmo que funcione em condições mínimas de atrito.
- b) não pode converter em trabalho útil toda a energia térmica a ela fornecida, mesmo que funcione em condições mínimas de atrito.
- c) pode converter em trabalho útil toda a energia térmica a ela fornecida, desde que a temperatura da fonte fria seja 0 °C.
- d) não pode converter em trabalho útil toda a energia térmica a ela fornecida, a menos que a temperatura da fonte fria seja diferente de 0 °C .
2002
A (UNIFESP 2002) Costuma-se especificar os motores dos automóveis com valores numéricos, 1.0, 1.6, 1.8 e 2.0, entre outros. Esses números indicam também valores crescentes da potência do motor. Pode-se explicar essa relação direta entre a potência do motor e esses valores numéricos porque eles indicam o volume aproximado, em litros,
- a) de cada cilindro do motor e, quanto maior esse volume, maior a potência que o combustível pode fornecer.
- b) do consumo de combustível e, quanto maior esse volume, maior a quantidade de calor que o combustível pode fornecer.
- c) de cada cilindro do motor e, quanto maior esse volume, maior a temperatura que o combustível pode atingir.
- d) do consumo de combustível e, quanto maior esse volume, maior a temperatura que o combustível pode fornecer.
- e) de cada cilindro do motor e, quanto maior esse volume, maior o rendimento do motor.