QUÍMICA – LISTA DE EXERCÍCIOS SOBRE TABELA PERIÓDICA
(ORGANIZAÇÃO DA TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS E APERIÓDICAS)
CAIU NO ENEM!
C (ENEM 2017) No ar que respiramos existem os chamados gases inertes”. Trazem curiosos nomes gregos, que significam “O Novo”, “o Oculto”, “o Inativo”. E de fato são de tal modo inertes, tão satisfeitos em sua condição, que não interferem em nenhuma reação química, não se combinam com nenhum outro elemento e justamente por esse motivo ficaram sem ser observados durante séculos: só em 1962 um químico, depois de longos e engenhosos esforços, conseguiu forçar “o Estrangeiro” (o Xenônio) a combinar-se fugazmente com o flúor ávido e vivaz, e a façanha pareceu tão extraordinária que lhe foi conferido o Prêmio Nobel.
Qual propriedade do flúor justifica sua escolha como reagente para o processo mencionado?
- a) Densidade.
- b) Condutância.
- c) Eletronegatividade
- d) Estabilidade nuclear
- e) Temperatura de ebulição.
CAIU NO VESTIBULAR!
2018
(PROPRIEDADES PERIÓDICAS) B (UNESP 2018) Considere os elementos K, Co, As e Br, todos localizados no quarto período da Classificação Periódica. O elemento de maior densidade e o elemento mais eletronegativo
são, respectivamente,
- a) K e As.
- b) Co e Br.
- c) K e Br.
- d) Co e As.
- e) Co e K.
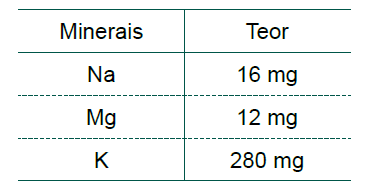
C (FCMSCSP 2018) A água de coco, bebida rica em potássio, contribui para reduzir a pressão arterial alta que está relacionada ao risco de doenças cardíacas. A tabela mostra os principais minerais encontrados em uma porção de 200 mL de água de coco.
O teor de potássio nessa porção da água de coco e o elemento listado na tabela que apresenta a maior energia de ionização são
- a) 1,4 g/L e sódio.
- b) 1,4 g/L e potássio.
- c) 1,4 g/L e magnésio.
- d) 2,8 g/L e sódio.
- e) 2,8 g/L e magnésio.
(PROPRIEDADES PERIÓDICAS) E (UFJF – PISM 1 2018) Metais como cobre, zinco, cobalto e molibdênio possuem função biológica conhecida e são constituintes obrigatórios para o metabolismo dos seres humanos e por isso são considerados essenciais. Porém, não podem ser ingeridos em altas concentrações, pois são suas propriedades, assinale a alternativa que apresenta a afirmativa
- a) O símbolo do elemento químico cobre é Co.
- b) O elemento mais eletronegativo é molibdênio.
- c) O zinco e o cobre estão na mesma família.
- d) A distribuição eletrônica do molibdênio é 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 4d5.
- e) O zinco é o elemento que possui maior energia de ionização quando comparado ao cobre e ao cobalto.
C (UDESC 2018) Analise as proposições em relação aos átomos na classificação periódica dos elementos químicos.
I. Os átomos do tálio são maiores que os átomos do bário.
II. Os átomos do germânio são mais eletronegativos que os de carbono.
III. A configuração eletrônica dos átomos de titânio, em ordem crescente de energia, é 1s22s22p63s23p64s23d2 .
IV. Os átomos de bromo são os mais eletronegativos do quarto período da tabela periódica.
Assinale a alternativa correta.
- a) Somente a afirmativa II é verdadeira.
- b) Somente as afirmativas I e IV são verdadeiras.
- c) Somente as afirmativas III e IV são verdadeiras.
- d) Somente as afirmativas I e III são verdadeiras.
- e) Somente a afirmativa III é verdadeira.
2017
C (UFJF – PISM 1 2017) O mercúrio é um elemento químico que apresenta como temperaturas de fusão -38 °C e de ebulição, 357 °C. Forma liga metálica facilmente com muitos outros metais, como o ouro ou a prata, produzindo amálgamas. Sobre o mercúrio é correto afirmar que:
- a) forma uma mistura heterogênea na produção de amálgamas com ouro.
- b) apresenta 80 elétrons e 80 nêutrons.
- c) encontra-se no estado líquido na temperatura ambiente (24 °C).
- d) localiza-se no quinto período da tabela periódica.
- e) apresenta distribuição eletrônica [Xe] 6s2 4f14 4d10.
B (UFPR 2017) As propriedades das substâncias químicas podem ser previstas a partir das configurações eletrônicas dos seus elementos. De posse do número atômico, pode-se fazer a distribuição eletrônica e localizar a posição de um elemento na tabela periódica, ou mesmo prever as configurações dos seus íons. Sendo o cálcio pertencente ao grupo dos alcalinos terrosos e possuindo número atômico Z = 20, a configuração eletrônica do seu cátion bivalente é:
- a) 1s2 2s2 2p6 3s2
- b) 1s2 2s2 2p6 3s2 3p6
- c) 1s2 2s2 2p6 3s2 3p6 4s2
- d) 1s2 2s2 2p6 3s2 3p6 4s2 3d2
- e) 1s2 2s2 2p6 3s2 3p6 4s2 4p2
D (FGV SP 2017) Um professor de química propôs uma atividade lúdica a seus alunos denominada “Caça ao PoQUÍmon”. Ele confeccionou fichas que apresentavam a figura e o nome de um personagem do jogo Pokemon Go®. O aluno deveria localizar, na tabela periódica, a família de origem do personagem e, para isso, ele deveria primeiro identificar, no nome do personagem,
as representações de símbolos de elementos químicos. Só valiam letras lidas da esquerda para direita. A família de origem do personagem era aquela do elemento com maior eletronegatividade, dentre os elementos químicos simbolizados nas letras do seu nome.
Considere estes personagens:
 No jogo “Caça ao PoQUÍmon”, esses personagens pertencem, respectivamente, às famílias dos elementos
No jogo “Caça ao PoQUÍmon”, esses personagens pertencem, respectivamente, às famílias dos elementos
- a) alcalinos e do nitrogênio.
- b) alcalinos e calcogênios.
- c) halogênios e do nitrogênio.
- d) halogênios e calcogênios.
- e) alcalinos terrosos e calcogênios.
2016
2015
(PROPRIEDADES PERIÓDICAS) D (UFJF – PISM 1 2015) A descoberta das relações periódicas pelo químico russo Dmitri Mendeleev foi olhada com algum ceticismo pelos químicos da época, mas ganhou credibilidade quando se provou capaz de prever propriedades de elementos químicos que não haviam sido ainda descobertos. Essas propriedades são as mais variadas, como, por exemplo, densidade, raio atômico e eletronegatividade. Sabendo-se que a eletronegatividade do lítio é 0,98 e a do potássio é 0,82, a eletronegatividade do sódio é:
- a) 0,98.
- b) 0,49.
- c) 0,41.
- d) 0,93.
- e) 0,82.
E (FUVEST 2015) Quando começaram a ser produzidos em larga escala, em meados do século XX, objetos de plástico eram considerados substitutos de qualidade inferior para objetos feitos de outros materiais. Com o tempo, essa concepção mudou bastante. Por exemplo, canecas eram feitas de folha de flandres, uma liga metálica, mas, hoje, também são feitas de louça ou de plástico. Esses materiais podem apresentar vantagens e desvantagens para sua utilização em canecas, como as listadas a seguir:
- ter boa resistência a impactos, mas não poder ser levado diretamente ao fogo;
- poder ser levado diretamente ao fogo, mas estar sujeito a corrosão;
- apresentar pouca reatividade química, mas ter pouca resistência a impactos.
Os materiais utilizados na confecção de canecas os quais apresentam as propriedades I, II e III são, respectivamente,
- a) metal, plástico, louça.
- b) metal, louça, plástico.
- c) louça, metal, plástico.
- d) plástico, louça, metal.
- e) plástico, metal, louça.
2014
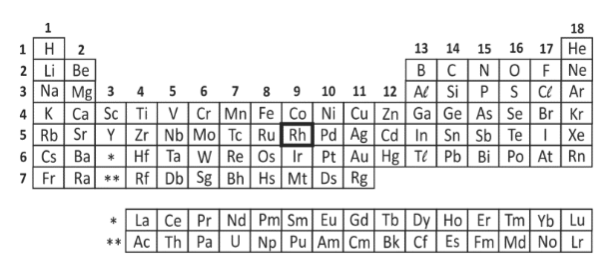
E (FUVEST 2014) Observe a posição do elemento químico ródio (Rh) na tabela periódica.
- a) Possui massa atômica menor que a do cobalto (Co).
- b) Apresenta reatividade semelhante à do estrôncio(Sr), característica do 5º período.
- c) É um elemento não metálico.
- d) É uma substância gasosa à temperatura ambiente.
- e) É uma substância boa condutora de eletricidade.
2013
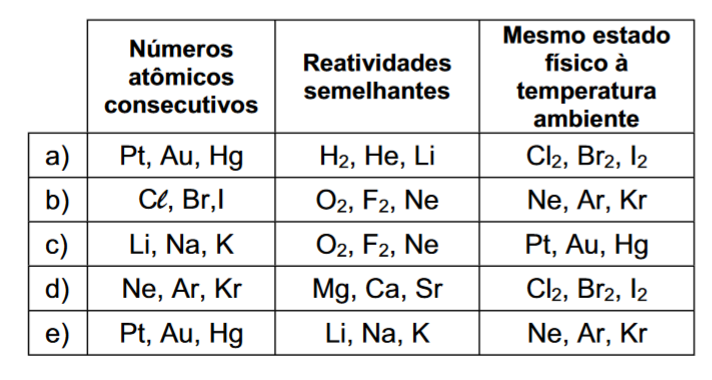
E (FUVEST 2013) Um aluno estava analisando a Tabela Periódica e encontrou vários conjuntos de três elementos químicos que apresentavam propriedades semelhantes.
Assinale a alternativa na qual os conjuntos de três elementos ou substâncias elementares estão corretamente associados às propriedades indicadas no quadro abaixo.
D (UFJF – PISM 1 2013) O enxofre é bastante utilizado na fabricação de fósforos, fogos de artifício e na vulcanização de borracha, entre outras aplicações. A distribuição eletrônica do elemento enxofre e sua posição na Tabela Periódica são, respectivamente:
- a) 1s2 2s2 2p6 3s2 3p4; grupo dos halogênios.
- b) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4; grupo do carbono.
- c) 1s2 2s2 2p6 3s2 3p6 3d104s2 4p4; grupo dos calcogênios.
- d) 1s2 2s2 2p6 3s2 3p4; grupo dos calcogênios.
- e) 1s2 2s2 2p6 3s2 3p4; grupo do carbono.
C (UERN 2013) De acordo com as propriedades da tabela periódica, marque a alternativa INCORRETA.
- a) Quanto maior um átomo, menor é a energia de ionização.
- b) O sódio apresenta um raio atômico maior do que o magnésio.
- c) Eletroafinidade é a energia absorvida quando um elétron é adicionado a um átomo neutro.
- d) A eletronegatividade aumenta de baixo para cima nas famílias da tabela periódica e, da esquerda para a direita, nos períodos.
2012
(PROPRIEDADES PERIÓDICAS) D (UFJF – PISM 1 2012) A tabela periódica é uma ferramenta importante que os químicos utilizam para organizar os elementos químicos de acordo com as propriedades periódicas. Utilizando a tabela periódica da prova, marque a opção que apresenta os átomos dos elementos Ne, K, He, Ar e Cs em ordem CRESCENTE de energia de ionização.
- a) He < Ne < Ar < K < Cs
- b) K< Cs < He < Ne < Ar
- c) Ne < Ar < He < K < Cs
- d) Cs < K < Ar < Ne < He
- e) Cs < K < He < Ar < Ne
C (UFJF – PISM 1 2012) O aço inoxidável é uma liga metálica cujos componentes majoritários são ferro e cromo, e os minoritários são, principalmente, níquel e molibdênio. Esse material apresenta alta resistência à oxidação atmosférica em relação ao aço comum. Analisando os elementos presentes no aço inoxidável, pode-se afirmar que:
- a) os elementos majoritários pertencem à mesma família da tabela periódica.
- b) todos os elementos citados estão no mesmo período da tabela periódica.
- c) o níquel apresenta configuração eletrônica [Ar] 4s2 3d8.
- d) os elementos minoritários possuem o elétron mais externo na mesma camada eletrônica.
- e) o ferro apresenta maior raio atômico que o cromo.
2011
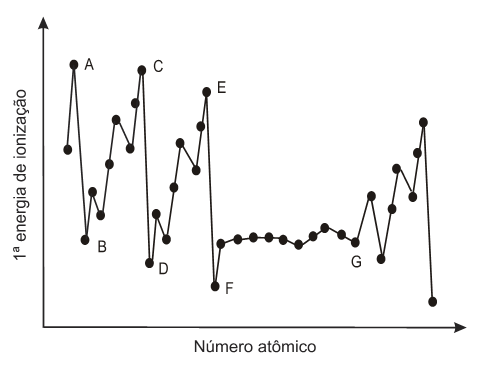
(PROPRIEDADES PERIÓDICAS) A (CEFET MG 2011) A curva a seguir mostra a variação da primeira energia de ionização com o numero atômico de alguns elementos da tabela periódica.
Com relação ao gráfico, é incorreto afirmar que o(os)
- a) trechos BC e DE estão associados as colunas 2A e 3A.
- b) elementos correspondentes aos pontos A, C e E são gases nobres.
- c) intervalo limitado pelos pontos F e G representa os elementos de transição.
- d) maior numero de níveis preenchidos causa a variação no eixo y entre os trechos AB, CD e EF.
(PROPRIEDADES PERIÓDICAS) D (UFPA 2011) Sobre o processo de ionização de um átomo A, mostrado abaixo,
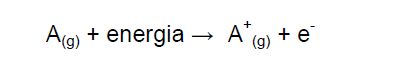 são feitas as seguintes afirmativas:
são feitas as seguintes afirmativas:
- A energia de ionização aumenta à medida que o raio atômico diminui; sendo assim, é necessária uma quantidade de energia maior para remover elétrons de átomos menores.
- O cátion formado possui um raio maior que o raio do átomo pelo fato de a perda do elétron deixar o átomo carregado mais positivamente e assim diminuir a atração entre os elétrons resultantes e o núcleo, o que promove a expansão da nuvem eletrônica.
- A primeira energia de ionização é sempre a maior e, consequentemente, a remoção de elétrons sucessivos do mesmo átomo se torna mais fácil.
- A energia de ionização em átomos localizados no mesmo período da tabela periódica aumenta no mesmo sentido do aumento da carga nuclear.
Estão corretas as afirmativas
- a) I e III
- b) II e IV
- c) II e III
- d) I e IV
- e) I, II e IV
2010
2009
(PROPRIEDADES PERIÓDICAS) A (UERJ 2009) Os metais formam um grupo de elementos químicos que apresentam algumas propriedades diferentes, dentre elas o raio atômico. Essa diferença está associada à configuração eletrônica de cada um. A ordenação crescente dos metais pertencentes ao terceiro período da tabela periódica, em relação a seus respectivos raios atômicos, está apontada em:
- a) alumínio, magnésio e sódio
- b) sódio, magnésio e alumínio
- c) magnésio, sódio e alumínio
- d) alumínio, sódio e magnésio