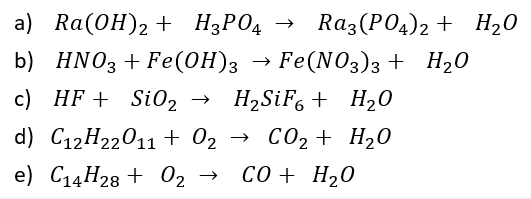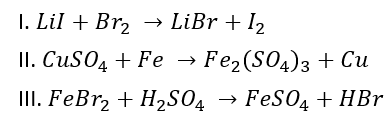QUÍMICA – LISTA DE EXERCÍCIOS SOBRE BALANCEAMENTO DE REAÇÕES
(MÉTODO DAS TENTATIVAS)
CAIU NO ENEM!
CAIU NO VESTIBULAR!
2018
A (UFPR 2018) O desenho abaixo ilustra como ocorre uma transformação química em que a espécie A (esferas cinzas) reage com a espécie B (esferas pretas), de modo a formar uma nova substância.
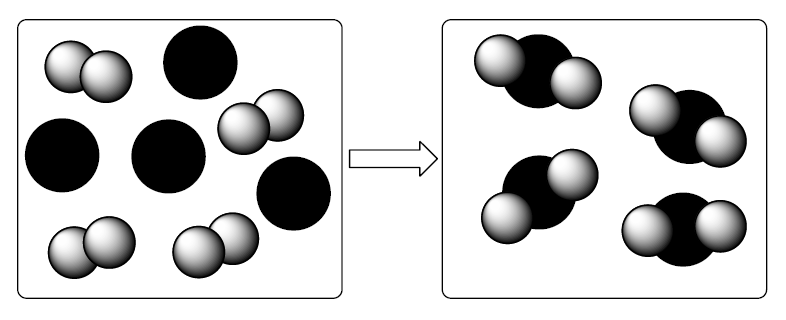
Qual é a equação química que descreve de maneira correta a reação que está esquematizada no desenho?
- a) A2 + B → A2B
- b) A2 + 4B → 2AB2
- c) 2A + B4 → 2AB2
- d) A + B2 → AB2
- e) A4 + B4 → 4AB
EXERCÍCIOS EXTRAS
(BALANCEAMENTO – MÉTODO DAS TENTATIVAS) E (CSA 1 – 2013 – BIA – S18) Devido ao seu alto valor de mercado, houve tentativas de sintetizar a quinina durante o século XIX. No entanto, como a estrutura da quinina ainda era desconhecida, essas tentativas dificilmente poderiam ser bem-sucedidas. Em 1856, o químico inglês William Perkin tentou sintetizá-la, sem sucesso, pela reação da aliltoluidina com uma fonte de oxigênio, conforme a equação não balanceada apresentada a seguir:
C10H13N + O2 → C20H24N2O2 + H2O
aliltoluidina quinina
A soma dos menores coeficientes inteiros que deixam a equação acima corretamente balanceada é:
- a) 7
- b) 8
- c) 9
- d) 10
- e) 11
BALANCEAMENTO – MÉTODO DAS TENTATIVAS) E (CSA 1 – 2012 – BIA – S25) (UFSM) O hidrogênio é o elemento mais abundante na nossa galáxia, ocorrendo principalmente na superfície solar, como H2 e, nos oceanos, lagos e gelos, como H2O. É também muito importante em diversos processos industriais.
O hidrogênio pode ser obtido por meio de vários processos, dentre eles:
- H2O + C → CO + H2
- H2O → O2 + H2
- C6H14 + H2O → CO2 + H2
Para balancear corretamente as equações, o coeficiente da molécula de hidrogênio em cada reação é, respectivamente:
- a) 1 – 2 – 14.
- b) 2 – 1 – 38.
- c) 2 – 1 – 19.
- d) 1 – 1 – 38.
- e) 1 – 2 – 19.
(BALANCEAMENTO – MÉTODO DAS TENTATIVAS) (CSA 1 – 2012 – BIA – U1) Faça o balanceamento das equações químicas a seguir:
(BALANCEAMENTO – MÉTODO DAS TENTATIVAS) E (CSA 1 – 2012 – BIA – UT10) Analise as seguintes equações químicas não balanceadas.
Balanceando-se as equações químicas com os menores coeficientes inteiros, obtêm-se, respectivamente, em:
- a) I: 1, 2, 1, 2.
- b) III: 1, 1, 1, 1.
- c) II e III: 3, 2, 1, 1.
- d) I e III: 2, 2, 1, 2.
- e) II: 3, 2, 1, 3.