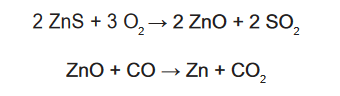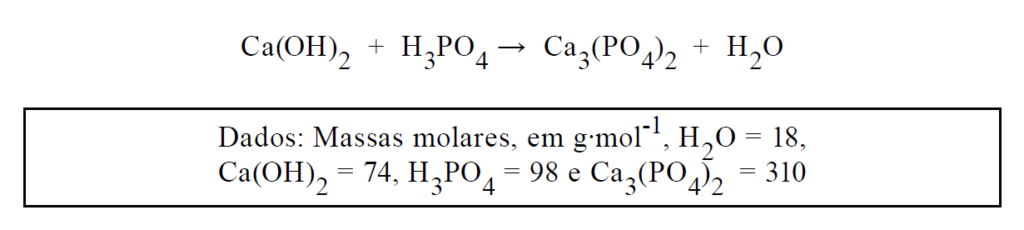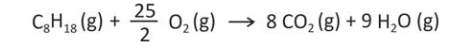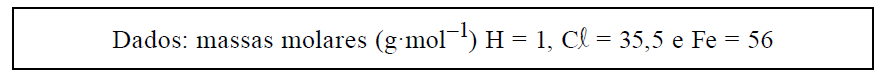CAIU NO ENEM!
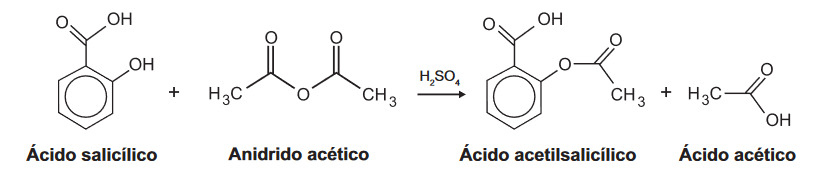
D (ENEM 2017) O ácido acetilsalicílico, AAS (massa molar igual a 180 g/mol) é sintetizado a partir da reação do ácido salicílico (massa molar igual a 138 g/mol) com anidrido acético, usando-se ácido sulfúrico como catalisador, conforme a equação química:
Após a síntese, o AAS é purificado e o rendimento final é de aproximadamente 50%. Devido às propriedades farmacológicas (antitérmico, analgésico e anti-inflamatório e antitrombótico), o AAS é utilizado como medicamento nas formas de comprimidos, nos quais se emprega tipicamente uma massa de 500 mg dessa substância.
Uma indústria farmacêutica pretende fabricar um lote de 900 mil comprimidos, de acordo com as especificações do texto. Qual é a massa de ácido salicílico, em kg, que deve ser empregada para esse fim?
- a) 293
- b) 345
- c) 414
- d) 690
- e) 828
D (ENEM 2016) A minimização do tempo e custo de uma reação química, bem como o aumento na sua taxa de conversão, caracterizam a eficiência de um processo químico. Como consequência, produtos podem chegar ao consumidor mais baratos. Um dos parâmetros que mede a eficiência de uma reação química é o seu rendimento molar (R, em %). definido como
 em que n corresponde ao número de mols. O metanol pode ser obtido pela reação entre brometo de metila e hidróxido de sódio, conforme a equação química:
em que n corresponde ao número de mols. O metanol pode ser obtido pela reação entre brometo de metila e hidróxido de sódio, conforme a equação química:
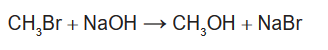 As massas molares (em g/mol) desses elementos são: H = 1: C = 12; O = 16; Na = 23; Br = 80.
As massas molares (em g/mol) desses elementos são: H = 1: C = 12; O = 16; Na = 23; Br = 80.
O rendimento molar da reação, em que 32 g de metanol foram obtidos a partir de 142,5 g de brometo de metila e 80 g de hidróxido de sódio, é mais próximo de
- a) 22%.
- b) 40%.
- c) 50%.
- d) 67%.
- e) 75%.
C (ENEM 2015) Para proteger estruturas de aço da corrosão, a indústria utiliza uma técnica chamada galvanização. Um metal bastante utilizado nesse processo é o zinco, que pode ser obtido a partir de um minério denominado esfalerita (ZnS), de pureza 75%. Considere que a conversão do minério em zinco metálico tem rendimento de 80% nesta sequência de equações químicas:
Considere as massas molares: ZnS (97 g/mol); O2 (32 g/mol); ZnO (81 g/mol); SO2 (64 g/mol); CO (28 g/mol); CO2 (44 g/mol); e Zn (65 g/mol).
Que valor mais próximo de massa de zinco metálico, em quilogramas, será produzido a partir de 100 kg de esfalerita?
- a) 25
- b) 33
- c) 40
- d) 50
- e) 54
D (ENEM 2014) Diesel é uma mistura de hidrocarbonetos que também apresenta enxofre em sua composição. Esse enxofre é um componente indesejável, pois o trióxido de enxofre gerado é um dos grandes causadores da chuva ácida. Nos anos 1980, não havia regulamentação e era utilizado óleo diesel com 13 000 ppm de enxofre. Em 2009, o diesel passou a ter 1 800 ppm de enxofre (S1800) e, em seguida, foi inserido no mercado o diesel S500 (500 ppm). Em 2012, foi difundido o diesel S50, com 50 ppm de enxofre em sua composição. Atualmente, é produzido um diesel com teores de enxofre ainda menores.
Os impactos da má qualidade do óleo diesel brasileiro. Disponlvel em: www.cnt.org.br. Acesso em: 20 dez. 2012 (adaptado).
A substituição do diesel usado nos anos 1980 por aquele difundido em 2012 permitiu uma redução percentual de emissão de SO3 de
- a) 86,2%.
- b) 96,2%.
- c) 97,2%.
- d) 99,6%.
- e) 99,9%.
B (ENEM 2013) O brasileiro consome em média 500 miligramas de cálcio por dia, quando a quantidade recomendada é o dobro. Uma alimentação balanceada é a melhor decisão para evitar problemas no futuro, como a osteoporose, uma doença que atinge os ossos. Ela se caracteriza pela diminuição substancial de massa óssea, tornando os ossos frágeis e mais suscetíveis a fraturas.
Disponível em: www.anvisa.gov.br. Acesso em: 1 ago. 2012 (adaptado).
Considerando-se o valor de 6 × 1023 mol–1 para a constante de Avogadro e a massa molar do cálcio igual a 40 g/mol, qual a quantidade mínima diária de átomos de cálcio a ser ingerida para que uma pessoa supra suas necessidades?
- a) 7,5 × 1021
- b) 1,5 × 1022
- c) 7,5 × 1023
- d) 1,5 × 1025
- e) 4,8 × 1025
D (ENEM 2013) A produção de aço envolve o aquecimento do minério de ferro, junto com carvão (carbono) e ar atmosférico em uma série de reações de oxirredução. O produto é chamado de ferro-gusa e contém cerca de 3,3% de carbono. Uma forma de eliminar o excesso de carbono é a oxidação a partir do aquecimento do ferro-gusa com gás oxigênio puro. Os dois principais produtos formados são aço doce (liga de ferro com teor de 0,3% de carbono restante) e gás carbônico. As massas molares aproximadas dos elementos carbono e oxigênio são, respectivamente, 12 g/mol e 16 g/mol.
LEE, J. D. Química Inorgânica não tão concisa. São Paulo: Edgard Blucher, 1999 (adaptado).
Considerando que um forno foi alimentado com 2,5 toneladas de ferro-gusa, a massa de gás carbônico formada, em quilogramas, na produção de aço doce, é mais próxima de
- a) 28.
- b) 75.
- c) 175.
- d) 275.
- e) 303.
B (ENEM 2012) No Japão, um movimento nacional para a promoção da luta contra o aquecimento global leva o slogan: 1 pessoa, 1 dia, 1 kg de CO2 a menos! A ideia é cada pessoa reduzir em 1 kg a quantidade de CO2 emitida todo dia, por meio de pequenos gestos ecológicos, como diminuir a queima de gás de cozinha.
Um hamburguer ecológico? É pra já! Disponível em: http://lqes.iqm.unicamp.br.
Acesso em: 24 fev. 2012 (adaptado).
Considerando um processo de combustão completa de um gás de cozinha composto exclusivamente por butano (C4H10), a mínima quantidade desse gás que um japonês deve deixar de queimar para atender à meta diária,apenas com esse gesto, é de
Dados: CO2 (44 g/mol); C4H10 (58 g/mol)
- a) 0,25 kg.
- b) 0,33 kg.
- c) 1,0 kg.
- d) 1,3 kg.
- e) 3,0 kg.
B (ENEM 2012) Aspartame é um edulcorante artificial (adoçante dietético) que apresenta potencial adoçante 200 vezes maior que o açúcar comum, permitindo seu uso em pequenas quantidades. Muito usado pela indústria alimentícia, principalmente nos refrigerantes diet, tem valor energético que corresponde a 4 calorias/grama. É contraindicado a portadores de fenilcetonúria, uma doença genética rara que
provoca o acúmulo da fenilalanina no organismo, causando retardo mental. O IDA (índice diário aceitável) desse adoçante é 40 mg/kg de massa corpórea.
Disponível em: http://boaspraticasfarmaceuticas.blogspot.com. Acesso em: 27 fev. 2012
Com base nas informações do texto, a quantidade máxima recomendada de aspartame, em mol, que uma pessoa de 70 kg de massa corporal pode ingerir por dia é mais próxima de
Dado: massa molar do aspartame = 294 g/mol
- a) 1,3 × 10–4.
- b) 9,5 × 10–3.
- c) 4 × 10–2.
- d) 2,6.
- e) 823.
CAIU NO VESTIBULAR!
2019
D (FCMSCSP 2019) Em um experimento de laboratório, um grupo de alunos recebeu uma amostra de certo metal M para determinar o valor de
sua massa, sem o uso de balança, a partir de dados fornecidos pelo professor e de um dado obtido pelo próprio grupo, no laboratório.
A amostra recebida pelo grupo tinha massa igual a
- a) 54 g.
- b) 142 g.
- c) 178 g.
- d) 158 g.
- e) 226 g.
2018
- a) 213,7 g.
- b) 196,5 g.
- c) 512,8 g.
- d) 17,1 g.
A (FMABC 2018) Ácido ascórbico, mais conhecido como vitamina C, é um antioxidante. Para dosar essa substância, pode-se realizar uma titulação baseada na seguinte reação:
![]() Uma solução foi preparada dissolvendo-se um comprimido efervescente contendo 500 mg de ácido ascórbico em 200 mL de água. Na análise de 20,0 mL dessa solução, espera-se consumir uma massa de iodo de, aproximadamente,
Uma solução foi preparada dissolvendo-se um comprimido efervescente contendo 500 mg de ácido ascórbico em 200 mL de água. Na análise de 20,0 mL dessa solução, espera-se consumir uma massa de iodo de, aproximadamente,
- a) 7,2 × 10−2 g
- b) 1,2 × 10−3 g
- c) 1,2 × 10−1 g
- d) 7,2 × 10−1 g
- e) 1,2 × 10−2 g
B (UNESP 2018) O cloreto de cobalto(II) anidro, CoCl2, é um sal de cor azul, que pode ser utilizado como indicador de umidade, pois torna-se rosa em presença de água. Obtém-se esse sal pelo aquecimento do cloreto de cobalto(II) hexa-hidratado, CoCl2.6H2O, de cor rosa, com liberação de vapor de água.
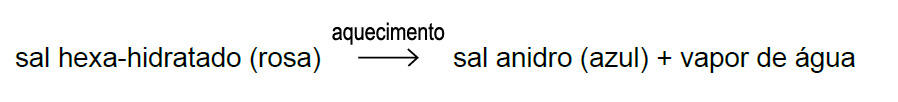 A massa de sal anidro obtida pela desidratação completa de 0,1 mol de sal hidratado é, aproximadamente,
A massa de sal anidro obtida pela desidratação completa de 0,1 mol de sal hidratado é, aproximadamente,
a) 11 g.
b) 13 g.
c) 24 g.
d) 130 g.
e) 240 g.
D (UNESP 2018) Bicarbonato de sódio sólido aquecido se decompõe, produzindo carbonato de sódio sólido, além de água e dióxido de carbono gasosos. O gráfico mostra os resultados de
um experimento em que foram determinadas as massas de carbonato de sódio obtidas pela decomposição de diferentes massas de bicarbonato de sódio.
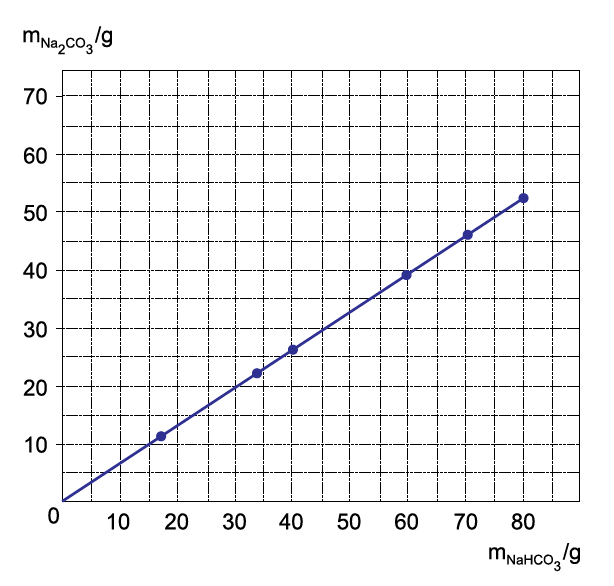
Os dados do gráfico permitem concluir que as massas de carbonato de sódio e bicarbonato de sódio nessa reação estão relacionadas pela equação
![]() e que o valor aproximado de k é
e que o valor aproximado de k é
- a) 0,3.
- b) 1,0.
- c) 0,2.
- d) 0,7.
- e) 1,2.
D (PUC PR 2018) O ácido nítrico fumegante é tão concentrado e reativo que propicia reações químicas pouco comuns como o fato de o hidrogênio ácido poder ser deslocado por um elemento nobre como o cobre.
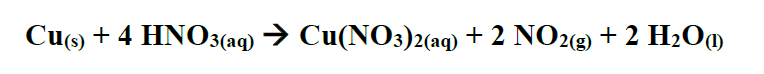 De acordo com a equação química apresentada, qual deve ser o volume aproximado, em litros, de gás formado nas CNTP, considerando que a amostra metálica de cobre de 200 g apresentava 18 % de impurezas em sua composição.
De acordo com a equação química apresentada, qual deve ser o volume aproximado, em litros, de gás formado nas CNTP, considerando que a amostra metálica de cobre de 200 g apresentava 18 % de impurezas em sua composição.
– Considere volume molar nas CNTP = 22,4 𝐿 .𝑚𝑜𝑙-1.
- a) 45 L
- b) 50 L
- c) 100 L
- d) 115 L
- e) 141 L
C (UPF 2018) Tendo por referência a reação química não balanceada
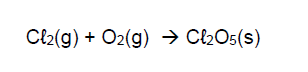 qual é o volume de oxigênio necessário para reagir com todo o cloro, considerando-se que se parte de 20 L de cloro gasoso medidos em condições ambientes de temperatura e pressão?
qual é o volume de oxigênio necessário para reagir com todo o cloro, considerando-se que se parte de 20 L de cloro gasoso medidos em condições ambientes de temperatura e pressão?
(Considere volume molar de 25 L mol-1 nas CATP)
- a) 20 L.
- b) 25 L.
- c) 50 L.
- d) 75 L.
- e) 100 L.
2017
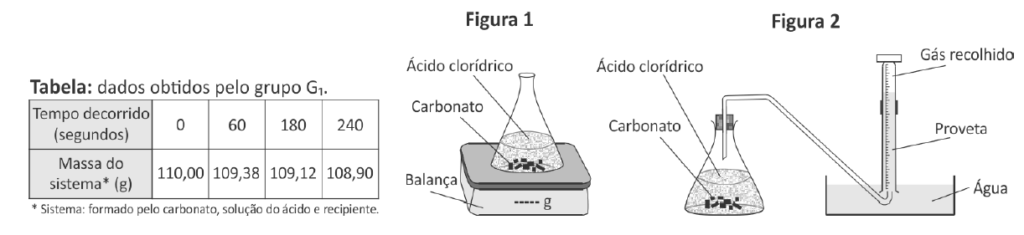
C (FUVEST 2017) Em uma aula experimental, dois grupos de alunos (G1 e G2) utilizaram dois procedimentos diferentes para estudar a velocidade da reação de carbonato de cálcio com excesso de ácido clorídrico. As condições de temperatura e pressão eram as mesmas nos dois procedimentos e, em cada um deles, os estudantes empregaram a mesma massa inicial de carbonato de cálcio e o mesmo volume de solução de ácido clorídrico de mesma concentração.
O grupo G1 acompanhou a transformação ao longo do tempo, realizada em um sistema aberto, determinando a variação de massa desse sistema (Figura 1 e Tabela).
O grupo G2 acompanhou essa reação ao longo do tempo, porém determinando o volume de dióxido de carbono recolhido (Figura 2).
Comparando os dois experimentos, os volumes aproximados de CO2, em litros, recolhidos pelo grupo G2 após 60, 180 e 240 segundos devem ter sido, respectivamente,
- a) 0,14; 0,20 e 0,25
- b) 0,14; 0,34 e 0,60
- c) 0,34; 0,48 e 0,60
- d) 0,34; 0,48 e 0,88
- e) 0,62; 0,88 e 1,10
D (FUVEST 2017) Nas mesmas condições de pressão e temperatura, 50 L de gás propano (C3H8) e 250 L de ar foram colocados em um reator, ao qual foi fornecida energia apenas suficiente para iniciar a reação de combustão. Após algum tempo, não mais se observou a liberação de calor, o que indicou que a reação havia-se encerrado.
Com base nessas observações experimentais, três afirmações foram feitas:
- Se tivesse ocorrido apenas combustão incompleta, restaria propano no reator.
- Para que todo o propano reagisse, considerando a combustão completa, seriam necessários, no mínimo, 750 L de ar.
- É provável que, nessa combustão, tenha se formado fuligem.
Está correto apenas o que se afirma em
- a) I.
- b) III.
- c) I e II.
- d) I e III.
- e) II e III.
D (MACKENZIE 2017) Na reação de neutralização, representada pela equação não balanceada, quando são misturados 444 g de Ca(OH)2 e 294 g de H3PO4 ,
- a) o hidróxido de cálcio encontra-se em excesso.
- b) são formados 162 g de água.
- c) a reação produz 465 g de fosfato de cálcio.
- d) permaneceram sem reagir 74 g de hidróxido de cálcio.
- e) o ácido fosfórico é o reagente limitante.
(CÁLCULO ESTEQUIOMÉTRICO FORA DAS CNTP) C (FGV SP 2017) O dióxido de carbono gerado pelos tripulantes na atmosfera artificial dos submarinos e estações espaciais deve ser removido do ar, e o oxigênio deve ser recuperado. Um dos possíveis métodos para realização desse processo envolve o uso do superóxido de potássio, KO2, de acordo com a reação:
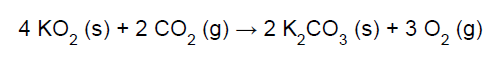 Em um processo a 27 °C e 1 atm, são produzidos 1 476 L de oxigênio. A quantidade de peróxido de potássio, em kg, mínima para esse processo é aproximadamente
Em um processo a 27 °C e 1 atm, são produzidos 1 476 L de oxigênio. A quantidade de peróxido de potássio, em kg, mínima para esse processo é aproximadamente
Adote: R = 0,082 atm. L. mol–1.K–1
- a) 1,4.
- b) 2,8.
- c) 5,7.
- d) 11,4.
- e) 14,8.
2016
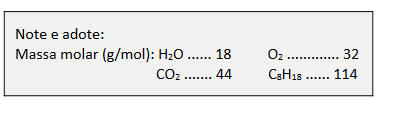
E (FUVEST 2016) Um dirigível experimental usa hélio como fluido ascensional e octano(C8H18) como combustível em seu motor, para propulsão. Suponha que, no motor, ocorra a combustão completa do octano:
Para compensar a perda de massa do dirigível à medida que o combustível é queimado, parte da água contida nos gases de exaustão do motor é condensada e armazenada como lastro. O restante do vapor de água e o gás carbônico são liberados para a atmosfera. Qual é a porcentagem aproximada da massa de vapor de água formado que deve ser retida para que a massa de combustível queimado seja compensada?
- a) 11%
- b) 16%
- c) 39%
- d) 50%
- e) 70%
D (MACKENZIE 2016) A reação entre o ferro e a solução de ácido clorídrico pode ser equacionada, sem o acerto dos coeficientes estequiométricos, por
![]() Em uma análise no laboratório, após essa reação, foram obtidos 0,002 mol de FeCl2. Considerando-se que o rendimento do processo seja de 80%, pode-se afirmar que reagiram
Em uma análise no laboratório, após essa reação, foram obtidos 0,002 mol de FeCl2. Considerando-se que o rendimento do processo seja de 80%, pode-se afirmar que reagiram
- a) 5,600·10–2 g de ferro.
- b) 1,460·10–1 g de ácido clorídrico.
- c) 1,680·10–1 g de ferro.
- d) 1,825·10–1 g de ácido clorídrico.
- e) 1,960·10–1 g de ferro.
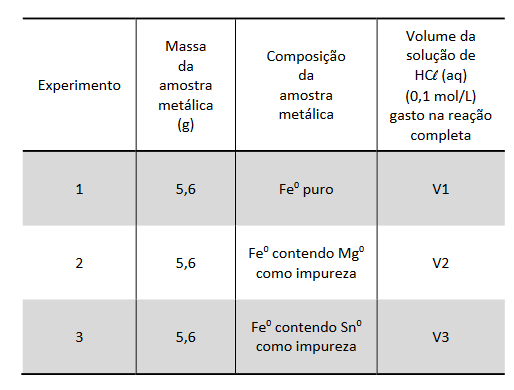
D (FUVEST 2016) Sabe-se que os metais ferro (Fe0), magnésio Mg0)e estanho (Sn0) reagem com soluções de ácidos minerais, liberando gás hidrogênio e formando íons divalentes em solução. Foram feitos três experimentos em que três amostras metálicas de mesma massa reagiram, separada e completamente, com uma solução aquosa de ácido clorídrico (HCl (aq)) de concentração 0,1 mol/L. Os resultados obtidos foram:
Colocando-se os valores de V1, V2 e V3 em ordem decrescente, obtém-se
- a) V2 > V3 > V1
- b) V3 > V1 > V2
- c) V1 > V3 > V2
- d) V2 > V1 > V3
- e) V1 > V2 > V3
 2015
2015
C (FUVEST 2015) Amônia e gás carbônico podem reagir formando ureia e água. O gráfico ao lado mostra as massas de ureia e de água que são produzidas em função da massa de amônia, considerando as reações completas. A partir dos dados do gráfico e dispondo-se de 270 g de amônia, a massa aproximada, em gramas, de gás carbônico minimamente necessária para reação completa com essa quantidade de amônia é
- a) 120
- b) 270
- c) 350
- d) 630
- e) 700
D (FUVEST 2015) Uma estudante de Química realizou o seguinte experimento: pesou um tubo de ensaio vazio, colocou nele um pouco de NaHCO3 (s) e pesou novamente. Em seguida, adicionou ao tubo de ensaio excesso de solução aquosa de HCl, o que provocou a reação química representada por:
![]() Após a reação ter-se completado, a estudante aqueceu o sistema cuidadosamente, até que restasse apenas um sólido seco no tubo de ensaio. Deixou o sistema resfriar até a temperatura ambiente e o pesou novamente. A estudante anotou os resultados desse experimento em seu caderno, juntamente com dados obtidos consultando um manual de Química:
Após a reação ter-se completado, a estudante aqueceu o sistema cuidadosamente, até que restasse apenas um sólido seco no tubo de ensaio. Deixou o sistema resfriar até a temperatura ambiente e o pesou novamente. A estudante anotou os resultados desse experimento em seu caderno, juntamente com dados obtidos consultando um manual de Química:
A estudante desejava determinar a massa de
- HCl que não reagiu;
- NaCl que se formou;
- CO2 que se formou.
Considerando as anotações feitas pela estudante, é possível determinar a massa de
- a) I, apenas.
- b) II, apenas.
- c) I e III, apenas.
- d) II e III, apenas.
- e) I, II e III.
2013
D (FUVEST 2013) Uma moeda antiga de cobre estava recoberta com uma camada de óxido de cobre (II). Para restaurar seu brilho original, a moeda foi aquecida ao mesmo tempo em que se passou sobre ela gás hidrogênio. Nesse processo, formou-se vapor de água e ocorreu a redução completa do cátion metálico.
As massas da moeda, antes e depois do processo descrito, eram, respectivamente, 0,795 g e 0,779 g. Assim sendo, a porcentagem em massa do óxido de cobre (II) presente na moeda, antes do processo de restauração, era
- a) 2%
- b) 4%
- c) 8%
- d) 10%
- e) 16%
 2011
2011
B (IFMG 2011) A amônia (NH3) tem uma ampla utilização no setor industrial, sendo consumida tanto na indústria de fertilizantes como na indústria da borracha, onde atua, por exemplo, na estabilização do látex natural e sintético. O processo de produção da amônia pode ser representado pela equação química abaixo: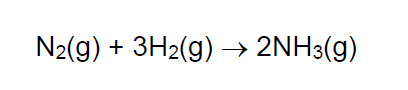 A massa em gramas de amônia produzida na reação de 2 mols de N2(g) com 15,0 g de H2(g) é:
A massa em gramas de amônia produzida na reação de 2 mols de N2(g) com 15,0 g de H2(g) é:
- a) 85,0
- b) 68,0
- c) 43,0
- d) 53,0