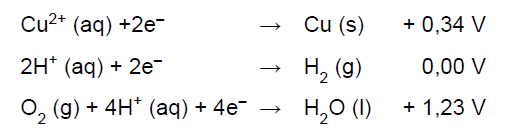QUÍMICA – LISTA DE EXERCÍCIOS SOBRE ELETRÓLISE
(ELETRÓLISE ÍGNEA/ELETRÓLISE AQUOSA/ESTEQUIOMETRIA DA ELETRÓLISE)
CAIU NO ENEM!
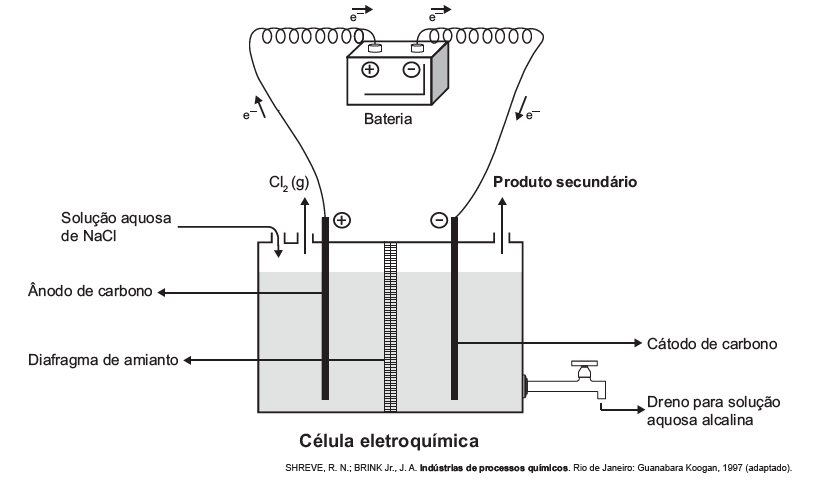
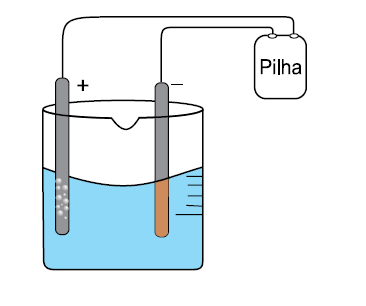
D (ENEM 2017) A eletrólise é um processo não espontâneo de grande importância para a indústria química. Uma de suas aplicações é a obtenção do gás cloro e do hidróxido de sódio, a partir de uma solução aquosa de cloreto de sódio. Nesse procedimento, utiliza-se uma célula eletroquímica, como ilustrado.
No processo eletrolítico ilustrado, o produto secundário obtido é o
- a) vapor de água.
- b) oxigênio molecular.
- c) hipoclorito de sódio.
- d) hidrogênio molecular.
- e) cloreto de hidrogênio.
E (ENEM 2016) A obtenção do alumínio dá-se a partir da bauxita (Al2O3 · 3H2O), que é purificada e eletrolisada numa temperatura de 1000 °C. Na célula eletrolítica, o ânodo é formado por barras de gráfica ou carvão, que são consumidas no processo de eletrólise, com formação de gás carbônico, e o cátodo é uma caixa de aço coberta de grafita.
A etapa de obtenção do alumínio ocorre no
- a) ânodo, com formação de gás carbônico.
- b) cátodo, com redução do carvão na caixa de aço.
- c) cátodo, com oxidação do alumínio na caixa de aço.
- d) ânodo, com depósito de alumínio nas barras de gráfica.
- e) cátodo, com o fluxo de elétrons das barras de grafita para a caixa de aço.
C (ENEM 2013) Eu também podia decompor a água, se fosse salgada ou acidulada, usando a pilha de Daniell como fonte de força. Lembro o prazer extraordinário que sentia ao decompor um pouco de água em uma taça para ovos quentes, vendo-a separar-se em seus elementos, o oxigênio em um eletrodo, o hidrogênio no outro. A eletricidade de uma pilha de 1 volt parecia tão fraca, e no entanto podia ser suficiente para desfazer um composto químico, a água…
SACKS, O. Tio Tungstênio: memórias de uma infância química. São Paulo: Cia. das Letras, 2002
O fragmento do romance de Oliver Sacks relata a separação dos elementos que compõem a água. O princípio do método apresentado é utilizado industrialmente na
- a) obtenção de ouro a partir de pepitas.
- b) obtenção de calcário a partir de rochas.
- c) obtenção de alumínio a partir da bauxita.
- d) obtenção de ferro a partir de seus óxidos.
- e) obtenção de amônia a partir de hidrogênio e nitrogênio.
D (ENEM 2010) A eletrólise é muito empregada na indústria com o objetivo de reaproveitar parte dos metais sucateados. O cobre, por exemplo, é um dos metais com maior rendimento no processo de eletrólise, com uma recuperação de aproximadamente 99,9%. Por ser um metal de alto valor comercial e de múltiplas aplicações, sua recuperação torna-se viável economicamente.
Suponha que, em um processo de recuperação de cobre puro, tenha-se eletrolisado uma solução de sulfato de cobre (II) (CuSO4) durante 3h, empregando-se uma corrente elétrica de intensidade igual a 10A. A massa de cobre puro recuperada é de aproximadamente
Dados: Constante de Faraday F = 96500C/mol; Massa molar em g/mol: Cu = 63,5
- a) 0,02 g
- b) 0,04 g
- c) 2,40 g
- d) 35,5 g
- e) 71,0 g
CAIU NO VESTIBULAR!
2018
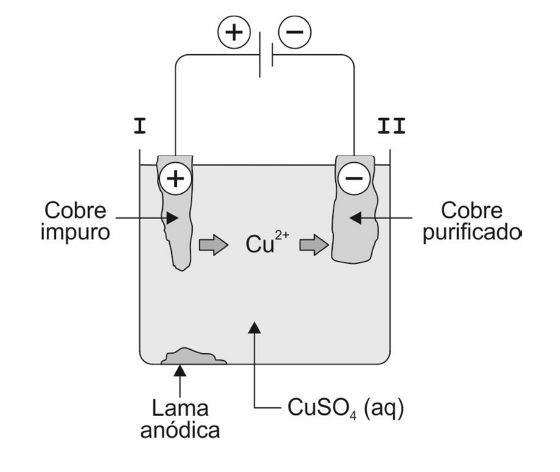
E (FMABC 2018) Considere o seguinte sistema utilizado na purificação de cobre metálico.
Nesse processo
- a) II representa o cátodo onde ocorre a oxidação.
- b) II representa o ânodo onde ocorre a redução.
- c) I representa o cátodo onde ocorre a oxidação.
- d) I representa o cátodo onde ocorre a redução.
- e) I representa o ânodo onde ocorre a oxidação.
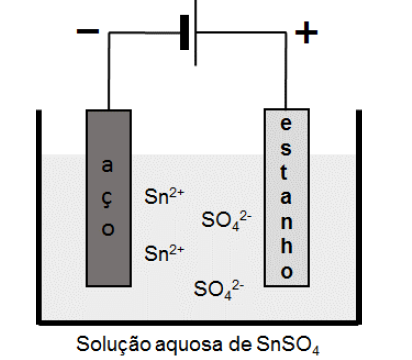
B (UNICAMP 2018) A galvanoplastia consiste em revestir um metal por outro a fim de protegê-lo contra a corrosão ou melhorar sua aparência. O estanho, por exemplo, é utilizado como revestimento do aço empregado em embalagens de alimentos. Na galvanoplastia, a espessura da camada pode ser controlada com a corrente elétrica e o tempo empregados. A figura abaixo é uma representação esquemática desse processo.
Considerando a aplicação de uma corrente constante com intensidade igual a 9,65 x 10-3 A, a massa depositada de estanho após 1 min 40 s será de aproximadamente
Dados: 1 mol de elétrons corresponde a uma carga de 96.500 C; Sn: 119 g∙mol-1.
- a) 0,6 mg e ocorre, no processo, a transformação de energia química em energia elétrica.
- b) 0,6 mg e ocorre, no processo, a transformação de energia elétrica em energia química.
- c) 1,2 mg e ocorre, no processo, a transformação de energia elétrica em energia química.
- d) 1,2 mg e ocorre, no processo, a transformação de energia química em energia elétrica.
D (MACKENZIE 2018) De acordo com os conceitos de eletroquímica, é correto afirmar que
- a) a ponte salina é a responsável pela condução de elétrons durante o funcionamento de uma pilha.
- b) na pilha representada por Zn(s) /Zn2+(aq )//Cu2+(aq )/Cu(s), o metal zinco representa o cátodo da pilha.
- c) o resultado positivo da ddp de uma pilha, por exemplo, +1,10 V, indica a sua não espontaneidade, pois essa pilha está absorvendo energia do meio.
- d) na eletrólise o ânodo é o polo positivo, onde ocorre o processo de oxidação.
- e) a eletrólise ígnea só ocorre quando os compostos iônicos estiverem em meio aquoso.
2017
B (FUVEST 2017) Células a combustível são opções viáveis para gerar energia elétrica para motores e outros dispositivos. O esquema representa uma dessas células e as transformações que nela ocorrem.
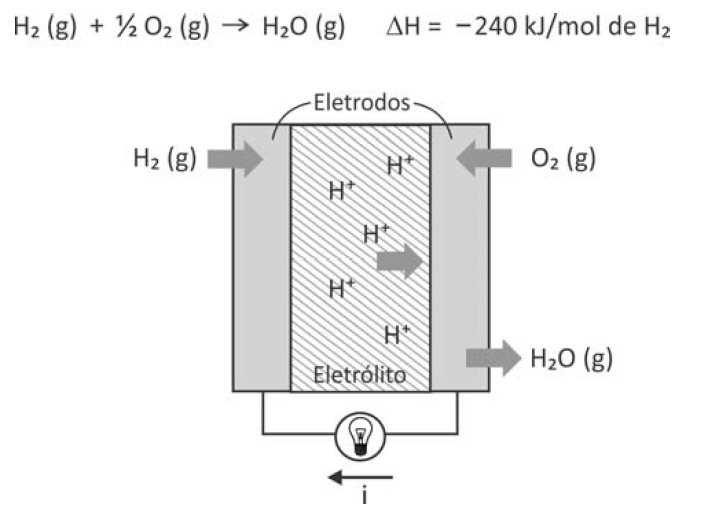 A corrente elétrica (i), em ampère (coulomb por segundo), gerada por uma célula a combustível que opera por 10 minutos e libera 4,80 kJ de energia durante esse período de tempo, é
A corrente elétrica (i), em ampère (coulomb por segundo), gerada por uma célula a combustível que opera por 10 minutos e libera 4,80 kJ de energia durante esse período de tempo, é
- a) 3,32.
- b) 6,43.
- c) 12,9.
- d) 386.
- e) 772.
A (MACKENZIE 2017) Um dos modos de se produzirem gás hidrogênio e gás oxigênio em laboratório é promover a eletrólise (decomposição pela ação da corrente elétrica) da água, na presença de sulfato de sódio ou ácido sulfúrico. Nesse processo, usando para tal um recipiente fechado, migram para o cátodo (polo negativo) e ânodo (polo positivo), respectivamente, H2 e O2. Considerando-se que as quantidades de ambos os gases são totalmente recolhidas em recipientes adequados, sob mesmas condições de temperatura e pressão, é correto afirmar que
Dados: massas molares (g·mol-1) H = 1 e O = 16.
- a) o volume de H2(g) formado, nesse processo, é maior do que o volume de O2(g).
- b) serão formados 2 mols de gases para cada mol de água decomposto.
- c) as massas de ambos os gases formados são iguais no final do processo.
- d) o volume de H2(g) formado é o quádruplo do volume de O2(g) formado.
- e) a massa de O2(g) formado é o quádruplo da massa de H2(g) formado.
A (UFPR 2017) A bauxita, constituída por uma mistura de óxidos, principalmente de alumínio (Al2O3) e ferro (Fe2O3 e Fe(OH)3), é o principal minério utilizado para a produção de alumínio. Na purificação pelo processo Bayer, aproximadamente 3 toneladas de resíduo a ser descartado (lama vermelha) são produzidas a partir de 5 toneladas do minério. Com a alumina purificada, alumínio metálico é produzido por eletrólise ígnea.
Dados – M (g mol-1): O = 16; Al = 27; Fe = 56.
A partir de 5 toneladas de minério, a quantidade (em toneladas) de alumínio metálico produzida por eletrólise ígnea é mais próxima de:
- a) 1.
- b) 0,5.
- c) 0,2.
- d) 0,1.
- e) 0,05.
2016
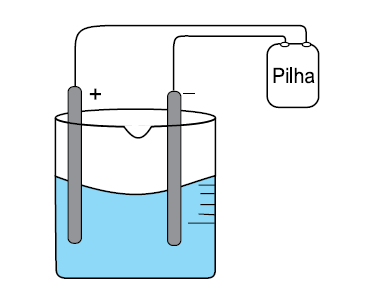
A (FGV SP 2016) Em um experimento em laboratório de química, montou-se uma célula eletrolítica de acordo com o esquema:
Usaram-se como eletrodo dois bastões de grafite, uma solução aquosa 1,0 mol.L–1 de CuSO4 em meio ácido a 20 °C e uma pilha.
Alguns minutos, após iniciado o experimento, observaram-se a formação de um sólido de coloração amarronzada sobre a superfície do eletrodo de polo negativo e a formação de bolhas na superfície do eletrodo de polo positivo.
Com base nos potenciais de redução a 20 °C,
É correto afirmar que se forma cobre no
- a) catodo; no anodo, forma-se O2.
- b) catodo; no anodo, forma-se H2O.
- c) anodo; no catodo, forma-se H2.
- d) anodo; no catodo, forma-se O2.
- e) anodo; no catodo, forma-se H2O.
2013
D (UERN 2013) Um brinquedo, movido a pilha, fica ligado durante 1,5 hora até ser desligado. Sabe-se que a pilha é recarregável e o seu metal é o magnésio, que possui uma corrente de 10800 mA. Qual foi o desgaste aproximado de magnésio nesse período?
- a) 17,8 g.
- b) 14,2 g.
- c) 8,9 g.
- d) 7,3 g.