QUÍMICA – LISTA DE EXERCÍCIOS SOBRE LIGAÇÕES QUÍMICAS
(TEORIA DO OCTETO/LIGAÇÃO IÔNICA/LIGAÇÃO COVALENTE/LIGAÇÃO METÁLICA)
CAIU NO ENEM!
CAIU NO VESTIBULAR!
2018
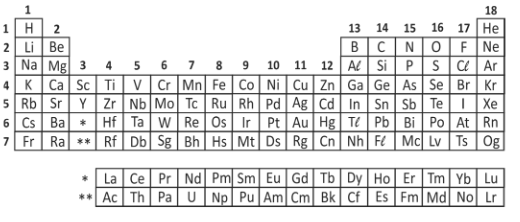
C (FUVEST 2018) Analise a tabela periódica e as seguintes afirmações a respeito do elemento químico enxofre (S):
- Tem massa atômica maior do que a do selênio (Se).
- Pode formar com o hidrogênio um composto molecular de fórmula H2S.
- A energia necessária para remover um elétron da camada mais externa do enxofre é maior do que para o sódio (Na).
- Pode formar com o sódio (Na) um composto iônico de fórmula Na3S.
São corretas apenas as afirmações
- a) I e II.
- b) I e III.
- c) II e III.
- d) II e IV.
- e) III e IV
B (MACKENZIE 2018) Assinale (V) para verdadeiro e (F) para falso, para as afirmações abaixo.
( ) Os metais apresentam alta condutividade elétrica, mas baixa condutividade térmica.
( ) O bronze é uma liga formada por cobre e estanho.
( ) Compostos iônicos conduzem corrente elétrica em meio aquoso e quando fundidos.
( ) A ligação covalente ocorre entre metais e não metais. O KBr é um exemplo.
( ) O dióxido de carbono é uma molécula apolar, mas que possui ligações covalentes polares.
A sequência correta de preenchimento dos parênteses, de cima para baixo é
- a) F, F, V, F e V.
- b) F, V, V, F e V.
- c) V, F, V, F e V.
- d) F, F, V, F e F.
- e) V, V, F, V e F.
C (UNESP 2018) Dos extensos efeitos nocivos que a radiação ionizante provoca na matéria viva, afigura-se a geração de radicais livres, que são espécies químicas eletricamente neutras que apresentam um ou mais elétrons desemparelhados na camada de valência. O íon cloreto, por exemplo, que, quantitativamente, constitui o principal ânion do plasma, transforma-se no radical livre Cl●, com 7 elétrons na camada de valência, podendo, assim, reagir facilmente com as biomoléculas, alterando o comportamento bioquímico de muitas proteínas solúveis do meio sanguíneo e também os constituintes membranários de células: hemácias, leucócitos, plaquetas.
(José Luiz Signorini e Sérgio Luís Signorini.
Atividade física e radicais livres, 1993. Adaptado.)
Ao transformar-se em radical livre, o ânion cloreto
- a) ganha 1 próton.
- b) ganha 1 elétron.
- c) perde 1 elétron.
- d) perde 1 nêutron.
- e) ganha 1 nêutron.
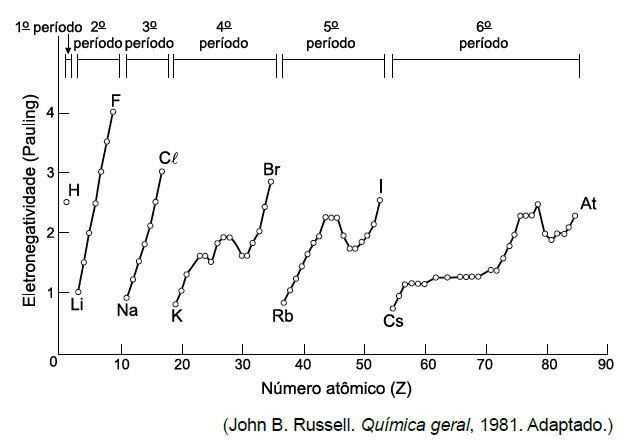
C (UNESP 2018) Analise o gráfico que mostra a variação da eletronegatividade em função do número atômico.
Devem unir-se entre si por ligação iônica os elementos de números atômicos
- a) 17 e 35.
- b) 69 e 70.
- c) 17 e 57.
- d) 15 e 16.
- e) 12 e 20.
DICA! CONSULTE A TABELA PERIÓDICA
A (UFJF – PISM 1 2018) Analise as observações a seguir relativas a um determinado elemento químico que possui 2 elétrons na camada K e assinale a opção CORRETA:
- a) O elemento apresenta 2 prótons e 2 elétrons.
- b) O elemento apresenta o mesmo número de elétrons na camada de valência que os outros elementos do mesmo grupo da Tabela Periódica.
- c) No período onde se situa o elemento em questão estão presentes sete outros.
- d) Ao formar ligações químicas, o elemento segue a regra do octeto.
- e) O elemento apresenta 4 nêutrons em seu núcleo.
2017
E (MACKENZIE 2017) Em dezembro de 2016, a IUPAC (International Union of Pure and Applied Chemistry) oficializou a nomenclatura dos novos elementos químicos, presentes no sétimo período da tabela periódica. Assim, os elementos 113 (grupo 13), 115 (grupo 15), 117 (grupo 17) e 118 (grupo 18) passaram a ser denominados, respectivamente, de Nihonium (Nh), Moscovium (Mc), Tennessine (Ts) e Oganesson (Og). Pode-se afirmar que o elemento
Dado: Número atômico (Z): O = 8
- a) Nh forma o íon Nh3-.
- b) Mc é um metal de transição.
- c) Ts é um elemento representativo e pertence ao mesmo grupo do oxigênio.
- d) Og é um gás nobre e apresenta configuração da camada de valência 6s2 6p2.
- e) Nh pode combinar-se com um halogênio (X), formando o composto hipotético NhX3.
B (MACKENZIE 2017) Assinale a alternativa que apresenta compostos químicos que possuam geometria molecular, respectivamente, linear, trigonal plana e piramidal.
Dados: número atômico (Z) H = 1, C = 6, N = 7, O = 8, F = 9 e S = 16.
- a) H2O, SO3 e CH4.
- b) CO2, SO3 e NH3.
- c) CH4, SO2 e HF.
- d) CO2, SO2 e NH3.
- e) H2O, SO2 e HF.
D (MACKENZIE 2017) Assinale a alternativa que apresenta compostos químicos que possuam, respectivamente, ligação covalente polar, ligação covalente apolar e ligação iônica.
- a) H2O, CO2 e NaCl.
- b) CCl4, O3 e HBr.
- c) CH4, SO2 e HI.
- d) CO2, O2 e KCl.
- e) H2O, H2 e HCl.
A (UFJF – PISM 1 2017) O selênio quando combinado com enxofre forma o sulfeto de selênio, substância que apresenta propriedades antifúngicas e está presente na composição de xampus anticaspa. Qual o tipo de ligação química existente entre os átomos de enxofre e selênio?
- a) Covalente.
- b) Dipolo-dipolo.
- c) Força de London.
- d) Iônica.
- e) Metálica.
2016
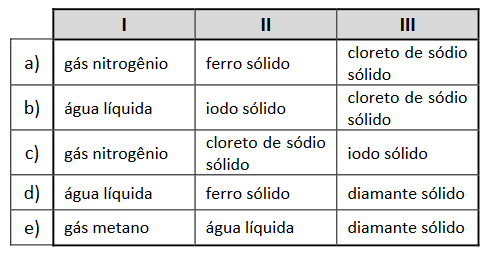
A (FUVEST 2016) Existem vários modelos para explicar as diferentes propriedades das substâncias químicas, em termos de suas estruturas submicroscópicas. Considere os seguintes modelos:
- moléculas se movendo livremente;
- íons positivos imersos em um “mar” de elétrons deslocalizados;
- íons positivos e negativos formando uma grande rede cristalina tridimensional.
Assinale a alternativa que apresenta substâncias que exemplificam, respectivamente, cada um desses modelos.
2015
B (UFJF – PISM 1 2015) O óxido nitroso (N2O(g)), também conhecido como gás hilariante, foi o primeiro anestésico utilizado em cirurgias. Hoje, também pode ser utilizado na indústria automobilística para aumentar a potência de motores de combustão interna. Abaixo, está representada uma possibilidade da estrutura de Lewis dessa molécula.
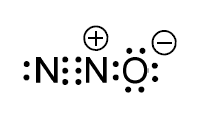 De acordo com a fórmula apresentada, marque a opção que descreve CORRETAMENTE as ligações existentes no N2O.
De acordo com a fórmula apresentada, marque a opção que descreve CORRETAMENTE as ligações existentes no N2O.
- a) Uma ligação iônica e duas ligações covalentes simples.
- b) Duas ligações covalentes, sendo uma tripla e uma simples.
- c) Duas ligações covalentes simples.
- d) Duas ligações iônicas.
- e) Duas ligações covalentes, sendo uma dupla e uma simples.
2013
D (UFJF – PISM 1 2013) Considere os elementos com número atômico Z = 17 e Z = 19 e as afirmações abaixo:
I) Quando ocorre uma reação entre os elementos com Z = 17 e Z = 19, a ligação química formada é uma ligação predominantemente covalente.
II) Através da estrutura eletrônica dos dois elementos, observa-se que os elétrons de valência ocupam a camada M e N, respectivamente.
III) Numa ligação química, o elemento com Z = 17 tem grande tendência a atrair um elétron do átomo ligado a ele.
IV) Quando o elemento com Z = 19 forma uma ligação química e doa um elétron, ele apresenta número de oxidação +1 e passa a possuir o número atômico Z = 18.
Assinale a alternativa CORRETA.
- a) Apenas a afirmação I está correta.
- b) Apenas as afirmações I e II estão corretas.
- c) Apenas a afirmação II está correta.
- d) Apenas as afirmações II e III estão corretas.
- e) Apenas a afirmação IV está correta.
2011
A (IFSP 2011) Nas condições do ambiente, apresentam átomos isolados, isto é, não unidos a outros átomos, os seguintes elementos químicos
- a) argônio e neônio (gases nobres).
- b) enxofre e oxigênio (calcogênios).
- c) sódio e potássio (metais alcalinos).
- d) magnésio e cálcio (metais alcalino-terrosos).
- e) cloro e bromo (halogênios).
B (COLÉGIO NAVAL 2011) Os átomos de certo elemento são constituídos cada um de 38 prótons, 50 nêutrons e 38 elétrons. Assinale a opção que apresenta os valores corretos de número atômico e número de massa, respectivamente, e do tipo de íon que ele é capaz de formar para atingir a estabilidade.
- a) 38 e 50; cátion monovalente.
- b) 38 e 88; cátion bivalente.
- c) 50 e 88; ânion monovalente.
- d) 76 e 50; ânion bivalente.
- e) 76 e 88; ânion trivalente.
2010
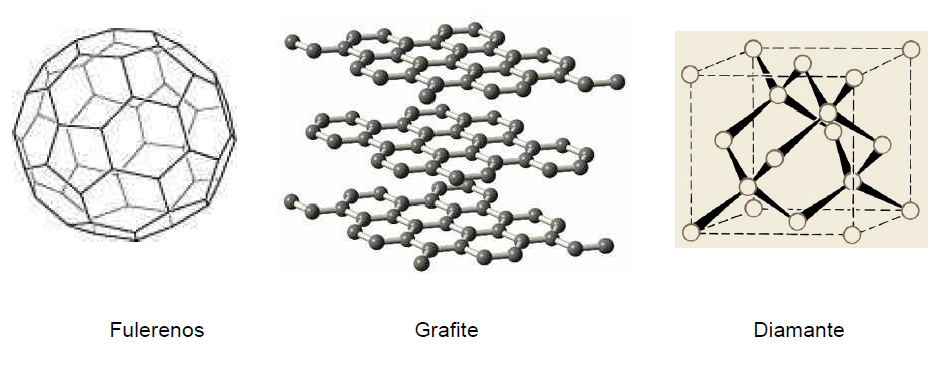
B (UFU 2010) Observe as representações a seguir e assinale a alternativa correta.
- a) As figuras mostram substâncias que possuem as mesmas propriedades físicas e químicas.
- b) As figuras representam formas alotrópicas do carbono, sendo que a estrutura dos fulerenos acima pode ser comparada a uma bola de futebol.
- c) As representações indicam que a ligação química entre os átomos de carbono − presentes nos fulerenos, diamante e grafite − é do tipo iônica.
- d) As substâncias representadas nas figuras podem ser classificadas como compostas, pois, por reações químicas, formam outras mais simples.
2008
C (PUC MG 2008) Z e X são elementos químicos que apresentam respectivamente 2 e 6 elétrons no nível de valência. A fórmula química resultante da combinação entre átomos dos elementos Z e X e o tipo de ligação que ocorre entre eles são, respectivamente:
- a) Z2X, iônica.
- b) ZX2, covalente.
- c) ZX, iônica .
- d) ZX, covalente.
A (PUC MG 2008) O elemento bromo forma compostos iônicos e moleculares. Assinale a alternativa que apresenta, respectivamente, um composto iônico e um molecular formado pelo bromo.
- a) CaBr2 e HBr
- b) CBr4 e KBr
- c) NaBr e MgBr2
- d) KBr e NH4Br