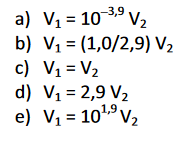CAIU NO ENEM!
CAIU NO VESTIBULAR!
2019
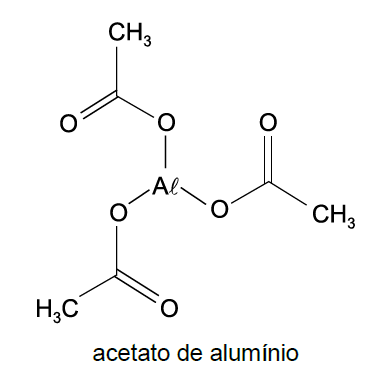
A (FCMSCSP 2019) O líquido de Bürow, com formulação descrita na farmacopeia brasileira, é utilizado como adstringente e antisséptico em
dermatites agudas e no alívio de queimaduras da pele. Esta formulação contém acetato de alumínio dissolvido em água purificada em quantidade suficiente para 100 mL de solução com densidade 1 g/mL.
Sabendo que a formulação descrita contém 0,025 mol de alumínio, o líquido de Bürow tem teor percentual, em massa, de acetato de alumínio próximo de
- a) 5%.
- b) 7%.
- c) 3%.
- d) 8%.
- e) 10%.
D (FCMSCSP 2019) Algumas pesquisas estudam o uso do cloreto de amônio na medicina veterinária para a prevenção da urolitíase em ovinos,
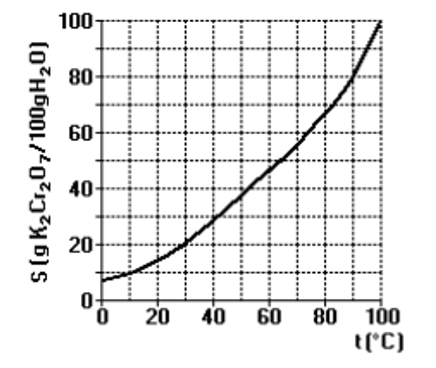
doença associada à formação de cálculos no sistema urinário. O cloreto de amônio (massa molar = 53,5 g/mol) é um sólido cristalino que apresenta a seguinte curva de solubilidade:
Uma solução aquosa saturada de cloreto de amônio a 90 °C, com massa total de 1 360 g, foi resfriada para 50 °C. Uma segunda solução aquosa com volume total de 1 000 mL foi preparada com o sólido obtido da cristalização da primeira solução.
Considerando que a cristalização foi completa no resfriamento realizado, a segunda solução aquosa de cloreto de amônio tem concentração próxima de
- a) 1,5 mol/L.
- b) 2,5 mol/L.
- c) 2,0 mol/L.
- d) 3,0 mol/L.
- e) 1,0 mol/L.
2018
B (FUVEST 2018) Um dos parâmetros que determina a qualidade do azeite de oliva é sua acidez, normalmente expressa na embalagem na forma de porcentagem, e que pode ser associada diretamente ao teor de ácido oleico em sua composição.
Uma amostra de 20,00 g de um azeite comercial foi adicionada a 100 mL de uma solução contendo etanol e etoxietano (dietiléter), 1:1 em volume, com o indicador fenolftaleína. Sob constante agitação, titulou se com uma solução etanólica contendo KOH 0,020 mol/L até a total. Para essa amostra, usaram se 35,0 mL de base, o que permite concluir que se trata de um azeite tipo .
As palavras que completam corretamente as lacunas são:
- a) oxidação; semifino.
- b) neutralização; virgem fino.
- c) oxidação, virgem fino.
- d) neutralização; extra virgem.
- e) neutralização, semifino.
(DILUIÇÃO) D (MACKENZIE 2018) Em uma embalagem de 2 L de água sanitária, facilmente encontrada em supermercados, encontra-se a seguinte informação:
- Há de 20 a 25 g de cloro ativo por litro dessa solução comercial.
- Na piscina A, a solução formada após a diluição seria irritante aos olhos do usuário dessa piscina.
- Na piscina B, a solução formada após a diluição seria adequada ao tratamento de água.
- a) nenhuma é correta.
- b) são corretas, apenas, I e II.
- c) são corretas, apenas, II e III.
- d) são corretas, apenas, I e III.
- e) todas são corretas.
(CONCENTRAÇÃO DAS SOLUÇÕES) C (UNESP 2018) De acordo com o Relatório Anual de 2016 da Qualidade da Água, publicado pela Sabesp, a concentração de cloro na água potável da rede de distribuição deve estar entre 0,2 mg/L, limite mínimo, e 5,0 mg/L, limite máximo. Considerando que a densidade da água potável seja igual à da água pura, calcula-se que o valor médio desses limites, expresso em partes por milhão, seja
- a) 5,2 ppm.
- b) 18 ppm.
- c) 2,6 ppm.
- d) 26 ppm.
- e) 1,8 ppm.
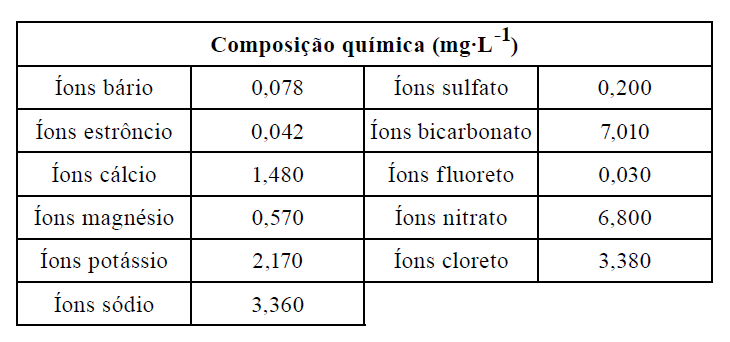
(CONCENTRAÇÃO DAS SOLUÇÕES) D (PUC PR 2018) A tabela apresentada a seguir indica a concentração de muitos íons minerais que compõem águas engarrafadas que fazem parte de nosso cotidiano.
Considerando as informações apresentadas, qual é a concentração em mmol/L do único ânion oxigenado apresentado na tabela?
- a) 0,16
- b) 0,26
- c) 1,6
- d) 2,6
- e) 26
D (FCMSCSP 2018) Uma indústria de galvanoplastia tinha 100 L de um efluente de ácido sulfúrico (H2SO4) 0,01 mol · L–1. Para o tratamento desse efluente, o operador de processos químicos utilizou uma das soluções relacionadas na tabela.
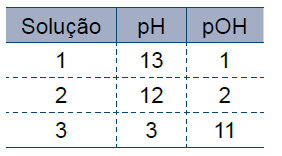 Para neutralizar completamente esse efluente foram utilizados
Para neutralizar completamente esse efluente foram utilizados
- a) 100 L da solução 2.
- b) 10 L da solução 1.
- c) 200 L da solução 1.
- d) 200 L da solução 2.
- e) 100 L da solução 3.
(DILUIÇÃO) E (FMABC 2018) Próteses de acrílico podem ser desinfetadas em ambiente odontológico por imersão em solução de hipoclorito de sódio a 1% (m/V) por 10 minutos. Partindo de uma solução a 5% (m/V) de hipoclorito de sódio, o preparo de 1,0 L de solução a 1% (m/V) requer a tomada de
- a) 500 mL da solução mais concentrada, adicionando-se água até completar o volume desejado.
- b) 100 mL da solução mais concentrada e adicionar 900 mL de água.
- c) 500 mL da solução mais concentrada e adicionar 500 mL de água.
- d) 100 mL da solução mais concentrada, adicionando-se água até completar o volume desejado.
- e) 200 mL da solução mais concentrada, adicionando-se água até completar o volume desejado.
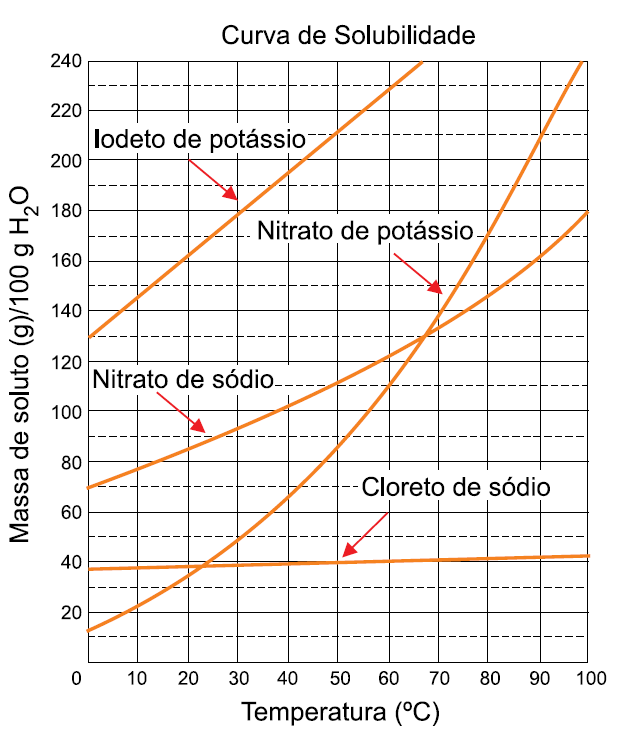
(SOLUBILIDADE) E (FGV SP 2018) Foram preparadas quatro soluções aquosas saturadas a 60 oC, contendo cada uma delas 100 g de água e um dos sais: iodeto de potássio, KI, nitrato de potássio, KNO3, nitrato de sódio, NaNO3, e cloreto de sódio, NaCl. Na figura, são representadas as curvas de solubilidade desses sais:
Em seguida, essas soluções foram resfriadas até 20 °C, e o sal cristalizado depositou-se no fundo de cada recipiente. Considerando-se que a cristalização foi completa, a maior e
a menor massa de sal cristalizado correspondem, respectivamente, aos sais
- a) KI e NaCl.
- b) KI e KNO3.
- c) NaNO3 e NaCl.
- d) KNO3 e NaNO3.
- e) KNO3 e NaCl.
(CONCENTRAÇÃO DAS SOLUÇÕES) E (FGV SP 2018) Uma resolução do Ministério da Saúde do Brasil regulamenta que o limite máximo da quantidade de ácido fosfórico, H3PO4, em bebidas refrigerantes é 0,07 g/100 mL. De acordo com essa regulamentação, a concentração máxima de ácido fosfórico, em mol/L, nos refrigerantes é, aproximadamente,
- a) 7 x 10+2.
- b) 7 x 10+1.
- c) 7 x 10–1.
- d) 7 x 10–2
- e) 7 x 10–3.
2017
 Analisando os valores tabelados, assinale a alternativa que representa corretamente a fórmula dos cátions e ânions, respectivamente, que se encontram em maior quantidade em mols, em 1 L dessa água mineral.
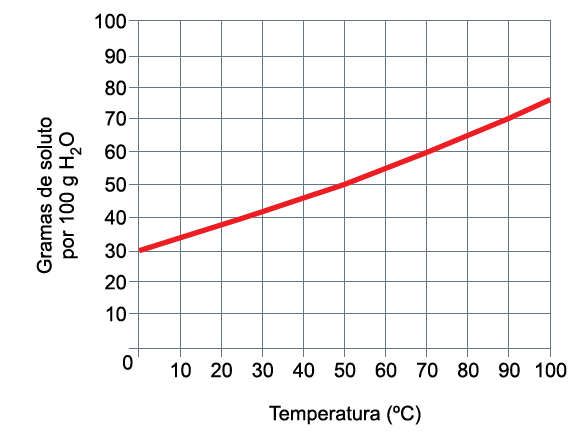
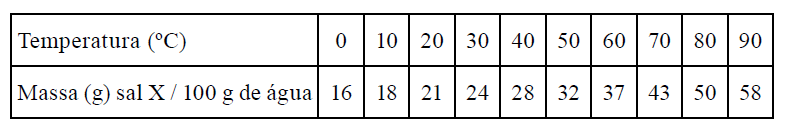
Analisando os valores tabelados, assinale a alternativa que representa corretamente a fórmula dos cátions e ânions, respectivamente, que se encontram em maior quantidade em mols, em 1 L dessa água mineral.- A solubilização do sal X, em água, é exotérmica.
- Ao preparar-se uma solução saturada do sal X, a 60 ºC, em 200 g de água e resfriá-la, sob agitação até 10 ºC, serão precipitados 19 g desse sal.
- Uma solução contendo 90 g de sal e 300 g de água, a 50 ºC, apresentará precipitado.
- a) nenhuma das afirmativas está certa.
- b) apenas a afirmativa II está certa.
- c) apenas as afirmativas II e III estão certas.
- d) apenas as afirmativas I e III estão certas.
- e) todas as afirmativas estão certas.
2016
(SOLUBILIDADE) D (FGV SP 2016) O nitrito de sódio, NaNO2, é um conservante de alimentos processados a partir de carnes e peixes. Os dados de solubilidade deste sal em água são apresentados na tabela.
 Em um frigorífico, preparou-se uma solução saturada de NaNO2 em um tanque contendo 0,5 m3 de água a 50 oC. Em seguida, a solução foi resfriada para 20 °C e mantida nessa
Em um frigorífico, preparou-se uma solução saturada de NaNO2 em um tanque contendo 0,5 m3 de água a 50 oC. Em seguida, a solução foi resfriada para 20 °C e mantida nessa
temperatura. A massa de NaNO2, em kg, cristalizada após o resfriamento da solução, é
Considere: Densidade da água = 1 g/mL
- a) 10.
- b) 20.
- c) 50.
- d) 100.
- e) 200.
2015
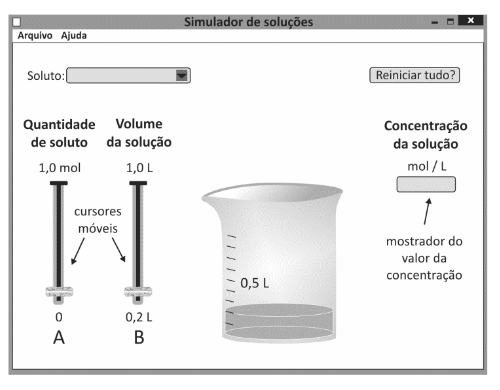
(CONCENTRAÇÃO DAS SOLUÇÕES) D (FUVEST 2015) Um estudante utilizou um programa de computador para testar seus conhecimentos sobre concentração de soluções. No programa de simulação, ele deveria escolher um soluto para dissolver em água, a quantidade desse soluto, em mol, e o volume da solução. Uma vez escolhidos os valores desses parâmetros, o programa apresenta, em um mostrador, a concentração da solução. A tela inicial do simulador é mostrada a seguir.
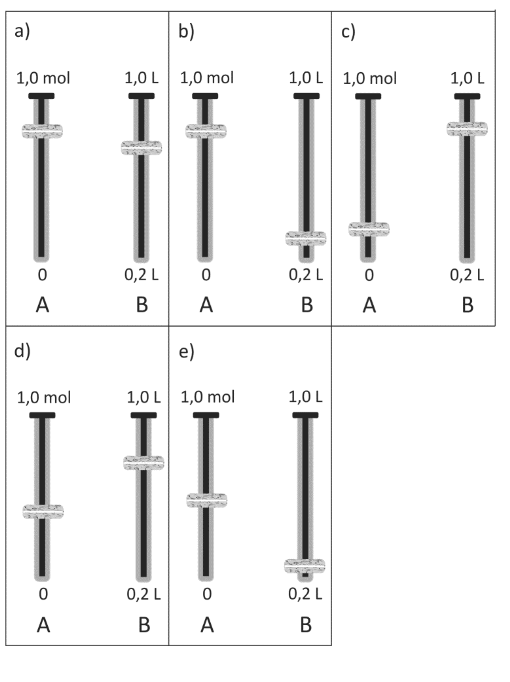
O estudante escolheu um soluto e moveu os cursores A e B até que o mostrador de concentração indicasse o valor 0,50 mol/L. Quando esse valor foi atingido, os cursores A e B poderiam estar como mostrado em
(TITULAÇÃO) C (FUVEST 2015) Soluções aquosas de ácido clorídrico, HCl (aq), e de ácido acético, H3CCOOH (aq), ambas de concentração 0,10 mol/L, apresentam valores de pH iguais a 1,0 e 2,9, respectivamente. Em experimentos separados, volumes iguais de cada uma dessas soluções foram titulados com uma solução aquosa de hidróxido de sódio, NaOH (aq), de concentração adequada. Nessas titulações, a solução de NaOH foi adicionada lentamente ao recipiente contendo a solução ácida, até reação completa. Sejam V1 o volume da solução de NaOH para reação completa com a solução de HCl e V2 o volume da solução de NaOH para reação completa com a solução de H3CCOOH. A relação entre V1 e V2 é
2014
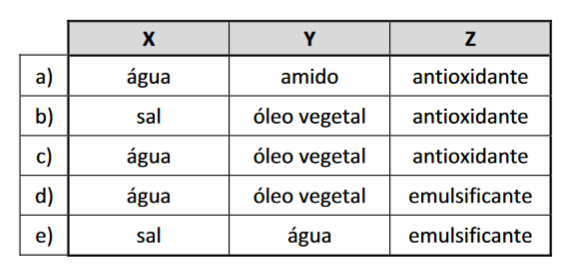
(COLOIDES) D (FUVEST 2014) Uma embalagem de sopa instantânea apresenta, entre outras, as seguintes informações: “Ingredientes: tomate, sal, amido, óleo vegetal, emulsificante, conservante, flavorizante, corante, antioxidante”. Ao se misturar o conteúdo da embalagem com água quente, poderia ocorrer a separação dos componentes X e Y da mistura, formando duas fases, caso o ingrediente Z não estivesse presente. Assinale a alternativa em que X, Y e Z estão corretamente identificados.
2013
B (FUVEST 2013) A porcentagem em massa de sais no sangue é de aproximadamente 0,9%. Em um experimento, alguns glóbulos vermelhos de uma amostra de sangue foram coletados e separados em três grupos. Foram preparadas três soluções, identificadas por X, Y e Z, cada qual com uma diferente concentração salina. A cada uma dessas soluções foi adicionado um grupo de glóbulos vermelhos. Para cada solução, acompanhou-se, ao longo do tempo, o volume de um glóbulo vermelho, como mostra o gráfico.
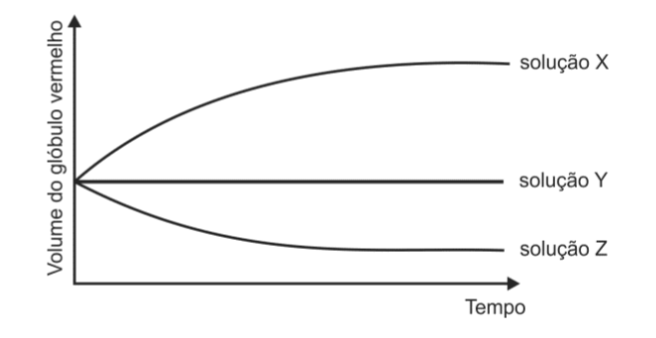 Com base nos resultados desse experimento, é correto afirmar que
Com base nos resultados desse experimento, é correto afirmar que
- a) a porcentagem em massa de sal, na solução Z, é menor do que 0,9%.
- b) a porcentagem em massa de sal é maior na solução Y do que na solução X.
- c) a solução Y e a água destilada são isotônicas.
- d) a solução X e o sangue são isotônicos.
- e) a adição de mais sal à solução Z fará com que ela e a solução X fiquem isotônicas.
2010
C (UFJF – PISM 2 2010) O Tamiflu (C16H28N2O4), medicamento utilizado no tratamento da gripe H1N1, pode ser distribuído na forma de cápsulas cuja massa total é 98,5 mg. Ao se dissolver totalmente o conteúdo dessa cápsula em 7,5 mL de água, a concentração da solução formada pelo princípio ativo é igual a 10 mg/mL. A percentagem em massa aproximada do princípio ativo na cápsula é:
- a) 44 %
- b) 65 %
- c) 76 %
- d) 87 %
- e) 99 %
2008
(CONCENTRAÇÃO DAS SOLUÇÕES) C (UFMS 2008) A cana-de-açúcar é atualmente, para o Brasil, uma das culturas mais promissoras. Além de fonte renovável para obtenção de combustível, é utilizada na obtenção de açúcar e, mais recentemente, tem sido utilizada como matéria-prima para a chamada indústria alcoolquímica. O etanol, combustível que tem sido exportado para vários países, é um liquido volátil, de densidade igual a 0,8 g/cm3. O número de moléculas de etanol (CH3CH2OH), contidas em 500 mL dessa substância, é igual a
(Número de Avogadro: 6 x 1023; massa molar, em g/mol: C=12; H=1; O=16).
- a) 6,0 × 1023
- b) 1,0 × 1025
- c) 5,2 × 1024
- d) 3,5 × 1025
- e) 2,8 × 1022
(CONCENTRAÇÃO DAS SOLUÇÕES) C (UFCSPA 2008) Ácido cítrico (C6H8O7), utilizado como acidulante, flavorizante e conservante, foi adicionado a um refrigerante numa concentração de 0,01 % em massa. Supondo que a densidade do refrigerante seja igual a 1,0 g.mL-1, a concentração do ácido cítrico, expressa em mol L-1, será de aproximadamente
a) 0,005.
b) 0,0002.
c) 0,0005.
d) 0,00002.
e) 0,00005.
(MOLARIDADE IÔNICA) D (UFMS 2008) Ao analisar 50 mL de amostra de leite integral de uma marca comercial de leite longa vida por titulometria de complexação, verificou-se a presença de 60 miligramas (mg) de cálcio. A concentração de cálcio (Ca2+) no leite em mol por litro (mol/L) será de
(Massa molar: Ca = 40 g/mol).
- a) 0,20.
- b) 1,50.
- c) 0,80.
- d) 0,03.
- e) 2,00.
D (PUC MG 2008) Assinale a concentração mol/L de solução em relação ao bicarbonato de sódio (NaHCO3), quando se dissolve um comprimido de Sonrisal em um copo com água formando 250 mL de solução.
- a) 0,20
- b) 0,80
- c) 0,02
- d) 0,08
(CONCENTRAÇÃO DAS SOLUÇÕES) B (PUC MG 2008) Uma solução de hidróxido de alumínio (MM = 78 g × mol-1) , utilizada no combate à acidez estomacal, apresenta uma concentração igual a 3,90 g . L-1. A concentração, em mol × L-1, dos íons hidroxila (OH– ) , presentes nessa solução, é igual a:
- a) 5,0 x 10 -1
- b) 1,5 x 10 -1
- c) 1,5 x 10 -2
- d) 5,0 x 10 -2
2007
(CONCENTRAÇÃO DAS SOLUÇÕES) E (UFCSPA 2007) Pretende-se preparar 50 mL de uma solução de Ca(OH)2 (74,0 g/mol) com concentração 1,0 mol/L. Se o grau de pureza do soluto é 74%, a massa da base que deverá ser pesada será de:
- a) 3,0 gramas.
- b) 3,5 gramas.
- c) 4,0 gramas.
- d) 4,5 gramas.
- e) 5,0 gramas.
(SOLUBILIDADE) E (FEI 2007) É correto afirmar com relação à solubilidade de um gás em um líquido, que:
- a) a variação da temperatura não é um fator significativo.
- b) a variação da pressão não é um fator significativo.
- c) o líquido de molécula polar dissolve um gás de molécula apolar.
- d) a solubilidade do gás diminui com a diminuição da temperatura.
- e) um aumento de pressão causa um aumento na solubilidade do gás.
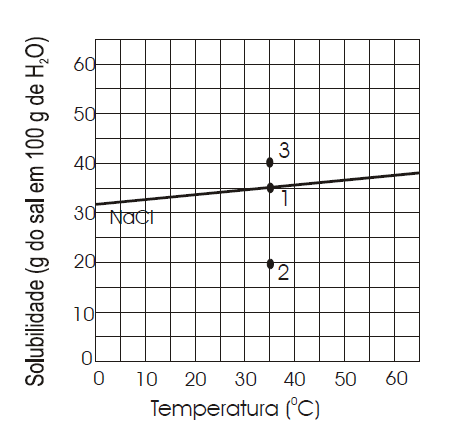
(SOLUBILIDADE) A (UFRN 2007) Os pontos (1), (2) e (3) do gráfico a seguir representam, respectivamente, soluções
- a) saturada, não-saturada e supersaturada.
- b) saturada, supersaturada e não-saturada.
- c) não-saturada, supersaturada e saturada.
- d) não-saturada, saturada e supersaturada.
(CONCENTRAÇÃO DAS SOLUÇÕES) D (UFMS 2007) A sacarose é um carboidrato muito solúvel em água; para saturar 0,5 L de água pura (d = 1,0 g/mL) à temperatura de 20°C, são necessários 1000 g desse açúcar. Qual é, aproximadamente, a concentração dessa solução em porcentagem (m/m)?
- a) 50 %.
- b) 25 %.
- c) 78 %.
- d) 67 %.
- e) 90 %.
(CONCENTRAÇÃO DAS SOLUÇÕES) B (UFMS 2007) Para combater a desidratação infantil, as mães utilizam o soro caseiro, que consiste na mistura de, aproximadamente, 11 gramas de açúcar com cerca de 3,51 gramas de sal de cozinha e água, para um volume total de 1000 mL. Considerando que o sal de cozinha seja constituído apenas de cloreto de sódio, qual a concentração em mols por litro desse sal na solução obtida?
Dados: Massas Atômicas: Na = 23 u; Cl = 35,5 u.
- a) 3,51 x 100.
- b) 6,00 x 10-2.
- c) 9,89 x 10-2.
- d) 3,51 x 10-3.
- e) 1,53 x 10-1.
(TITULAÇÃO) A (UFCSPA 2007) Numa titulação ácido-base de 15,0 mL de ácido sulfúrico (H2SO4) foram gastos 22,5 mL de solução de NaOH 0,2 mol/L. Então, a concentração molar de ácido da solução titulada será de:
- a) 0,15 mol/L.
- b) 0,20 mol/L.
- c) 0,30 mol/L.
- d) 0,60 mol/L.
- e) 1,50 mol/L.
(CONCENTRAÇÃO DAS SOLUÇÕES) C (UNESP 2007) Com o objetivo de diminuir a incidência de cáries na população, em muitas cidades adiciona-se fluoreto de sódio à água distribuída pelas estações de tratamento, de modo a obter uma concentração de 2,0 × 10–5 mol⋅L–1. Com base neste valor e dadas as massas molares em g⋅mol–1: F = 19 e Na = 23, podemos dizer que a massa do sal contida em 500 mL desta solução é:
- a) 4,2 × 10–1 g.
- b) 8,4 × 10–1 g.
- c) 4,2 × 10–4 g.
- d) 6,1 × 10–4 g.
- e) 8,4 × 10–4 g.
2006
(DILUIÇÃO) B (UFAC 2006) Um estudante de química deseja preparar 250 mL de uma solução de sacarose na concentração de 0,10 mol/L, mas dispõe apenas de uma solução estoque do mesmo composto na concentração de 0,25 mol/L. Qual deve ser o volume de água a ser completado para que o estudante obtenha a solução desejada?
- a) 100 mL
- b) 150 mL
- c) 200 mL
- d) 50 mL
- e) 125 mL
(CONCENTRAÇÃO DAS SOLUÇÕES) B (UNESP 2006) Uma pastilha contendo 500 mg de ácido ascórbico (vitamina C) foi dissolvida em um copo contendo 200 mL de água. Dadas as massas molares C = 12 g·mol–1, H = 1 g·mol–1 e
O = 16 g·mol–1 e a fórmula molecular da vitamina C, C6H8O6, a concentração da solução obtida é:
- a) 0,0042 mol·L–1.
- b) 0,0142 mol·L–1.
- c) 2,5 mol·L–1.
- d) 0,5 g·L–1.
- e) 5,0 g·L–1.
2005
(CONCENTRAÇÃO DAS SOLUÇÕES) B (FGV 2005) O gás carbônico, massa molar 0,044 kg/mol, pode ser retido em uma solução de carbonato de potássio, cuja reação pode ser representada pela equação:
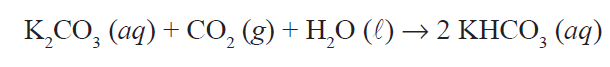 A quantidade mínima, em litros, de uma solução de carbonato de potássio de concentração 0,5 mol/L, que deve ser utilizada para dissolver completamente o CO2 presente em 100 kg de uma amostra de ar contendo 2 200 ppm, em massa, desse gás é
A quantidade mínima, em litros, de uma solução de carbonato de potássio de concentração 0,5 mol/L, que deve ser utilizada para dissolver completamente o CO2 presente em 100 kg de uma amostra de ar contendo 2 200 ppm, em massa, desse gás é
- a) 100.
- b) 10.
- c) 1.
- d) 0,1.
- e) 0,01.
(MOLARIDADE IÔNICA) B (IFRN 2005) Ao analisar-se as concentrações em quantidade de matéria por litro de solução de algumas espécies químicas iônicas em solução aquosa, obteve-se o seguinte resultado: 0,3 mol/L de Mg2+(aq), 0,4 mol/L de Fe3+(aq), 0,4 mol/L de SO42-(aq), 1,2 mol/L de Cl–(aq) e uma quantidade de X mol/L de íons hidroxônio. Pode-se afirmar que o valor assumido pela letra X na situação acima é de:
- a) 0,3 mol/L
- b) 0,2 mol/L
- c) 0,4 mol/L
- d) 0,5 mol/L
(MISTURA COM REAÇÃO QUÍMICA) C (PUC RS 2005) Misturando-se volumes iguais de uma solução de ácido sulfúrico com pH 1,0 e de hidróxido de lítio com pH 13,0, obtém-se uma solução que apresenta pH, aproximadamente,
- a) 0
- b) 1
- c) 7
- d) 12
- e) 14
(CONCENTRAÇÃO DAS SOLUÇÕES) B (PUC RS 2005) Um acadêmico do curso de Química necessita preparar uma solução de ácido bórico (H3BO3) 0,5 mol/L para ser utilizada como fungicida. Para preparar tal solução, ele dispõe de 2,5 g do ácido. O volume, em mL, de solução com a concentração desejada que pode ser preparado utilizando toda a massa disponível é, aproximadamente,
- a) 41
- b) 81
- c) 161
- d) 246
- e) 1000
(CONCENTRAÇÃO DAS SOLUÇÕES) B (UNESP 2005) Há décadas são conhecidos os efeitos da fluoretação da água na prevenção da cárie dentária. Porém, o excesso de fluoreto pode causar a fluorose, levando, em alguns casos, à perda dos dentes. Em regiões onde o subsolo é rico em fluorita (CaF2), a água subterrânea, em contato com ela, pode dissolvê-la parcialmente. Considere que o VMP (Valor Máximo Permitido) para o teor de fluoreto (F–) na água potável é 1,0 mg·L–1 e que uma solução saturada em CaF2, nas condições normais, apresenta 0,0016% em massa (massa de soluto/massa de solução) deste composto, com densidade igual a 1,0 g·cm–3. Dadas as massas molares, em g·mol–1, Ca = 40 e F = 19, é correto afirmar que, nessas condições, a água subterrânea em contato com a fluorita:
- a) nunca apresentará um teor de F– superior ao VMP.
- b) pode apresentar um teor de F– até cerca de 8 vezes maior que o VMP.
- c) pode apresentar um teor de F– até cerca de 80 vezes maior que o VMP.
- d) pode apresentar um teor de F– até cerca de 800 vezes maior que o VMP.
- e) pode apresentar valores próximos a 10–1mol·L–1 em F–.
2004
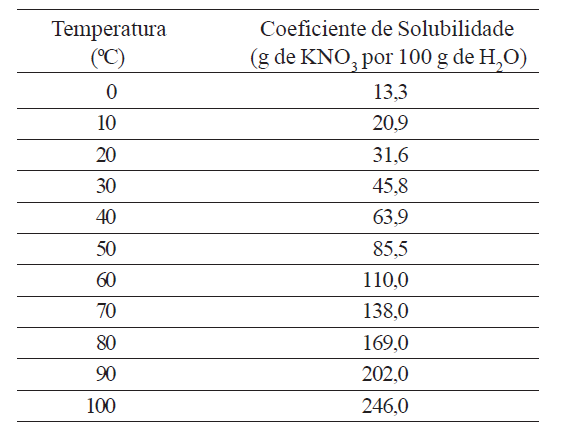
(SOLUBILIDADE) A (UNESP 2004) A quantidade máxima de soluto que pode ser dissolvida numa quantidade padrão de solvente é denominada Coeficiente de Solubilidade. Os valores dos Coeficientes de
Solubilidade do nitrato de potássio (KNO3) em função da temperatura são mostrados na tabela.
Considerando-se os dados disponíveis na tabela, a quantidade mínima de água (H2O), a 30 °C, necessária para dissolver totalmente 6,87 g de KNO3 será de
- a) 15 g.
- b) 10 g.
- c) 7,5 g.
- d) 3 g.
- e) 1,5 g.
(MISTURA SEM REAÇÃO QUÍMICA) A (UNESP 2004) Em um laboratório, foram misturados 200 mL de solução 0,05 mol/L de cloreto de cálcio (CaCl2) com 600 mL de solução 0,10 mol/L de cloreto de alumínio (AlCl3), ambas aquosas. Considerando o grau de dissociação desses sais igual a 100% e o volume final igual à soma dos volumes de cada solução, a concentração, em quantidade de matéria (mol/L),
dos íons cloreto (Cl–) na solução resultante será de
- a) 0,25.
- b) 0,20.
- c) 0,15.
- d) 0,10.
- e) 0,05.
(COLOIDES) D (UNESP 2004) Soluções ou dispersões coloidais são misturas heterogêneas onde a fase dispersa é denominada disperso ou coloide. Quando uma solução coloidal, constituída por coloides liófilos, é submetida a um campo elétrico, é correto afirmar que
- a) as partículas coloidais não conduzem corrente elétrica.
- b) as partículas coloidais irão precipitar.
- c) as partículas coloidais não irão migrar para nenhum dos polos.
- d) todas as partículas coloidais irão migrar para o mesmo polo.
- e) ocorre a eliminação da camada de solvatação das partículas coloidais.
(MISTURA DO MESMO SOLUTO) E (UFMS 2004) O ácido sulfúrico, H2SO4, quando concentrado, é um líquido incolor, oleoso, muito corrosivo, oxidante e desidratante. Nas indústrias químicas, ele é utilizado na fabricação de fertilizantes, de filmes, de tecidos, de medicamentos, de corantes, de tintas, de explosivos, de acumuladores de baterias, no refino do petróleo, como decapante de ferro e aço, etc. Nos laboratórios, é utilizado em titulações, como catalisador de reações e na síntese de outros compostos. Suponha que um químico precise preparar 1 litro de solução aquosa de ácido sulfúrico de concentração 3,5mol/L, usando apenas duas soluções aquosas desse ácido, disponíveis em estoque no laboratório: 1 litro de Solução A de concentração 5,0mol/L e 1 litro de Solução B de concentração 3,0mol/L. Sabendo-se que não há expansão ou contração de volume no preparo da solução desejada, é correto afirmar que os volumes necessários, em mililitros, de A e de B são, respectivamente,
- a) 310 e 690.
- b) 300 e 700.
- c) 240 e 760.
- d) 220 e 780.
- e) 250 e 750.
(DILUIÇÃO) A (UFLA 2004) Uma solução aquosa de nitrato de prata (AgNO3) de concentração 1,5 mol.L-1 foi colocada em aquecimento e seu volume foi reduzido a 300 mL com concentração igual a 4,5 mol.L-1. O volume de água evaporado da solução inicial é de
- a) 600 mL
- b) 900 mL
- c) 1350 mL
- d) 100 mL
- e) 450 mL
2003
(CONCENTRAÇÃO DAS SOLUÇÕES) E (UFAC 2003) Para adoçar um copo de suco de limão, você colocou 3 colheres de sopa de açúcar (glicose, cuja massa molar é 180 g/ mol). Ficou doce! A concentração molar (molaridade) de glicose em solução é: (Dados: 1 copo = 200 mL e 1 colher de sopa = 6 g)
- a) 5,00 M
- b) 5,00 x 10-4 M
- c) 0,05 M
- d) 50,0 M
- e) 0,50 M
EXERCÍCIOS EXTRAS
(CSA 2011 – BIB – U4a) Se 10 cm3 de uma solução 0,3 M de uréia (CO(NH2)2) forem diluídos com 20 cm3 de água, qual será a concentração em gramas por litro da solução obtida?
C (CSA 2011 – BIB – U11) (FATEC) A tabela abaixo mostra o resultado da análise de todos os íons presentes em 1 L de uma solução aquosa.
| Íon | Concentração molar (mol/L) |
| NO3– | 0,5 |
| SO42- | 0,75 |
| Na+ | 0,8 |
| Mg2+ | x |
Com base nos dados apresentados e sabendo que toda solução é eletricamente neutra, podemos afirmar que a concentração molar dos íons Mg2+ é:
- a) 0,4
- b) 0,5
- c) 0,6
- d) 1,0
- e) 1,2
(CSA 2011 – BIB – U12) (FUVEST 1990) O processo de recristalização, usado na purificação de sólidos, consiste no seguinte:
1º) Dissolve-se o sólido em água quente, até a saturação;
2º) Resfria-se a solução até que o sólido se cristalize.
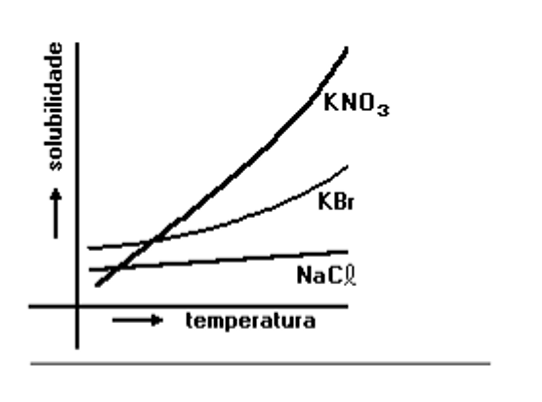
Os gráficos abaixo mostram a variação, com a temperatura, da solubilidade de alguns compostos em água.
O método de purificação descrito acima é mais eficiente e menos eficiente, respectivamente, para:
- a) NaCℓ e KNO3
- b) KBr e NaCℓ
- c) KNO3 e KBr
- d) NaCℓ e KBr
- e) KNO3 e NaCℓ
E (CSA 2011 – BIB – U13) (UFSJ 2005) Uma mistura é preparada adicionando-se 80 g de acetato de sódio em 100 g de água a uma temperatura de 20 °C. Esta mistura é, então, aquecida até 50 °C, obtendo-se a dissolução completa do sal. A seguir, resfria-se a mistura, cuidadosamente sem agitação, até 20 °C. Após acrescenta-se um pequeno cristal de acetado de sódio à mistura.
Dado: O coeficiente de solubilidade do acetato de sódio é de 46,5 g/100 g de H2O a 20 °C. Estes procedimentos são esquematizados abaixo:
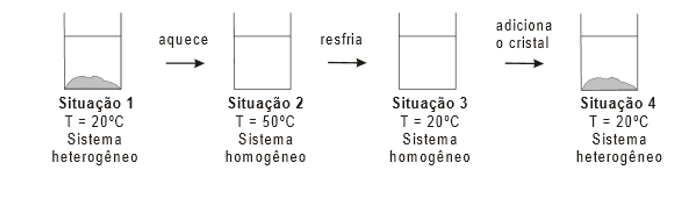 As soluções obtidas nas situações 1, 2, 3 e 4 são, respectivamente:
As soluções obtidas nas situações 1, 2, 3 e 4 são, respectivamente:
- a) insaturada, concentrada, saturada e insaturada.
- b) supersaturada, insaturada, saturada e concentrada.
- c) saturada, diluída, supersaturada e concentrada.
- d) supersaturada, diluída, concentrada e supersaturada.
- e) saturada, insaturada, supersaturada e saturada.
E (CSA 2011 – BIB – U14) (PUCCAMP 2000) Para produzir 1,0 tonelada de açúcar refinado (sacarose) de beterraba, são necessárias 8,0 toneladas de beterrabas açucareiras que, para o plantio, requerem uma área de 1,8 × 103 m2. Sendo assim, o preparo de 100 litros de solução aquosa 1mol/L do açúcar, requer uma área de plantio próxima de:
Dado: Massa molar da sacarose = 3,4 × 102 g/mol
- a) 10 m2
- b) 20 m2
- c) 40 m2
- d) 50 m2
- e) 60 m2
D (CSA 2011 – BIB – U15) O ácido clorídrico reage com cálcio segundo a equação não balanceada:
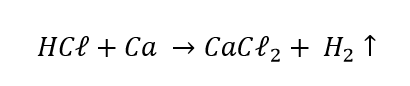 Que massa de cálcio consome totalmente o ácido existente em 500 cm3 de solução 0,8 M de HCℓ?
Que massa de cálcio consome totalmente o ácido existente em 500 cm3 de solução 0,8 M de HCℓ?
- a) 0,4 g
- b) 0,8 g
- c) 4 g
- d) 8 g
- e) 20 g
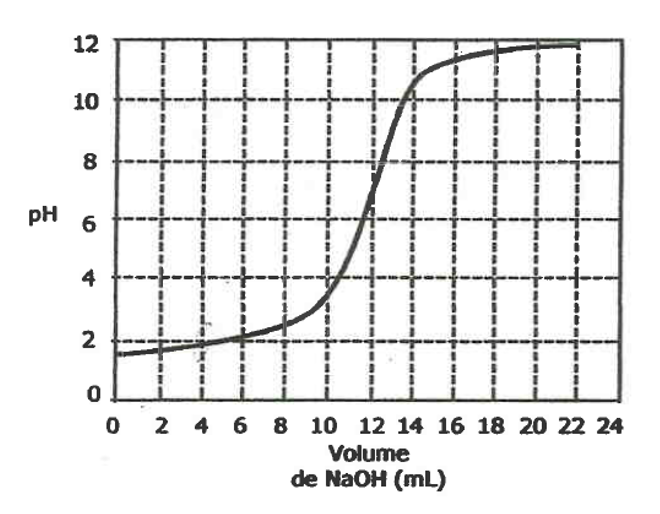
D (CSA 2011 – BIB – U16) A titulação potenciométrica de 25 mL de uma solução de H2SO4 foi realizada utilizando-se uma solução padrão 0,1 M de NaOH, sendo obtida a curva representada no gráfico a seguir:
Com base nesses dados, podemos concluir que a concentração do ácido sulfúrico titulado é, em mol/L:
- a) 0,080
- b) 0,040
- c) 0,048
- d) 0,024
- e) 0,012
(CSA 2010 – BIB – U6a)
- a) Que volume de água deve ser adicionado a 200 mL de solução de NaOH a 40% em massa de soluto e densidade 1,2 g/mL, para transformá-la numa solução 3 M?
- b) Que massa de KOH é capaz de neutralizar 400 cm3 de solução 0,2 M de H2SO4?
E (CSA 2010 – BIB – U7) (FUVEST 1998) O gráfico abaixo mostra a solubilidade (S) de K2Cr2O7, sólido em água, em função da temperatura (t).
Uma mistura constituída de 30 g de K2Cr2O7 e 50 g de água, a uma temperatura inicial de 90 °C, foi deixada esfriar lentamente e com agitação. A que temperatura aproximada deve começar a cristalizar o K2Cr2O7?
- a) 25 °C
- b) 80 °C
- c) 60 °C
- d) 45 °C
- e) 70 °C
D (CSA 2010 – BIB – U8) (UFPA) Para conhecer com exatidão a concentração de uma solução de NaOH, preparada previamente, um aluno no laboratório de química da UFPA executou o seguinte procedimento:
1 – retirou uma alíquota de 25 mL de solução da base
2 – titulou esta alíquota utilizando solução padrão de HCℓ
Para realizar corretamente esta operação o aluno precisa de
- a) proveta, béquer, balão de fundo redondo e solução de indicador.
- b) pipeta graduada de 25 mL, erlenmeyer, pisseta e bureta.
- c) proveta, erlenmeyer, pisseta e bureta.
- d) pipeta volumétrica, erlenmeyer, bureta e solução de indicador.
- e) proveta, béquer, funil de separação e bureta.