QUÍMICA – LISTA DE EXERCÍCIOS SOBRE ESTADOS FÍSICOS E DIAGRAMAS DE ESTADO
CAIU NO VESTIBULAR!
2018
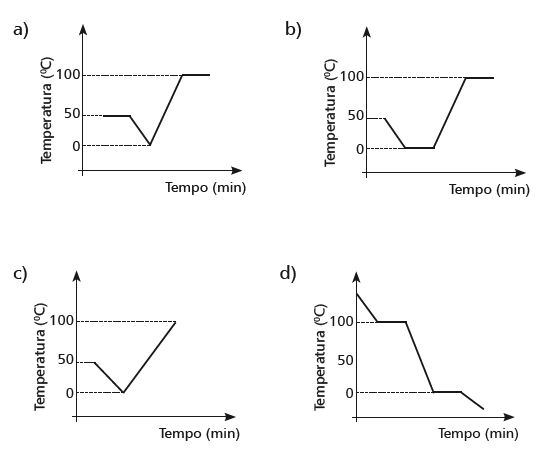
(ESTADOS FÍSICOS) B (CEFET MG 2018) Um estudante recebeu uma amostra de água pura, sob pressão de 1 atm, inicialmente à 50°C. A amostra foi submetida ao resfriamento até alcançar 0°C, permanecendo por alguns minutos, nessa temperatura. Posteriormente, foi aquecida e mantida a 100°C.
Considerando-se que as temperaturas de fusão e ebulição da água pura, a 1 atm, são, respectivamente, 0 e 100°C, o gráfico da temperatura em função do tempo que esboça essa transformação é
B (FGV SP 2018) O gráfico apresenta a variação da temperatura de uma substância durante aquecimento sob pressão constante.
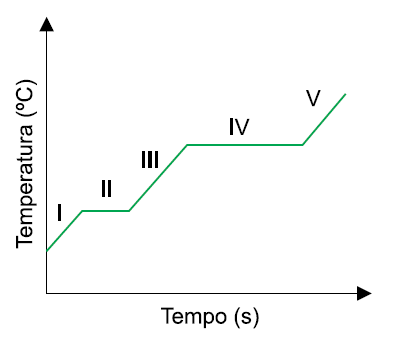 Na representação gráfica, a fusão da substância ocorre no segmento
Na representação gráfica, a fusão da substância ocorre no segmento
- a) I.
- b) II.
- c) III.
- d) IV.
- e) V.
D (UERJ 2018) Observe no diagrama as etapas de variação da temperatura e de mudanças de estado físico de uma esfera sólida, em função do calor por ela recebido. Admita que a esfera é constituída por um metal puro.
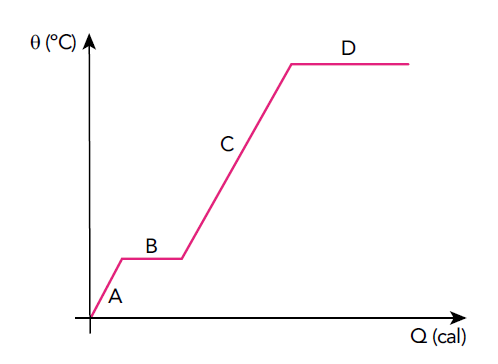
Durante a etapa D, ocorre a seguinte mudança de estado físico:
- a) fusão
- b) sublimação
- c) condensação
- d) vaporização
2017
2016
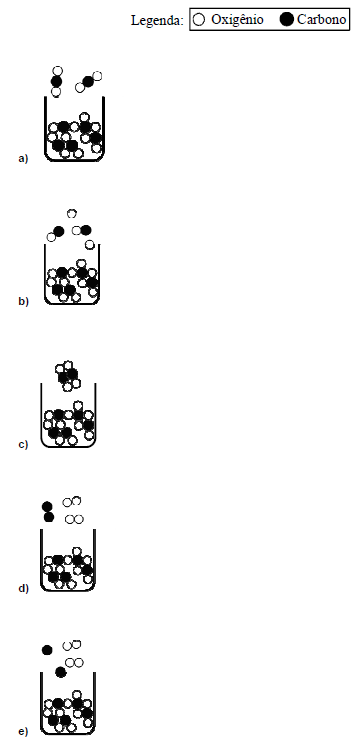
(ESTADOS FÍSICOS) A (UFJF – PISM 1 2016) Gelo-seco é o nome popular do dióxido de carbono sólido. Nas condições ambientais esse material sofre sublimação rompendo suas ligações intermoleculares. Assinale a alternativa que representa o processo de sublimação do gelo seco.
2015
(ESTADOS FÍSICOS) A (UFJF – PISM 1 2015) O gráfico abaixo apresenta a variação de temperatura observada ao se aquecer uma substância A, a partir de 25 °C, em função do tempo.
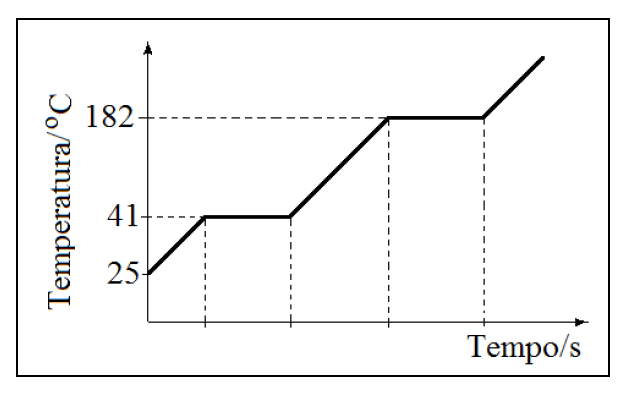
Assinale a alternativa CORRETA.
- a) A faixa de temperatura em que a substância permanece sólida é 25-41 °C.
- b) A substância A não é uma substância pura.
- c) A temperatura de ebulição da substância A é 41 °C.
- d) A faixa de temperatura em que a substância permanece líquida é 25-182 °C.
- e) Em 25 °C, a substância é um líquido.
2014
(ESTADOS FÍSICOS) D (UFJF – PISM 1 2014) Dois materiais sólidos, A e B, são aquecidos a uma velocidade de 10°C.min -1. A figura a seguir representa o diagrama de aquecimento desses dois materiais.
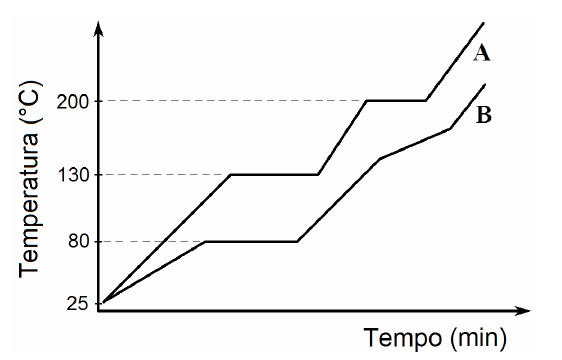
Com base no gráfico, assinale a alternativa que apresenta a afirmativa CORRETA.
- a) Os materiais A e B são substâncias puras e possuem pontos de fusão iguais a 130°C e 80°C, respectivamente.
- b) O material B é uma mistura azeotrópica de ponto de fusão igual a 80°C.
- c) Na temperatura de 120°C, o material A encontra-se na fase líquida e o material B encontra-se na fase sólida.
- d) O material A é uma substância pura, na qual a fase líquida e a fase gasosa coexistem em 200°C.
- e) No material B, entre 130°C e 200°C, coexistem as fases sólida, l íquida e gasosa em pressão atmosférica.
a (FGV SP 2014) O conhecimento das propriedades físico-químicas das substâncias é muito útil para avaliar condições adequadas para a sua armazenagem e transporte.
Considere os dados das três substâncias seguintes:
 É correto afirmar que em um ambiente a 35 ºC, sob pressão atmosférica, as substâncias I, II e III apresentam-se, respectivamente, nos estados físicos
É correto afirmar que em um ambiente a 35 ºC, sob pressão atmosférica, as substâncias I, II e III apresentam-se, respectivamente, nos estados físicos
- a) sólido, gasoso e líquido.
- b) sólido, gasoso e gasoso.
- c) sólido, líquido e líquido.
- d) líquido, gasoso e líquido.
- e) líquido, líquido e gasoso.
2013
2012
2011
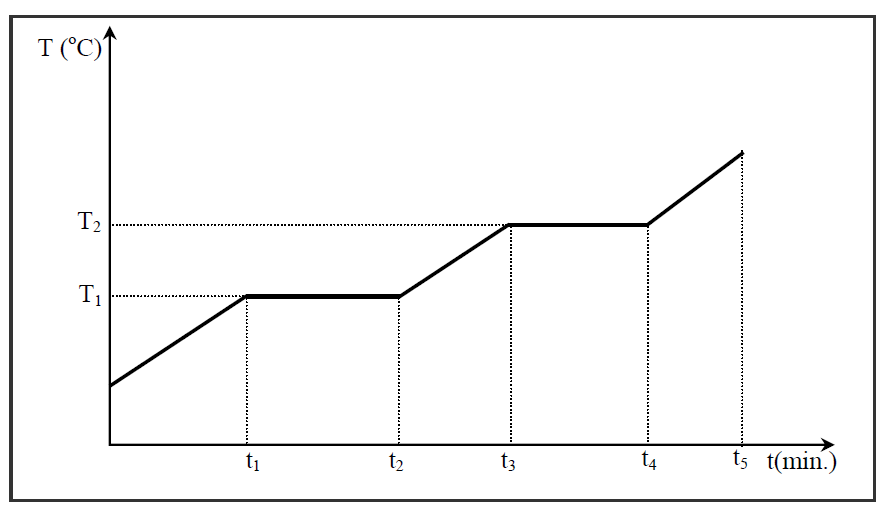
(UFSC 2011) Considere a curva de aquecimento de uma substância sólida até seu estado gasoso, em função do tempo, à pressão de 1 atm.
De acordo com as informações do enunciado e com o gráfico acima, assinale a(s) proposição(ões) correta(s).
- 01) No tempo t2 coexistem sólido e líquido.
- 02) A temperatura T2 representa o ponto de ebulição da substância.
- 04) No intervalo de tempo t3 a t4, os estados líquido e vapor da substância coexistem a uma temperatura constante.
- 08) A curva de aquecimento mostra que a substância não é pura, mas sim, uma mistura homogênea simples.
- 16) O tempo t1 representa o início da vaporização da substância.
- 32) No intervalo de tempo t2 a t3, a substância se encontra no estado líquido a uma temperatura que varia de T1 a T2.
RESPOSTA: 02 + 04 + 32 = 38.
2010
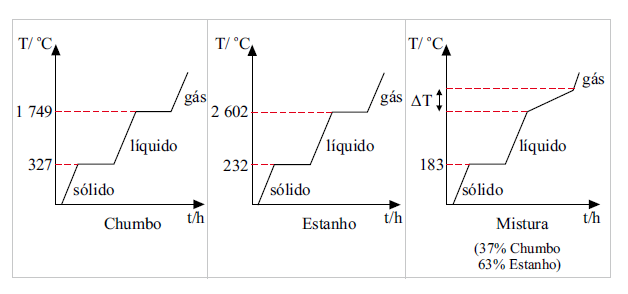
A (UNESP 2010) No campo da metalurgia é crescente o interesse nos processos de recuperação de metais, pois é considerável a economia de energia entre os processos de produção e de reciclagem, além da redução significativa do lixo metálico. E este é o caso de uma microempresa de reciclagem, na qual desejava-se desenvolver um método para separar os metais de uma sucata, composta de aproximadamente 63 % de estanho e 37 % de chumbo, usando aquecimento. Entretanto, não se obteve êxito nesse procedimento de separação. Para investigar o problema, foram comparadas as curvas de aquecimento para cada um dos metais isoladamente com aquela da mistura, todas obtidas sob as mesmas condições de trabalho.
Considerando as informações das figuras, é correto afirmar que a sucata é constituída por uma
- a) mistura eutética, pois funde a temperatura constante.
- b) mistura azeotrópica, pois funde a temperatura constante.
- c) substância pura, pois funde a temperatura constante.
- d) suspensão coloidal que se decompõe pelo aquecimento.
- e) substância contendo impurezas e com temperatura de ebulição constante.
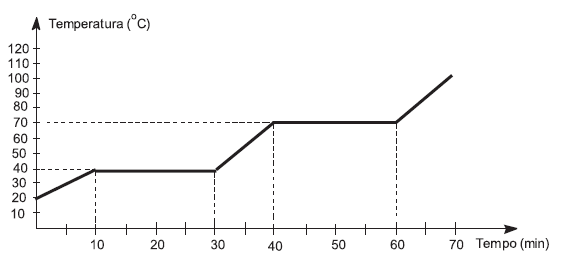
(ESTADOS FÍSICOS) C (UTFPR 2010) Um cientista recebeu uma substância desconhecida, no estado sólido, para ser analisada. O gráfico abaixo representa o processo de aquecimento de uma amostra dessa substância.
Analisando o gráfico, podemos concluir que a amostra apresenta:
- a) duração da ebulição de 10 min.
- b) duração da fusão de 40 min.
- c) ponto de fusão de 40o
- d) ponto de fusão de 70o
- e) ponto de ebulição de 50o
(ESTADOS FÍSICOS/SEPARAÇÃO DE MISTURAS) E (UFJF – PISM 1 2010) Um estudante dissolveu uma pequena quantidade de sal de cozinha (NaCl) em um copo contendo 200 mL de água; depois aqueceu o sistema até a ebulição e mediu a temperatura. Feito esse experimento, ele escreveu as seguintes observações:
I – A dissolução do sal na água produziu uma mistura em que não se pode distinguir seus componentes nem a olho nu nem com um microscópio, portanto a mistura é homogênea.
II – Durante a ebulição da solução, a temperatura não foi constante, e isso aconteceu porque a solução é uma mistura e não uma substância pura.
III -Para recuperar o sal, podem ser usados dois processos de separação: evaporação ou destilação simples.
De acordo com as observações feitas pelo estudante, assinale a alternativa CORRETA.
- a) Somente as afirmativas I e II estão corretas.
- b) Somente as afirmativas I e III estão corretas.
- c) Somente as afirmativas II e III estão corretas.
- d) Todas as afirmativas estão incorretas.
- e) Todas as afirmativas estão corretas.
EXERCÍCIOS EXTRAS
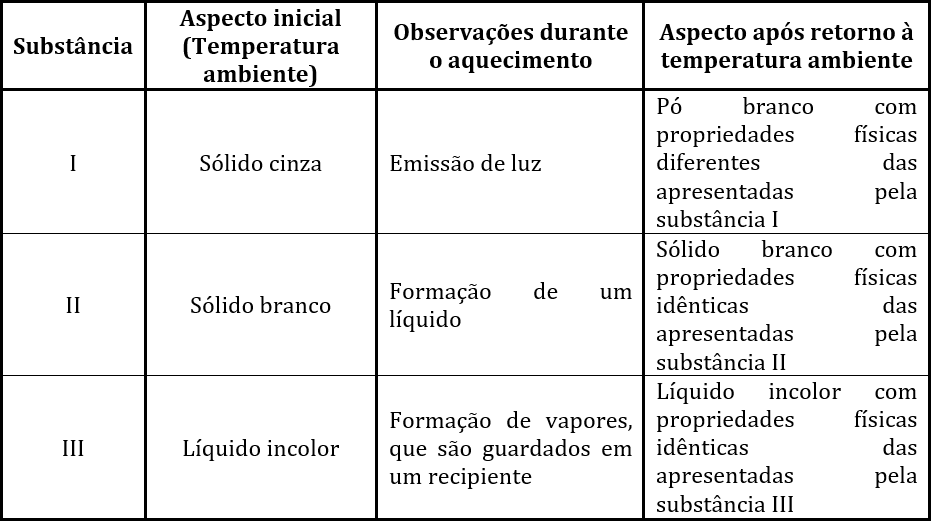
(ESTADOS FÍSICOS) B (CSA 1 – 2013 – BIA – S17) (UFRGS) Amostras de três substâncias foram aquecidas sob pressão constante. Os dados relativos ao procedimento constam da tabela abaixo.
Os processos que ocorreram com as substâncias I, II e III durante o aquecimento podem ser denominados, respectivamente:
- a) Fusão, ebulição e condensação.
- b) Combustão, fusão e ebulição.
- c) Sublimação, liquefação e condensação.
- d) Combustão, liquefação e sublimação.
- e) Sublimação, ebulição e vaporização.
(ESTADOS FÍSICOS) E (CSA 1 – 2012 – BIA – S22) (UEL-PR) Considere os seguintes dados de pontos de fusão e de ebulição, sob pressão de 1 atm:
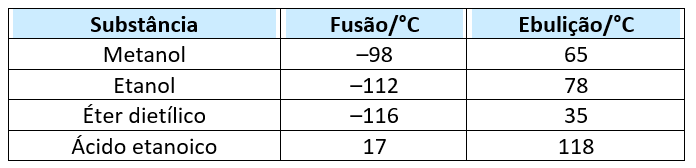 Ao nível do mar e no verão, dentre as substâncias acima, deve-se estocar em geladeira, por razões de segurança, apenas:
Ao nível do mar e no verão, dentre as substâncias acima, deve-se estocar em geladeira, por razões de segurança, apenas:
- a) metanol e etanol.
- b) éter dietílico e ácido etanóico.
- c) etanol e ácido etanóico.
- d) ácido etanóico.
- e) éter dietílico
(ESTADOS FÍSICOS) E (CSA 1 – 2012 – BIA – S17) Dois copos, A e B, contendo respectivamente 100 mL e 200 mL de água destilada, são aquecidos uniformemente com a mesma fonte de calor. Sendo: tA e tB os tempos gastos para iniciar a ebulição, respectivamente, nos copos A e B; TEA e TEB as temperaturas de ebulição, respectivamente, nos copos A e B, podemos afirmar que:
- a) tA = tB ; TEA = TEB
- b) tA < tB ; TEA < TEB
- c) tA > tB ; TEA > TEB
- d) tA > tB ; TEA = TEB
- e) tA < tB ; TEA = TEB
(ESTADOS FÍSICOS) B (CSA 1 – 2012 – BIA – S23) No esquema a seguir, X, Y e Z representam os estados de agregação de uma substância:
X → transformação exotérmica → Y → transformação endotérmica → Z
Pode-se dizer que uma possibilidade para os estados de agregação de X, Y e Z é, respectivamente:
- a) sólido, líquido e gasoso.
- b) líquido, sólido e gasoso.
- c) líquido, gasoso e sólido.
- d) gasoso, líquido e sólido.
- e) sólido, gasoso e líquido.
(ESTADOS FÍSICOS) C (CSA 1 – 2012 – BIA – S24) Considere uma mistura de três gases A, B e C, que possui os seguintes pontos de condensação (PC):
Gás A: PC = 0 oC
Gás B: PC = –25 oC
Gás C: PC = –40 oC
Pode-se afirmar que:
- a) A mistura das três substâncias será, a 10 oC, certamente heterogênea.
- b) Se a mistura for resfriada a 10 oC, apenas o gás A irá se condensar.
- c) Efetuando-se a condensação total da mistura e, em seguida, começar um aquecimento lento, a primeira substância a entrar em ebulição será a C.
- d) Abaixando-se gradativamente a temperatura, o gás C irá condensar em primeiro lugar.
- e) A mistura, na temperatura de –60 oC, certamente estará no estado gasoso.
(ESTADOS FÍSICOS) E (CSA 1 – 2012 – BIA – UT1) (Cftmg 2007 – adaptada) O ácido láurico é conhecido na indústria farmacêutica pela sua propriedade antimicrobiana. O gráfico representa a curva de resfriamento de uma amostra desse ácido, inicialmente no estado líquido, a uma temperatura acima de seu ponto de solidificação.
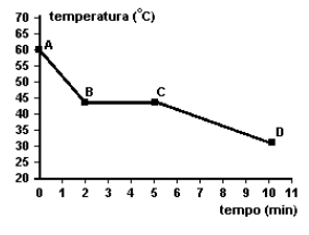 Sobre esse sistema e suas transformações, afirma-se, corretamente, que
Sobre esse sistema e suas transformações, afirma-se, corretamente, que
- a) a temperatura de fusão do ácido láurico é 30 °C.
- b) a temperatura de ebulição do ácido láurico é 60 °C.
- c) nos primeiros dois minutos, a temperatura decresce 15 °C/min.
- d) as moléculas de ácido se movimentam mais no ponto D, do que no A.
- e) as fases líquida e sólida coexistem no segmento BC.
(ESTADOS FÍSICOS) C (CSA 1 – 2012 – BIA – UT9) (Utfpr 2007) Em uma noite de inverno rigoroso uma dona de casa estendeu as roupas recém lavadas no varal, expostas ao tempo. Pela manhã as roupas congelaram, em função do frio intenso. Com a elevação da temperatura no decorrer da manhã, começou a pingar água das roupas, em seguida elas ficaram apenas úmidas, e elas logo estavam secas. Ocorreram nestas roupas, respectivamente, as seguintes passagens de estados físicos:
- a) fusão, solidificação e evaporação.
- b) solidificação, evaporação e fusão.
- c) solidificação, fusão e evaporação.
- d) fusão, evaporação e solidificação.
- e) evaporação, solidificação e fusão
(ESTADOS FÍSICOS) (CSA 1 – 2008 – BIA – U6) Uma mistura eutética comporta-se, na fusão, como uma substância pura e, na ebulição, como uma mistura. Construa o gráfico temperatura x tempo, indicando os estados físicos em cada trecho, que represente o aquecimento de uma mistura eutética inicialmente sólida a 0°C. Depois de 5 minutos, ocorre a primeira mudança de estado a 15°C, que dura 3 minutos. Prossegue então o procedimento por mais 4 minutos até atingir 60°C. Começa então a segunda mudança de estado, que dura o dobro do tempo da primeira e termina a 80°C. A amostra é aquecida por mais 4 minutos, até o momento em que atinge 100 °C.