QUÍMICA – LISTA DE EXERCÍCIOS SOBRE MODELOS ATÔMICOS
(MODELOS ATÔMICOS/PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO [NÚMERO ATÔMICO,
NÚMERO DE MASSA, SEMELHANÇAS ATÔMICAS, ÍONS] E DISTRIBUIÇÃO ELETRÔNICA)
CAIU NO ENEM!
B (ENEM 2017) Um fato corriqueiro ao se cozinhar arroz é o derramamento de parte da água de cozimento sobre a chama azul do fogo, mudando-a para uma chama amarela. Essa mudança de cor pode suscitar interpretações diversas, relacionadas às substâncias presentes na água de cozimento. Além do sal de cozinha (NaCl), nela se encontram carboidratos, proteínas e sais minerais. Cientificamente, sabe-se que essa mudança de cor da chama ocorre pela
- a) reação do gás de cozinha com o sal, volatilizando gás cloro.
- b) emissão de fótons pelo sódio, excitado por causa da chama.
- c) produção de derivado amarelo, pela reação com o carboidrato.
- d) reação do gás de cozinha com a água, formando gás hidrogênio.
- e) excitação das moléculas de proteínas, com formação de luz amarela.
CAIU NO VESTIBULAR!
2018
2017
2016
(MODELOS ATÔMICOS) D (UFJF – PISM 1 2016) Desde a Grécia antiga, filósofos e cientistas vem levantando hipóteses sobre a constituição da matéria. Demócrito foi uns dos primeiros filósofos a propor que a matéria era constituída por partículas muito pequenas e indivisíveis, as quais chamaram de átomos. A partir de então, vários modelos atômicos foram formulados, à medida que novos e melhores métodos de investigação foram sendo desenvolvidos. A seguir, são apresentadas as representações gráficas de alguns modelos atômicos:
Assinale a alternativa que correlaciona o modelo atômico com a sua respectiva representação gráfica.
- a) I- Thomson, II- Dalton, III- Rutherford-Bohr.
- b) I- Rutherford-Bohr, II- Thomson, III- Dalton.
- c) I- Dalton, II- Rutherford-Bohr, III- Thomson.
- d) I- Dalton, II- Thomson, III- Rutherford-Bohr.
- e) I- Thomson, II- Rutherford-Bohr, III- Dalton.
2015
(DISTRIBUIÇÃO ELETRÔNICA) C (UFJF – PISM 1 2015) O metal que dá origem ao íon metálico mais abundante no corpo humano tem, no estado fundamental, a seguinte configuração eletrônica:
- a) ferro (Z=26).
- b) silício (Z = 14).
- c) cálcio (Z = 20).
- d) magnésio (Z= 12).
- e) zinco (Z= 30).
2014
(MODELOS ATÔMICOS) A (UFJF – PISM 1 2014) A emissão de radiação eletromagnética (luz) dos corpos com o aumento da temperatura ocorre quando elétrons excitados retornam para níveis energéticos inferiores. Assinale a alternativa que relaciona o modelo atômico com esse fenômeno.
- a) O modelo de Rutherford-Bohr, no qual os elétrons movem-se ao redor do núcleo em órbitas bem definidas.
- b) O modelo de Rutherford, no qual o feixe de partículas alfa que atravessa uma lâmina fina de ouro causa a excitação dos elétrons.
- c) O modelo de Thomson, no qual o aumento da temperatura faz com que elétrons sejam ejetados do átomo, formando um íon colorido.
- d) O modelo atômico de Dalton, no qual os elétrons, movendo-se em órbitas estacionárias, não emitem nem absorvem energia.
- e) O modelo conhecido como “pudim de passas”, no qual os elétrons estão distribuídos no interior de uma esfera carregada positivamente.
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) E (FGV SP 2014) Uma nova e promissora classe de materiais supercondutores tem como base o composto diboreto de zircônio e vanádio. Esse composto é sintetizado a partir de um sal de zircônio (IV).
(Revista Pesquisa FAPESP, Junho 2013. Adaptado)
O número de prótons e de elétrons no íon Zr4+ e o número de elétrons na camada de valência do elemento boro no estado fundamental são, respectivamente:
- a) 36; 40; 5.
- b) 36; 40; 3.
- c) 40; 44; 3.
- d) 40; 36; 5.
- e) 40; 36; 3.
2013
(MOLDELOS ATÔMICOS) B (UFJF – PISM 1 2013) Ernest Rutherford (1871-1937) fez diversos experimentos para propor sua teoria atômica. O mais famoso experimento consistiu no bombardeamento de um feixe de partículas alfa em uma fina folha de ouro. A partir desse experimento, ele evidenciou que:
- a) o átomo era indivisível.
- b) o átomo contém imensos vazios.
- c) o modelo proposto por Dalton estava correto.
- d) os elétrons existiam.
- e) os elétrons nos átomos giram em torno do núcleo.
2012
A (UNESP 2012) A Lei da Conservação da Massa, enunciada por Lavoisier em 1774, é uma das leis mais importantes das transformações químicas. Ela estabelece que, durante uma transformação química, a soma das massas dos reagentes é igual à soma das massas dos produtos. Esta teoria pôde ser explicada, alguns anos mais tarde, pelo modelo atômico de Dalton. Entre as ideias de Dalton, a que oferece a explicação mais apropriada para a Lei da Conservação da Massa de Lavoisier é a de que:
- a) Os átomos não são criados, destruídos ou convertidos em outros átomos durante uma transformação química.
- b) Os átomos são constituídos por 3 partículas fundamentais: prótons, nêutrons e elétrons.
- c) Todos os átomos de um mesmo elemento são idênticos em todos os aspectos de caracterização.
- d) Um elétron em um átomo pode ter somente certas quantidades específicas de energia.
- e) Toda a matéria é composta por átomos.
2011
(MODELOS ATÔMICOS) D (ESPCEX 2011) Considere as seguintes afirmações, referentes à evolução dos modelos atômicos:
- No modelo de Dalton, o átomo é dividido em prótons e elétrons.
- No modelo de Rutherford, os átomos são constituídos por um núcleo muito pequeno e denso e carregado positivamente. Ao redor do núcleo estão distribuídos os elétrons, como planetas em torno do Sol.
- O físico inglês Thomson afirma, em seu modelo atômico, que um elétron, ao passar de uma órbita para outra, absorve ou emite um quantum (fóton) de energia.
Das afirmações feitas, está(ão) correta(s)
- a) apenas III.
- b) apenas I e II.
- c) apenas II e III.
- d) apenas II.
- e) todas
(MODELOS ATÔMICOS) C (IFCE 2011) Ricardo, ao observar sua mãe cozinhar em fogão a gás, percebeu que a chama azul do bico de gás do fogão ficava amarelada, sempre que nela caía um pouco de sal ou alimento com sal. Sabe-se que o elemento químico sódio (Na) é responsável por essa alteração de cor. Este efeito ocorre, porque
- a) a ação da chama produz uma excitação dos elétrons da eletrosfera do sódio, fazendo com que eles migrem para níveis de menor energia na eletrosfera.
- b) a excitação provocada pela ação da chama faz com que os elétrons da eletrosfera do sódio saltem de um nível mais interno para um nível mais externo.
- c) os elétrons da eletrosfera do sódio, que foram excitados pela ação da chama, retornam ao nível mais interno.
- d) os elétrons do sódio possuem uma coloração amarelada e, ao caírem na chama, fazem com que ela adquira essa cor.
- e) ocorre uma reação química com os átomos de sódio, ao serem aquecidos pela chama.
(MODELOS ATÔMICOS) (UFSC 2011) Quando uma pequena quantidade de cloreto de sódio é colocada na ponta de um fio de platina e levada à chama de um bico de Bunsen, a observação macroscópica que se faz é que a chama inicialmente azul adquire uma coloração laranja. Outros elementos metálicos ou seus sais produzem uma coloração característica ao serem submetidos à chama, como exemplo: potássio (violeta), cálcio (vermelho-tijolo), estrôncio (vermelho-carmim) e bário (verde). O procedimento descrito é conhecido como teste de chama, que é uma técnica utilizada para a identificação de certos átomos ou cátions presentes em substâncias ou misturas.
Sobre o assunto acima e com base na Teoria Atômica, é correto afirmar que:
- 01) as cores observadas para diferentes átomos no teste de chama podem ser explicadas pelos modelos atômicos de Thomson e de Rutherford.
- 02) as cores observadas na queima de fogos de artifícios e da luz emitida pelas lâmpadas de vapor de sódio ou de mercúrio não são decorrentes de processos eletrônicos idênticos aos observados no teste de chama.
- 04) a cor da luz emitida depende da diferença de energia entre os níveis envolvidos na transição das partículas nucleares e, como essa diferença varia de elemento para elemento, a luz apresentará uma cor característica para cada elemento.
- 08) no teste de chama as cores observadas são decorrentes da excitação de elétrons para níveis de energia mais externos provocada pela chama e, quando estes elétrons retornam aos seus níveis de origem, liberam energia luminosa, no caso, na região da luz visível.
- 16) as cores observadas podem ser explicadas considerando-se o modelo atômico proposto por Bohr.
RESPOSTA: 08 + 16 = 24.
(MODELOS ATÔMICOS) A (IFCE 2011) Ao longo da história da humanidade, muitos cientistas se envolveram na tentativa de explicar do que a matéria era formada. Desse modo, muitos modelos foram sendo sugeridos, na tentativa de solucionar essa questão.
O modelo da estrutura atômica formulado por Rutherford apresentou como novidade a noção de
- a) núcleo
- b) massa atômica
- c) energia quantizada
- d) orbital
- e) spin
(MODELOS ATÔMICOS) C (UFPB 2011) Rutherford idealizou um modelo atômico com duas regiões distintas. Esse modelo pode ser comparado a um estádio de futebol com a bola no centro: a proporção entre o tamanho do estádio em relação à bola é comparável ao tamanho do átomo em relação ao núcleo (figura).
 Acerca do modelo idealizado por Rutherford e considerando os conhecimentos sobre o átomo, é correto afirmar:
Acerca do modelo idealizado por Rutherford e considerando os conhecimentos sobre o átomo, é correto afirmar:
- a) Os prótons e os nêutrons são encontrados na eletrosfera.
- b) Os elétrons possuem massa muito grande em relação à massa dos prótons.
- c) O núcleo atômico é muito denso e possui partículas de carga positiva.
- d) A eletrosfera é uma região onde são encontradas partículas de carga positiva.
- e) O núcleo atômico é pouco denso e possui partículas de carga negativa.
(MODELOS ATÔMICOS) A (UFPR 2011) A constituição elementar da matéria sempre foi uma busca do homem. Até o início do século XIX, não se tinha uma ideia concreta de como a matéria era constituída. Nas duas últimas décadas daquele século e início do século XX, observou-se um grande avanço das ciências e com ele a evolução dos modelos atômicos. Acerca desse assunto, numere a coluna da direita de acordo com sua correspondência com a coluna da esquerda.
| 1. Próton. | ( ) Partícula de massa igual a 9,109 × 10-31 kg e carga elétrica de -1,602 × 10-19 C. |
| 2. Elétron. | ( ) Partícula constituída por um núcleo contendo prótons e nêutrons, rodeado por elétrons que circundam em órbitas estacionárias. |
| 3. Átomo de Dalton. | ( ) Partícula indivisível e indestrutível durante as transformações químicas. |
| 4. Átomo de Rutherford. | ( ) Partícula de massa igual a 1,673 × 10−27 kg, que corresponde à massa de uma unidade atômica. |
| 5. Átomo de Bohr. | ( ) Partícula que possui um núcleo central dotado de cargas elétricas positivas, sendo envolvido por uma nuvem de cargas elétricas negativas. |
Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
- a) 2 – 5 – 3 – 1 – 4.
- b) 1 – 3 – 4 – 2 – 5.
- c) 2 – 4 – 3 – 1 – 5.
- d) 2 – 5 – 4 – 1 – 3.
- e) 1 – 5 – 3 – 2 – 4.
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) A (CEFET MG 2011) O íon X+3 possui 30 nêutrons e número de massa igual a 54. A quantidade de elétrons que essa espécie possui é
- a) 21
- b) 24
- c) 27
- d) 84
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) C (UFU 2011) Há um grande medo nas pessoas em relação aos avanços das técnicas nucleares. Porém, áreas como a medicina, a agricultura e particularmente a indústria farmacêutica são beneficiadas com o desenvolvimento destas técnicas. A radioterapia, por exemplo, que teve sua origem na aplicação do elemento rádio pelo casal Curie, para destruir células cancerosas, é hoje realizada com radioisótopos do iodo, como o iodo-131, em terapia para eliminar lesões, identificadas nos radiodiagnósticos da tireoide.
Fonte: http://www.cnen.gov.br/ensino/apostilas/aplica.pdf
Sobre esse radioisótopo, assinale a alternativa correta.
- a) A principal diferença entre radioisótopos do iodo, como o iodo-131 e o iodo-123, está no número de prótons presentes no núcleo destes elementos.
- b) O iodo-131 possui 77 nêutrons e seu número atômico é 53.
- c) Sabendo que o iodo-131 é incorporado ao corpo do paciente através da ingestão de iodeto de potássio (KI), pode-se afirmar que, neste composto, o número de oxidação do iodo é -1.
- d) Os isótopos, que são átomos de diferentes elementos químicos, podem ser explicadas a partir dos postulados de Dalton sobre a teoria atômica.
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) E (UESC 2011) As espécies químicas iônicas 82Pb2+ e 82Pb4+, provenientes de isótopos distintos de chumbo encontrados na natureza, apresentam
- a) massas atômicas iguais.
- b) número de massa e de nêutrons iguais.
- c) número atômico e de prótons diferentes.
- d) raios iônicos e configurações eletrônicas iguais.
- e) configurações eletrônicas com diferentes números de elétrons.
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) B (G1 – ccampos 2011) O elemento químico B possui 20 nêutrons, é isótopo do elemento químico A, que possui x prótons, e isóbaro do elemento químico C, que tem 16 nêutrons. O número de massa de C é 2x+2. Sabendo-se que A e C são isótonos, pode-se afirmar que o somatório do número de massa, do número atômico e de número de nêutrons dos elementos A, B e C, respectivamente, está relacionado na alternativa:
- a) 109, 56 e 53.
- b) 110, 58 e 52.
- c) 112, 54 e 48.
- d) 118, 62 e 56.
2010
(MODELOS ATÔMICOS) C (UFRGS 2010) A partir do século XIX, a concepção da ideia de átomo passou a ser analisada sob uma nova perspectiva: a experimentação. Com base nos dados experimentais disponíveis, os cientistas faziam proposições a respeito da estrutura atômica. Cada nova teoria atômica tornava mais clara a compreensão da estrutura do átomo.
Assinale, no quadro a seguir, a alternativa que apresenta a correta associação entre o nome do cientista, a fundamentação de sua proposição e a estrutura atômica que propôs.
| Cientista | Fundamentação | Estrutura atômica | |
| a) | John Dalton | Experimentos com raios catódicos que foram interpretados como um feixe de partículas carregadas negativamente denominadas elétrons, os quais deviam fazer parte de todos os átomos. | O átomo deve ser um fluído homogêneo e quase esférico, com carga positiva, no qual estão dispersos uniformemente os elétrons. |
| b) | Niels Bohr | Leis ponderais que relacionavam entre si as massas de substâncias participantes de reações. | Os elétrons movimentam-se em torno do núcleo central positivo em órbitas específicas com níveis energéticos bem definidos. |
| c) | Ernest Rutherford | Experimentos envolvendo o fenômeno da radioatividade. | O átomo é constituído por um núcleo central positivo, muito pequeno em relação ao tamanho total do átomo, porém com grande massa, ao redor do qual orbitam os elétrons com carga negativa. |
| d) | Joseph Thomson | Princípios da teoria da mecânica quântica. | A matéria é descontínua e formada por minúsculas partículas indivisíveis denominadas átomos. |
| e) | Demócrito | Experimentos sobre condução de corrente elétrica em meio aquoso. | Os átomos são as unidades elementares da matéria e comportam-se como se fossem esferas maciças, indivisíveis e sem cargas. |
(MODELOS ATÔMICOS) A (ITA 2010) Historicamente, a teoria atômica recebeu várias contribuições de cientistas.
Assinale a opção que apresenta, na ordem cronológica CORRETA, os nomes de cientistas que são apontados como autores de modelos atômicos.
- a) Dalton, Thomson, Rutherford e Bohr.
- b) Thomson, Millikan, Dalton e Rutherford.
- c) Avogadro, Thomson, Bohr e Rutherford.
- d) Lavoisier, Proust, Gay-Lussac e Thomson.
- e) Rutherford, Dalton, Bohr e Avogadro.
(MODELOS ATÔMICOS) A (CEFET SC 2010) Toda a matéria é constituída de átomos. Atualmente essa afirmação suporta todo o desenvolvimento da química. Ao longo dos anos, foram propostos vários modelos para descrever o átomo. Em 1911, Rutherford realizou um experimento com o qual fazia um feixe de partículas alfa, de carga positiva, incidir sobre uma fina lâmina de ouro. Com esse experimento, observou que a maior parte dessas partículas atravessava a lâmina sem sofrer qualquer desvio.
Diante dessa evidência experimental, é correto afirmar que:
- a) o átomo não é maciço, mas contém muitos espaços vazios.
- b) o átomo é maciço e indivisível.
- c) os elétrons são partículas de carga negativa e se localizam no núcleo do átomo.
- d) o núcleo do átomo é constituído de cargas positivas e negativas.
- e) o átomo é formado por uma “massa” de carga positiva, “recheada” de partículas de carga negativa: os elétrons.
(MODELOS ATÔMICOS) D (CEFET MG 2010) Os recentes “apagões” verificados no Brasil, sobretudo no Rio de Janeiro, mostram a grande dependência da sociedade atual em relação a energia elétrica. O fenômeno da eletricidade só pode ser explicado, no final do século XIX, por meio de experiências em tubos, contendo um polo positivo e outro negativo, sob vácuo. Tais experimentos resultaram no modelo atômico de
- a) Bohr
- b) Dalton
- c) Rutherford
- d) Thomson
(MODELOS ATÔMICOS) D (UFPR 2010) Considere as seguintes afirmativas sobre o modelo atômico de Rutherford:
- O modelo atômico de Rutherford é também conhecido como modelo planetário do átomo.
- No modelo atômico, considera-se que elétrons de cargas negativas circundam em órbitas ao redor de um núcleo de carga positiva.
- Segundo Rutherford, a eletrosfera, local onde se encontram os elétrons, possui um diâmetro menor que o núcleo atômico.
- Na proposição do seu modelo atômico, Rutherford se baseou num experimento em que uma lamínula de ouro foi bombardeada por partículas alfa.
Assinale a alternativa correta.
- a) Somente a afirmativa 1 é verdadeira.
- b) Somente as afirmativas 3 e 4 são verdadeiras.
- c) Somente as afirmativas 1, 2 e 3 são verdadeiras.
- d) Somente as afirmativas 1, 2 e 4 são verdadeiras.
- e) As afirmativas 1, 2, 3 e 4 são verdadeiras.
(DISTRIBUIÇÃO ELETRÔNICA) A (CPS 2010) Considere os átomos neutros dos elementos químicos representados abaixo:
- oxigênio (Z = 8)
- argônio (Z = 18)
- cálcio (Z = 20)
- sódio (Z = 11)
Os dois elementos químicos que apresentam maior número de elétrons na camada de valência são
- a) I e II.
- b) I e III.
- c) II e III.
- d) II e IV.
- e) III e IV.
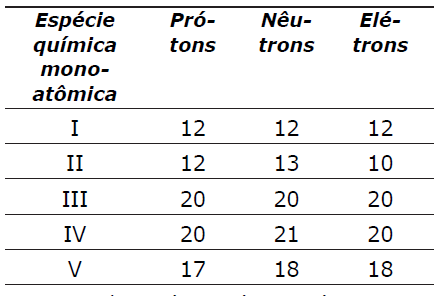
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) A (UTFPR 2010) Considere as espécies químicas monoatômicas indicadas na tabela abaixo.
Em relação às espécies químicas monoatômicas apresentadas na tabela, pode-se afirmar que:
- a) III e IV são de mesmo elemento químico.
- b) V é cátion.
- c) III é ânion.
- d) II é eletricamente neutro.
- e) I e II não são isótopos.
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) C (UNEMAT 2010) Isótopos radioativos do iodo têm grande importância na medicina. São usados no diagnóstico e no tratamento de problemas da tireoide. O isótopo do iodeto 53I– usado para esse fim apresenta os seguintes números de prótons, nêutrons e elétrons, respectivamente:
- a) 131; 53; 78
- b) 53; 53; 132
- c) 53; 78; 54
- d) 54; 131; 53
- e) 131; 78; 53
(MODELOS ATÔMICOS) B (UFJF – PISM 1 2010) Associe a coluna da esquerda, que descreve os modelos atômicos, com a da direita, em que se encontram os cientistas que as propuseram.
- a) A-I, B-II, C-III
- b) A-II, B-III, C-I
- c) A-III, B-I. C-II
- d) A-III, B-II, C-I
- e) A-II, B-I, C-III
2009
(MODELOS ATÔMICOS) D (PUC RJ 2009) Na produção de fogos de artifício, diferentes metais são misturados à pólvora para que os fogos, quando detonados, produzam cores variadas. Por exemplo, o sódio, o estrôncio e o cobre produzem, respectivamente, as cores amarela, vermelha e azul.
Se a localização dos elétrons num determinado nível depende da sua quantidade de energia, é INCORRETO afirmar que:
- a) quando a pólvora explode, a energia produzida excita os elétrons dos átomos desses metais, fazendo-os passar de níveis de menor energia para níveis de maior energia.
- b) os níveis de menor energia são aqueles mais próximos do núcleo, e os níveis de maior energia são aqueles mais distantes do núcleo.
- c) quando o elétron retorna para o estado fundamental, ele cede energia anteriormente recebida sob a forma de luz.
- d) a luminosidade colorida nos fogos de artifício não depende do salto de elétrons de um nível para outro.
- e) no laboratório, o estrôncio poderia ser identificado pela coloração vermelha quando este recebe o calor de uma chama.
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) C (ESPCEX 2009) Um elemento químico teórico M tem massa atômica igual a 24,31 u e apresenta os isótopos 24M, 25M e 26M. Considerando os números de massa dos isótopos iguais às massas atômicas e sabendo-se que a ocorrência do isótopo 25 é de 10,00%, a ocorrência do isótopo 26 é
- a) 31,35%
- b) 80,00%
- c) 10,50%
- d) 69,50%
- e) 46,89%
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) C (FGV 2009) Na figura, é representado o espectro de massa dos isótopos naturais do elemento gálio.
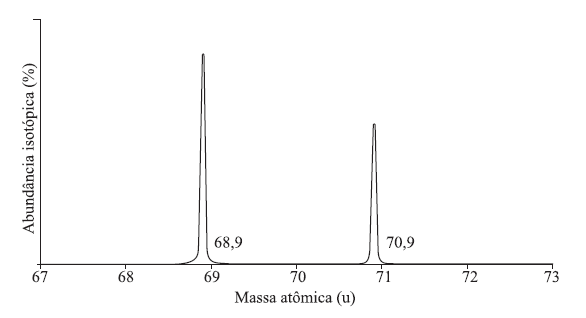 A abundância isotópica, em percentual inteiro, do isótopo do Ga-69, é:
A abundância isotópica, em percentual inteiro, do isótopo do Ga-69, é:
Dado: Ga = 69,7
- a) 50 %.
- b) 55 %.
- c) 60 %.
- d) 65 %.
- e) 70 %.
EXERCÍCIOS EXTRAS
(PRINCIPAIS CARACTERÍSTICAS DO ÁTOMO) A (CSA 1 – 2008 – BIA – UT2) O enxofre é uma substância simples cujas moléculas são formadas pela união de 8 átomos; logo, sua fórmula molecular é S8. Quando no estado sólido ele forma cristais do sistema rômbico ou monoclínico, conforme a figura a seguir.
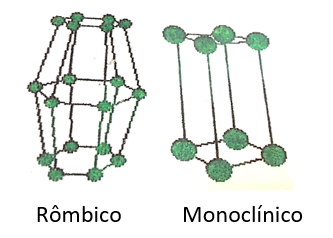 A respeito do enxofre rômbico e do enxofre monoclínico é correto afirmar que eles se constituem em:
A respeito do enxofre rômbico e do enxofre monoclínico é correto afirmar que eles se constituem em:
- a) formas alotrópicas do elemento químico enxofre, cujo símbolo é S.
- b) átomos isótopos do elemento químico enxofre, cujo símbolo é S.
- c) átomos isótopos do elemento químico enxofre, cujo símbolo é S8.
- d) formas alotrópicas do elemento químico enxofre, cujo símbolo é S8.
- e) formas isobáricas, da substância química enxofre, cujo símbolo é S.